
часть 1
.pdf
Из (1) вычтем (2):
P1 P2 V m1 m2 RT ,
или
P P1 P2 VRT m1 m2 VRT m . Учли, что масса израсходованного водорода:
m m1 m2 ,
или
m PV .
RT
Подставим численные значения:
m 0,4 10 6 25 10 3 2 10 3 8,3 10 3 (кг ). 8,31 290
Ответ: m 8,3 10 3 кг .
Домашнее задание №2
В цилиндр длиной l 1,6м (рис.5, а), заполненный воздухом при но р- мальном атмосферном давлении P0 начали медленно вдвигать поршень пл о-
щадью основания S 200см2 . Определить силу F , действующую на поршень, если его остановить на расстоянии 1 10см от дна цилиндра
(рис.5, б).
Дано: |
|
СИ: |
|
Решение: |
|
|
|
|
|
||
|
|
|
|
|
|
|
|||||
1,6м |
|
|
|
|
P0 |
|
|
P |
|||
|
|
|
|
|
|
0 |
|
||||
|
|
|
|
|
|
|
|
||||
P0 101325Па |
|
2 10 2 м2 |
|
|
|
|
|
|
F |
|
|
S 200см2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
1 10см |
|
0,1м |
|
ℓ |
|
|
|
ℓ1 |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
F ? |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
а) |
|
|
б) |
|||
|
|
|
|
|
|
|
|
рис.5 |
|||
21
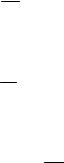
Механическое давление по определению: |
|
|
P |
F . |
(1) |
|
S |
|
Следовательно, сила F, с которой действуют на поршень:
F PS .
Процесс считаем долгим, т.е. температура неи зменна, тогда по закону Бойля - Мариотта:
P0V0 PV ,
или с учётом того, что объём цилиндра равен V Sоснования h :
P0 S P 1 S .
Откуда конечное давление Р:
P P0 ,
1
а ,следовательно, и сила F :
F P0 S .
1
Подставим численные значения:
F 101325 10,,61 2 10 2 32,3 103 32,3 103 (H ) .
Ответ: F 32,3кН .
Домашнее задание №3
Найти плотность газовой смеси водорода и кислорода, если их массовые доли 1 и 2 равны соответственно 1/9 и 8/ 9 . Давление P смеси равно 100кПа , температура T 300К .
22

|
Дано: |
|
|
СИ: |
||
1 |
2 10 3 |
|
кг |
|
||
моль |
||||||
|
|
|||||
2 |
32 10 3 |
кг |
|
|||
моль |
||||||
|
|
|
||||
1 |
1/ 9 |
|
|
|
||
2 |
8/9 |
|
|
|
||
P 100кПа |
|
|
105 Па |
|||
T300К
смеси ?
PV mсм RT ,
см
откуда объём:
Решение:
Плотность смеси:
смеси mсм m1 m2 |
|
1mсм 2 mсм |
|
V |
V |
|
V |
|
1 2 |
mсм , |
(1) |
|||
|
||||||
|
|
V |
|
|
|
|
|
|
где |
|
mсмеси m1 m2 |
- общая масса, |
|
i |
|
mi |
|
- массовая доля. Для нахождения |
||
|
mсм |
|||||
|
|
|
|
|
||
объема V запишем уравнение Менделеева - Клапейрона для смеси:
V |
mсм |
RT . |
(2) |
|
см |
P |
|
Найдем молярную массу смеси . |
|
По закону Дальтона давление смеси: |
|
P P1 P2 , |
(3) |
где P1 , P2 - парциальные давления компонентов смеси. |
|
Запишем уравнение Менделеева - Клапейрона для водорода и азота соответственно:
P1V m1 RT ,
1
P2V m2 RT .
2
Выразим давления смеси, водорода и азота и по дставим в (3):
mсм |
|
RT |
|
RT |
m |
|
|
m |
2 |
|
|
|
|
|
|
|
|
|
1 |
|
|
|
, |
||
|
|
|
|
|
|
|||||||
см |
|
V |
|
V |
|
|
|
|
M |
|
|
|
|
|
M |
1 |
|
2 |
|
|
|||||
сократим на RTV , тогда молярная масса смеси:
23
|
см |
|
|
|
mсм |
|
|
|
|
|
|
|
|
|
|
mсм |
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
1 |
2 |
|
. |
|
|
|
|||||||||||||||
|
|
m1 |
|
m2 |
|
|
1mсм |
|
2 mсм |
1 |
|
|
2 |
|
|
|
|
|
|
|
(4) |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
1 |
2 |
|
|
|
|
|
|
|
1 |
|
|
2 |
|
|
|
|
1 |
|
2 |
|
|
|
|
1 |
2 |
|
|
2 |
1 |
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
Подставим (2) в (1): |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
смеси |
|
1 |
2 |
|
mсм см P |
1 |
|
2 |
|
СМ P , |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
mсмRT |
|
RT |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
с учётом (4): |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
смеси |
|
1 |
2 |
|
|
|
|
|
|
|
|
1 2 |
|
|
|
|
|
P |
|
P 1 |
2 1 2 |
|
|
. |
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
RT |
|
|
|
1 2 2 1 |
|
|
RT 1 2 2 1 |
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
Подставим численные значения: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
10 |
5 |
|
|
1 |
|
8 |
|
10 |
3 |
|
32 |
|
10 |
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
9 |
9 |
2 |
|
|
|
|
|
|
|
|
|
|
6,4 |
|
|
|
|
|
кг |
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
смеси |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,481 |
|
|
. |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
3 |
|
|
|
8 |
|
|
|
|
|
|
3 |
|
|
13,296 |
|
|
|
|
м3 |
|
|||||||||
|
|
|
8,31 300 |
|
|
32 |
10 |
|
|
|
2 |
10 |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
9 |
|
|
|
9 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Ответ: смеси |
|
0,481 |
|
|
кг |
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
м3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Домашнее задание №4
Найти эффективную молекулярную массу воздуха, рассматривая его как
смесь азота (20 частей) и кислорода (80 частей). M r |
28 , M r |
32 . |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
o2 |
|
|
Дано: |
|
СИ: |
|
Решение: |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||||||||
M r 1 |
28 |
|
|
|
Из формулы (4) домашней задачи №3, моляр- |
|||||||||||
M r |
|
32 |
|
|
|
ная масса смеси: |
|
|
|
|
|
|
||||
2 |
|
|
|
|
|
mсм |
|
m1 |
m2 |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
m 0,2m |
|
|
|
см |
|
|
. |
|
||||||||
|
|
m1 |
m2 |
m1 |
|
|
||||||||||
1 |
|
|
|
|
|
|
|
|
|
m2 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
m2 0,8m |
|
|
|
|
1 |
2 |
|
1 |
|
2 |
|
|||||
k 10 |
3 кг |
|
|
|
Связь молярной массы и относительной мо- |
|||||||||||
|
моль |
|
|
|
лекулярной массы вещества: |
|
||||||||||
|
|
|
|
|
|
|
|
|||||||||
M rcм |
? |
|
|
|
Mr к . |
|
|
|
|
|
|
|||||
Тогда эффективная молекулярная масса возд уха: |
|
|
|
|
||||||||||||
24
M r |
к |
|
|
m1 m2 |
|
|
|
|
m1 m2 |
к , |
||||
m1 |
m2 |
|
|
|
m1 |
m2 |
||||||||
см |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
M r |
1 |
к |
M r |
к |
М r |
|
М r |
|
||||
|
|
|
|
|
2 |
|
|
|
|
1 |
2 |
|
||
окончательно:
M r |
m1 |
m2 |
. |
|
m1 |
|
|||
см |
m2 |
|||
|
|
|
|
|
|
|
|
|
|
|
М r |
|
М r |
|
|
1 |
2 |
|
|
Подставим численные значения:
M r |
|
0,2m 0,8m |
|
28 32 |
|
896 |
31,1. |
||
0,2m |
0,8m |
0,2 32 0,8 28 |
28,8 |
||||||
см |
|
|
|
|
|||||
|
|
32 |
|
|
|
|
|
||
|
|
28 |
|
|
|
|
|
||
Ответ: M r |
31,1. |
|
|
|
|
|
|||
|
|
см |
|
|
|
|
|
|
|
Занятие № 2 «Закон Авогадро. Масса и размер молекул. Количество в е- щества. Основное уравнение кинетической теории газов. Энергия мол е- кул. Скорость молекул»
|
|
|
Рекомендуемое задание № 1 |
|
|||||
В баллоне вместимостью V 5л содержится кислород массой |
m 20г . Оп- |
||||||||
ределить концентрацию n молекул в баллоне. |
|
|
|
|
|||||
Дано: |
|
СИ: |
|
Решение: |
|
|
|
|
|
|
|
|
|
|
|
||||
V 5л |
|
5 10 3 м3 |
|
Основное |
уравнение |
кинетической |
|||
m 20г |
|
2 10 2 кг |
|
теории газов: |
|
|
|
|
|
32 10 3 |
кг |
|
|
|
P |
2 n |
|
. |
(1) |
|
|
|
п |
||||||
моль |
|
|
|||||||
|
|
|
|
|
3 |
|
|
|
|
n ? |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Средняя кинетическая энергия поступательного движения молекулы:
|
|
3 kT . |
(2) |
п |
|||
|
|
2 |
|
25

Подставим (2) в (1) получим зависимость давления газа от концентрации молекул и температуры:
|
|
|
P n k Т . |
(3) |
||
Откуда концентрация молекул: |
|
|
|
|||
|
|
|
n |
P |
. |
(4) |
|
|
|||||
|
|
|
|
k T |
|
|
Уравнение Менделеева – Клапейрона: |
|
|||||
P V m |
R T , |
|
|
|
||
|
|
|
|
|
|
|
выразим давление: |
|
|
|
|||
P m R T . |
|
|
|
|||
V |
|
|
|
|||
Подставим в (4): |
|
|
|
|||
n mRT |
|
mR |
. |
|
|
|
|
|
|
|
|||
VkT |
|
Vk |
|
|
|
|
Постоянная Больцмана, число Авогадро и универсальная газовая постоянная
связаны следующим соотношением:
k Na R . |
(5) |
Тогда:
Na Rk ,
следовательно, концентрация молекул:
n m N a .V
Подставим численные значения:
n 2 10 2 6,02 1023 0,07525 1027 7,525 1019 106 7,525 1019 (м 3 ) . 32 10 3 5 10 3
Ответ: n 7,525 1019 м 3 .
26
Рекомендуемое задание № 2
Определить молярную массу и массу m1 одной молекулы следующих га-
зов: 1) кислорода, 2) азота, 3) окиси азота |
NO . |
|
|
|
||||||||||
|
Дано: |
|
СИ: |
|
|
|
Решение: |
|
|
|
||||
|
|
|
|
|
|
|
||||||||
ArO |
16 |
|
|
|
|
|
|
Атомные массы |
Ar взяты из таблицы хими- |
|||||
ArN |
14 |
|
|
|
|
ческих элементов Д.И. Менделеева. Относитель- |
||||||||
k 10 3 |
кг |
|
|
|
ные молекулярные массы найдем из соотношения: |
|||||||||
|
|
|
|
|
M r n Ar , |
|
|
|
||||||
моль |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
где n – число атомов в молекуле. Молярная мас- |
||||||||
O2 |
? |
|
|
|
|
|||||||||
N 2 |
? |
|
|
|
|
са: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
M r |
k . |
|
|
|
||||
NO |
? |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
Тогда: |
|
|
|
|
|
|
||||
mO2 |
? |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
O |
|
M r |
k n0 Ar |
k |
||||||
|
|
|
|
|
|
2 |
||||||||
mN 2 |
? |
|
|
|
|
|
O 2 |
|
|
|
O 2 |
|||
|
|
|
|
|
|
|
3 |
|
3 |
|
кг |
|||
mNO |
? |
|
|
|
|
2 |
16 10 |
|
|
32 10 |
|
|
. |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
моль |
|||
.N |
|
M r |
|
k n0 |
Ar |
|
k 2 14 |
10 |
|
3 |
28 |
10 |
|
3 |
|
|||
|
|
|
|
|
|
|||||||||||||
|
|
2 |
|
|
N 2 |
|
|
|
N 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
NO |
M |
rNO |
k n |
0 |
A |
|
k 14 16 10 3 30 10 |
||||||||||
|
|
|
rNO |
|
|
|
|
|
|
|
|
|
||||||
Массу одной молекулы найдем из соотношения:
m1 N a . Тогда:
m1 |
|
|
|
, |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
N a |
|
|
|
|
|
|
|
|
|
|
|
|||
m |
|
|
|
O |
2 |
|
|
|
32 10 3 |
|
5,3 10 26 |
(кг), |
|||||
O2 |
|
N a |
|
6,02 |
10 |
23 |
|
||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
m |
|
|
|
N |
2 |
|
|
|
28 10 3 |
|
4,65 10 26 (кг) , |
||||||
|
|
N a |
|
6,02 |
10 |
|
|
||||||||||
|
N2 |
|
|
|
|
23 |
|
|
|
||||||||
|
кг |
|
|
||
|
|
|
|
. |
|
|
|
|
|
||
моль |
|||||
3 |
|
кг |
|||
|
|
|
|
|
. |
|
|
|
|
||
|
моль |
||||
27

mNO |
|
NO |
|
|
30 10 3 |
|
4,98 10 26 (кг) . |
|
|
|
|
|
|
|||||
|
|
6,02 |
10 |
|
|
|
|
|
|
|
|
|||||||
|
N a |
23 |
|
|
|
|
|
|
|
|
|
|
||||||
Ответ: O2 |
32 10 |
3 |
кг |
, |
.N2 28 10 |
3 |
кг |
, |
NO 30 10 3 |
кг |
, |
|||||||
моль |
моль |
моль |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
mO2 5,3 10 26 кг, |
mN 2 |
4,65 10 26 |
кг, mNO 4,98 10 26 кг. |
|
|
|
||||||||||||
Рекомендуемое задание № 3
В баллоне вместимостью V 3л находится кислород массой m 4г . Опреде-
лить количество вещества |
газа и концентрацию n его молекул. |
|||||||||
Дано: |
|
|
СИ: |
|
Решение: |
|
|
|||
|
|
|
|
|
||||||
V 3л |
|
|
3 10 3 м3 |
|
Количество вещества: |
|||||
m 4г |
|
|
4 10 |
3 |
кг |
|
m |
4 10 |
3 |
0,125(моль). |
|
|
|
|
|
|
|
|
|||
|
кг |
|
|
|
|
|
|
|
|
|
O2 32 10 3 |
|
|
|
32 10 3 |
|
|||||
моль |
|
|
|
|
Зависимость давления газа от концен- |
|||||
|
|
|
|
|
||||||
? |
|
|
|
|
|
|
трации молекул и температуры: |
|||
n ? |
|
|
|
|
|
|
P n k Т . |
|
|
|
Откуда концентрация: |
|
|
|
|
|
|
|
|||
n kTP .
Уравнение Менделеева – Клапейрона:
P V m R T , откуда давление:
P m R T .
V
Тогда концентрация:
n |
mRТ |
|
mR |
|
m Na |
, |
|
VkТ |
Vk |
V |
|||||
|
|
|
|
учли формулу: k Na R . Подставим численные значения:
28

n 4 10 3 6,02 1023 0,251 1026(м 3 ) . 32 10 3 3 10 3
Ответ: 0,125моль, n 2,51 1025 м 3 .
Рекомендуемое задание № 4
Сколько молекул газа содержится в баллоне вместимостью V 30л при температуре T 300К и давлении P 5МПа ?
Дано: |
|
СИ: |
|
Решение: |
|
|
|||
V 30л |
|
3 10 2 м3 |
|
1й способ. |
T 300К |
|
|
|
Зависимость давления газа от концентрации м о- |
P 5МПа |
|
5 106 Па |
|
лекул и температуры: |
|
|
|
|
P n k Т . |
N ? |
|
|
|
|
|
|
|
|
Концентрация молекул: |
|
|
|
|
n VN , тогда давление:
P N k T ,
V
откуда число молекул:
NP V . k T
Подставим численные значения:
N |
5 106 |
3 10 2 |
3,62 10 |
25 |
. |
1,38 10 23 300 |
|
||||
|
|
|
|
||
2й способ.
Количество вещества по определению:
m N .
N a
Уравнение Менделеева – Клапейрона:
P V |
m R T |
R T , |
|
|
|
29

откуда количество вещества:
P V
R T
или
N |
|
P V . |
|
||
N a |
R T |
|
Число молекул:
N P V N a .
R T
Учитывая формулу: k Na R ,
1k NRa ,
NP V . k T
Получили ту же самую конечную формулу. Ответ: N 3,62 1025.
Рекомендуемое задание № 5
Давление P газа равно 1мПа , концентрация n его молекул равна 1010 см 3 .
Определить: 1) температуру |
T газа; 2) среднюю кинетическую энергию |
|
|
||||||||
п |
|||||||||||
поступательного движения молекул газа. |
|
|
|
|
|||||||
|
Дано: |
|
СИ: |
|
|
Решение: |
|||||
|
|
||||||||||
P 1мПа |
|
10 3 Па |
|
|
1. Зависимость давления газа от концен- |
||||||
n 1010 см 3 |
|
1016 м 3 |
|
|
трации молекул и температуры: |
||||||
1. T ? |
|
|
|
|
P n k Т , |
||||||
|
|
|
|
|
|
|
откуда температура: |
||||
2. п ? |
|
|
|
|
|||||||
|
|
|
|
|
P |
|
|
|
|||
|
|
|
|
|
|
|
T |
. |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
n k |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
Подставим численные значения:
30
