
- •2.Строение и уровни структурной организации белков
- •3. Найти самой4. Определение общего белка в сыворотке крови по биуретовой реакции
- •Гипопротеинемия
- •Азотистые основания.
- •Нуклеозиды.
- •2. Оксокислоты
- •Химические свойства.
- •1.3. Биологически важные гидроксикислоты.
- •2. Оксокислоты
- •2.2. Химические свойства
- •1. Протеиногенные аминокислоты
- •1. "Альдегиды. Кетоны".
- •Осмотическое давление
- •Критерии ароматичности[править | править вики-текст]
- •4. Определение общего белка в сыворотке крови по биуретовой реакции
- •Гипопротеинемия
- •1. Конкурентное ингибирование
- •2. Неконкурентное ингибирование
- •1. Специфические и неспецифические ингибиторы
- •Обратимое ингибирование
- •Неконкурентное ингибирование
- •Ингибирование субстратом[править | править вики-текст]
- •Аллостерическое ингибирование[править | править вики-текст]
- •Значения pH в растворах различной кислотности[править | править вики-текст]
- •Методы определения значения pH[править | править вики-текст]
- •3.Лекарственные препараты как конкурентные ингибиторы
- •2. Оксокислоты
- •Химические свойства.
- •1.3. Биологически важные гидроксикислоты.
- •2. Оксокислоты
- •2.2. Химические свойства
- •Причины ацидоза[править | править вики-текст]
- •Классификации ацидоза[править | править вики-текст]
- •Лечение[править | править вики-текст]
- •Классификация[править | править вики-текст]
- •Этиология[править | править вики-текст]
- •Газовый (респирато́рный) алкалоз[править | править вики-текст]
- •Негазовый алкалоз[править | править вики-текст]
- •Смешанный алкалоз[править | править вики-текст]
- •Патогенез[править | править вики-текст]
- •Лечение[править | править вики-текст]
- •1 Аксиома. Изменение рСо2 крови на 10 мм рт.Ст. Обусловливает реципрокное изменение pH на 0,08.
- •2 Аксиома. Изменение pH на 0,15 является результатом изменения концентрации буферных оснований на 10 ммоль/л.
- •1. 1. Протеиногенные аминокислоты
- •10) Запасная (резервная) функция
- •11) Моторная (двигательная) функция
- •Классификация по типу строения
- •Простые и сложные белки
1. Протеиногенные аминокислоты
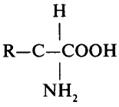
Структурными блоками или мономерами белков служат α-аминокислоты L-ряда (см. табл. 4). Общая формула α-аминокислот имеет следующий вид:
14
Выделенное звено формулы α-аминокислоты является неизменным для всех протеиногенных аминокислот, его можно назватьаминокислотным блоком. Аминокислоты различаются по структуре бокового радикала (R), а следовательно, и по физико-химическим свойствам, присущим этим радикалам.
По кислотно-основным свойствам аминокислоты делят в зависимости от физико-химических свойств бокового радикала на три группы: кислые, основные и нейтральные.
К кислым относятся аминокислоты с карбоксильными группами в боковом радикале: аспарагиновая и глутаминовая кислоты. Косновным относятся аминокислоты лизин, аргинин и гистидин, имеющие в боковом радикале группировку с основными свойствами: аминогруппу, гуанидиновую и имидазольную группы. Все остальные аминокислоты - нейтральные, так как их боковой радикал не проявляет ни кислых, ни основных свойств.
Следовательно, аминокислоты имеют суммарный нулевой, положительный или отрицательный заряд, зависящий от рН-среды. Значение рН-среды, при котором заряд аминокислоты равен нулю, называется изоэлектрической точкой. Изоэлектрическая точка отражает кислотно-основные свойства разных групп в аминокислотах и является одной из важных констант, характеризующих аминокислоту.
По биологическому значению аминокислоты подразделяются на заменимые, полузаменимые и незаменимые.
Заменимые аминокислоты синтезируются в организме человека в достаточном количестве. К ним относятся глицин, аланин, серин, цистеин, тирозин, аспарагиновая кислота, глутаминовая кислота, аспарагин, глутамин.
Полузаменимые аминокислоты образуются в организме, но в недостаточном количестве, поэтому их недостаток должен восполняться белковой пищей. Для организма человека такими аминокислотами являются тирозин, аргинин, гистидин.
Незаменимые аминокислоты в организме человека не синтезируются, поэтому они должны поступать с пищей. Незаменимых аминокислот восемь: валин, лейцин, изолейцин, треонин, лизин, метионин, фенилаланин, триптофан.
Аминокислотный состав белков определяется не доступностью или незаменимостью той или иной аминокислоты, а назначением белка, его биологической функцией. В настоящее время определен аминокислотный состав многих сотен белков.
Примерами олигомерных белков могут служить эритроцитарный белок гемоглобин, фермент фосфофруктокиназа и многие другие.
Более подробно структурная организация и функционирование олигомерных белков будут рассмотрены в следующей теме на примере гемоглобина (рисунок 2.3).
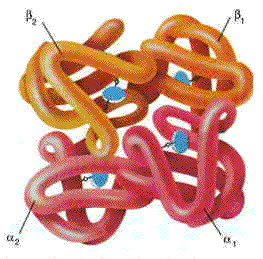
Рисунок 2.3. Пространственное строение гемоглобина. В состав его молекулы входят четыре попарно одинаковые субъединицы, обозначаемые буквами α и β. Небелковая часть гемоглобина — гем — показана синим цветом.
2.Смотри в учебнике
3
в уч.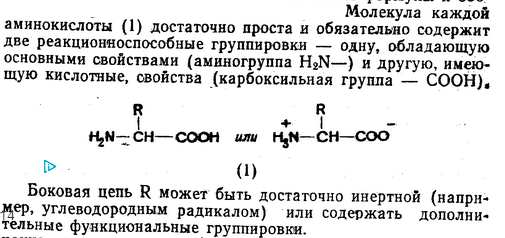
4.
нейтр, а надо основный 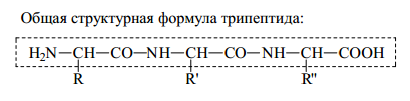
БИЛЕТ 8
1. "Альдегиды. Кетоны".
Альдегиды -
органические вещества, молекулы которых
содержат карбонильную группу —![]() —,
связанную с атомом водорода и углеводородным
радикалом.
Общая формула альдегидов
—,
связанную с атомом водорода и углеводородным
радикалом.
Общая формула альдегидов![]() или
R—CHO. Функциональная группа альдегидов
(—CHO) называется альдегидной
группой.Кетоны -
органические вещества, молекулы которых
содержат карбонильную группу —
или
R—CHO. Функциональная группа альдегидов
(—CHO) называется альдегидной
группой.Кетоны -
органические вещества, молекулы которых
содержат карбонильную группу —![]() —,
связанную с двумя углеводородными
радикалами.
Общая формула кетонов
—,
связанную с двумя углеводородными
радикалами.
Общая формула кетонов![]() или
R—CO—R'.
Альдегиды и кетоны называются
карбонильными соединениями, их общая
формула - CnH2nO.
или
R—CO—R'.
Альдегиды и кетоны называются
карбонильными соединениями, их общая
формула - CnH2nO.
Изомеры и гомологи
|
г о м о л о г и |
HCHO метаналь (формальдегид, муравьиный альдегид) |
| |
|
CH3CHO этаналь (ацетальдегид, уксусный альдегид) |
| ||
|
CH3CH2CHO пропаналь (пропионовый альдегид) |
|
CH3—CO—CH3 пропанон (ацетон) | |
|
CH3CH2CH2CHO бутаналь (масляный альдегид) |
|
CH3—CO—CH2CH3 бутанон (метилэтилкетон) | |
|
|
и з о м е р ы | ||
В молекулах альдегидов, а тем более кетонов, в отличие от спиртов нет атомов водорода со значительным положительным частичным зарядом, поэтому между молекулами как альдегидов, так и кетонов нет водородных связей.
Алгоритм составления названий альдегидов
Найдите главную углеродную цепь - это самая длинная цепь атомов углерода, включающая атом углерода альдегидной группы.
Пронумеруйте атомы углерода в главной цепи, начиная с атома углерода альдегидной группы.
Назовите соединение по алгоритму для углеводородов.
В конце названия допишите суффикс -аль.
Физические
свойства: формальдегид - газ с удушливым
запахом, растворим в воде (с молекулами
воды водородные связи образуются, 40
%-ный водный раствор называется формалином
с увеличением температуры растворимость
уменьшается); ацетальдегид - бесцветная
легкокипящая жидкость с фруктовым
запахом, растворим в воде; ацетон -
бесцветная жидкость с резким запахом,
растворим в воде.
В ряду
алканы ![]() альдегиды
(кетоны)
альдегиды
(кетоны)![]() спирты
растворимость в воде и температура
кипения увеличивается.
спирты
растворимость в воде и температура
кипения увеличивается.
Химические свойства
Химические
свойства альдегидов и кетонов в
значительной степени обусловлены
наличием в их молекулах сильно полярной
карбонильной группы (связь ![]() поляризована
в сторону атома кислорода). Чем больше
частичный заряд (
поляризована
в сторону атома кислорода). Чем больше
частичный заряд (![]() +)
на атоме углерода этой группы, тем выше
активность соединения.
+)
на атоме углерода этой группы, тем выше
активность соединения.
Горение:
2CH3CHO
+ 5O2 ![]() 4CO2 +
4H2O
2CH3COCH3 +
9O2
4CO2 +
4H2O
2CH3COCH3 +
9O2 ![]() 6CO2 +
6H2O
6CO2 +
6H2O
Присоединение (по двойной связи карбонильной группы). В ряду HCHO
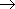 RCHO
RCHO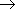 RCOR'
склонность к реакциям присоединения
уменьшается. Это связано с наличием и
числом углеводородных радикалов,
связанных с атомом углерода карбонильной
группы.
а) Гидрирование
(восстановление водородом):
RCOR'
склонность к реакциям присоединения
уменьшается. Это связано с наличием и
числом углеводородных радикалов,
связанных с атомом углерода карбонильной
группы.
а) Гидрирование
(восстановление водородом):
HCHO
+ H2 ![]() CH3OH
CH3—CO—CH3 +
H2
CH3OH
CH3—CO—CH3 +
H2 ![]() CH3—CH(OH)—CH3
CH3—CH(OH)—CH3
Из альдегидов при этом получаются первичные спирты, а из кетонов - вторичные.
Окисление:
CH3CHO
+ Ag2O ![]() 2Ag
2Ag![]() +
CH3COOH
(реакция "серебряного зеркала" -
качественная реакция)
HCHO + 2Cu(OH)2
+
CH3COOH
(реакция "серебряного зеркала" -
качественная реакция)
HCHO + 2Cu(OH)2 ![]() 2H2O
+ Cu2O
2H2O
+ Cu2O![]() +
HCOOH (образуется красный осадок -
качественная реакция)
+
HCOOH (образуется красный осадок -
качественная реакция)
Кетоны слабыми окислителями не окисляются.
Замещение атомов водорода в углеводородном радикале (замещение происходит в
 -положение,
т. е. замещается атом водорода у 2-го
атома углерода):
-положение,
т. е. замещается атом водорода у 2-го
атома углерода):
|
3 |
2( |
1 |
|
|
CH3 |
—CH2 |
—CHO |
+
Cl2 |
СМ ПО УЧЕБНИКУ ХИМ. СВОЙСТВА – РЕАКЦ ОК-Я, ВОССТ, ДИСМУТАЦИИ, АЛЬДОЛЬНОЙ КОНДЕНСАЦИИ, ОБР АЦЕТАЛЕЙ, ПОЛУАЦЕТАЛЕЙ, ПРИСОЕД-ОТЩИПЛЕНИЯ
2. вода - активный участник молекулярных взаимодействий в биологических системах.
1. Молекулы воды полярны. Они имеют не линейную, а треугольную форму, вследствие чего распределение заряда оказывается асимметричным. Ядро атома кислорода оттягивает электроны от атомов водорода, и вокруг последних возникает область с общим положительным зарядом. Если вокруг атома кислорода описать тетраэдр так, чтобы в двух его углах находились атомы водорода, то два других угла тетраэдра окажутся электроотрицательными. Таким образом, молекула воды представляет собой полярную структуру
2. Молекулы воды обладают высоким сродством друг к другу. Группа молекул воды образует конгломерат, в котором область положительного заряда отдельной молекулы ориентируется относительно области с отрицательным зарядом одной из близлежащих молекул. Каждая из двух областей с отрицательным зарядом притягивает протон от соседней молекулы. В то же время их собственные протоны притягивают кислородный конец соседней молекулы. Таким образом, каждый атом кисло
Вода ведет себя как конкурент при образовании водородных связей.
рода является центром тетраэдра, образованного другими кислородами, причем расстояние О—О составляет 2,76 А.
Регуляция каталитической активности ферментов ассоциацией/диссоциацией протомеров Протеинкиназы - группа ферментов, катализирующих перенос остатка фосфорной кислоты с АТФ на специфические ОН-группы аминокислотных остатков белков (вызывают фосфорилирование белков). Механизмы активации различных протеинкиназ неодинаковы. В качестве примера регуляции каталитической активности ферментов ассоциацией или диссоциацией протомеров можно привести регуляцию активности фермента Протеинкиназы А.
Протеинкиназа А (цАМФ-зависимая) состоит из 4 субъединиц 2 типов: 2 регуляторных (R) и 2 каталитических (С). Такой тетрамер не обладает каталитической активностью. Регуляторные субъединицы имеют участки связывания для циклического 3',5'-АМФ (цАМФ), по 2 на каждую субъединицу. Присоединение 4 молекул цАМФ к 2 регуляторным субъединицам приводит к изменению конфор-мации регуляторных протомеров и к диссоциации тетрамерного комплекса, при этом высвобождаются 2 активные каталитические субъединицы (рис. 2-32). Такой механизм регуляции обратим. Отщепление молекул цАМФ от регуляторных субъединиц приведёт к ассоциации регуляторных и каталитических субъединиц Протеинкиназы А с образованием неактивного комплекса.
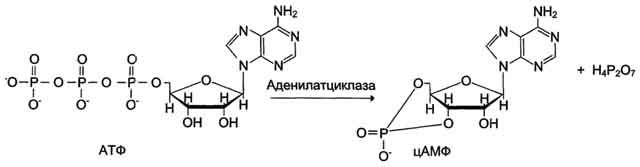
4 Почему миоглобин не способен транспортировать кислород, но зато активно его запасает? Для миоглобина изотерма адсорбции кислорода имеет форму гиперболы. Давление О2 в ткани, окружающей легочные капилляры, составляет 100 мм рт.ст., поэтому миоглобин в легких мог бы весьма эффективно насыщаться кислородом. В венозной крови Р О2 равно 40 мм рт. ст., а в активно работающей мышце - 20 мм рт.ст. Но даже при парциальном давлении 20 мм рт. ст. степень насыщения миоглобина кислородом будет весьма значительна, и поэтому миоглобин не может служить транспортной молекулой для доставки О2 от легких к периферическим тканям. Однако при кислородном голодании, которым сопровождается тяжелая физическая работа, парциальное давление О2 в тканях может понизиться и до 5 мм рт.ст.; при столь низком давлении миоглобин легко отдает кислород, обеспечивая тем самым окислительный синтез АТФ в митохондриях мышечных клеток.
Кинетика оксигенирования гемоглобина коренным образом отличается от кинетики оксигенированиямиоглобина. Кривая насыщения гемоглобина О2 имеет сигмоидальную форму. Т.о., способность гемоглобина связывать О2 зависит от того, содержатся ли в данном тетрамере другие молекулы О2. Если да, то последующие молекулы О2 присоединяются легче. Для гемоглобина характерна кинетика кооперативного связывания, благодаря которой он связывает максимальное количество О2 в легких и отдает максимальное количество О2 при тех значениях Р О2 , которые имеют место в периферических тканях.
Сродство гемоглобинов к О2 характеризуется величиной Р50- значением парциального давления О2, при котором наблюдается полунасыщение гемоглобина кислородом. Например, для HbA Р50 = 26 мм рт.ст., а для HbF - 20 мм рт. ст. Благодаря этой разнице гемоглобин F отбирает кислород у HbA, находящегося в плацентарной крови.
Молекулярная основа эффекта Бора
Протоны, ответственные за эффект Бора, высвобождаются в результате разрушения солевых мостиков, которым сопровождается связывание О2, они отсоединяются от остатков His (146) в -цепях гемоглобина. Наоборот, при высвобождении кислорода вновь формируется структура с солевыми мостиками, при образовании которых происходит присоединение протонов к остаткам His.
БИЛЕТ 9
1. СМ В УЧ
2. СОЛЬВАТАЦИЯ, взаимод. молекул растворенного в-ва (или их ассоциатов) с молекулами р-рителя. Приводит к изменению св-в молекул в р-ре (в сравнении со св-вами газовой фазы), влияет на все физ. и физ.-хим. процессы, протекающие в р-рах, в т.ч. определяет скорость реакций в растворах и положение равновесия, а в ряде случаев и их механизм. Сольватация в водных средах часто наз. гидратацией. Наиб. интенсивна сольватация ионов в растворах электролитов.
Сольватация состоит в том, что молекула растворенного в-ва оказывается окруженной сольватной оболочкой, состоящей из более или менее тесно связанных с ней молекул р-рителя. В результате сольватации образуются сольваты-мол. образования постоянного или переменного состава. Время жизни соль-ватов определяется характером и интенсивностью межмолекулярных взаимодействий; даже в случае сильного взаимод. время жизни отдельного сольвата мало из-за непрерывного обмена частицами в сольватной оболочке. В соответствии с типами межмол. взаимод. выделяют неспецифическую и специфическую сольватацию. Неспецифическая сольватация обусловлена ван-дер-ваальсовыми взаимод., специфическая сольватация проявляется гл. обр. вследствие электростатич. взаимод., коор-динац. и водородных связей.
См в уч
3. см в уч
4. –
БИЛЕТ 10
1. В молекулах алифатических соединений, содержащих сопряженные связи, а также в ароматических молекулахвзаимное влияние атомов осуществляется преимущественно другим путем, качественно отличающимся отиндукционного взаимного влияния атомов. Для того чтобы уяснить характер такого влияния, рассмотрим, например, свойства систем с сопряженными двойными связями в жирных соединениях.
Среди химических особенностей систем с двумя сопряженными двойными связями наиболее характерным является протекание реакций 1,4-присоединения. В таких реакциях атакующие молекулы или их части (ионы, радикалы) присоединяются к крайним (первому и четвертому) атомам сопряженной системы, причем между вторым и третьиматомами возникает новая двойная связь, например:

Кроме того, в целом такие системы более реакционноспособ-ны (в первую очередь за счет повышенной реакционной способности первого и четвертого атомов) и могут вступать в реакции, не свойственные молекулам с изолированными двойными связями. Таково восстановление систем
![]()
водородом в момент выделения, присоединение к системам С=С—С=С щелочных металлов и ихметаллоорганических соединений, присоединение анионов CN-, SO3H- и R- (при действии RMgX) к четвертому (углеродному) атому системы О=С—С=С и др.
Таким образом, химические свойства сопряженных систем показывают, что содержащиеся в них двойные связиотличаются от изолированных двойных связей. Это отличие обусловлено особым характером взаимного влияния ненасыщенных атомов сопряженных систем. Такой специфический вид взаимного влияния атомов, качественно отличный от индукционного влияния, может быть интерпретирован как результат взаимодействия π-электронов двух или нескольких сопряженных двойных связей. Вследствие этого такой вид взаимного влияния атомов предложено называть сопряжением связей.
Молекулы с сопряженными двойными связями характеризуются и некоторыми физическими особенностями, например повышенной энергией образования сравнительно с молекулами, имеющими изолированные двойные связи, некоторым выравниванием межатомных расстояний и высокой поляризуемостью электронной системы связей. Физические показатели такого рода характеризуют строение нереагирующей молекулы, а следовательно, Они указывают на то, что сопряжение двойных связей представляет собой фактор, находящий свое отражение и в нереагирующей молекуле. Результат сопряжения связей в нереа-лирующей молекуле предложено называть статическим эффектом сопряжения или мезомерным эффектом.
Как мы уже указывали, природу сопряжения двойных связей можно интерпретировать как результат большой подвижности π-электронов, смещение которых происходит во всей сопряженной системе в делом. Роль π-злектронной пары одной из связей сопряженной системы может играть необобщенная пара р-электронов такихатомов, как N, О, S и т. п. Для того чтобы отразить этот вид взаимного влияния в структурных формулах, смещения π-электронов обычно отмечают изогнутыми стрелками, проведенными, например, от кратной связи С = С к простой связи С—С или от атома с неподеленной парой р-электронов к простой связи в направлении смещения:

Рассмотрим в качестве примера молекулу ацетамида, в которой неподеленная пара электронов атома азотанаходится в
сопряжении с π-связью:
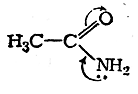
Распределение электронной плотности в молекуле ацетамида определяется конкуренцией атомов О и N в соответствии с их сродством к электрону. Смещение неподеленной пары электронов атома азота к атому углеродакарбонильной группы является причиной понижения основных свойств аминогруппы ацетамида сравнительно саминогруппой в амине
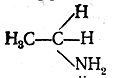
и вместе с тем причиной понижения электрофильной реакционной способности карбонильной группы (точнее —атома углерода этой группы) сравнительно, например, с карбонильной группой в альдегидах:
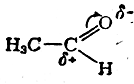
Этот пример ясно показывает, что под термином «сопряжение связей» в сущности понимается определенного рода взаимодействие электронных систем атомов, в первую очередь такое взаимодействие, в котором участвуют валентные электроны.
Представления о сопряжении связей являются дальнейшим развитием проблемы взаимного влияния атомов в молекулах. С их помощью удается уже в настоящее время понять и объединить большой круг явлений органической химии, казавшихся ранее совершенно обособленными и загадочными.
Необходимо еще раз отметить, что сопряжение связей следует понимать как проявление определенного рода взаимного влияния атомов.
Представления о сопряжении связей позволяет вскрыть характер взаимного влияния атомов и систематизировать имеющийся фактический материал. Было бы глубоко ошибочным отрывать вопрос сопряжения связей от проблемы взаимного влияния атомов.
Химическая связь есть только форма взаимодействия ато-моз и, естественно, не может рассматриваться независимо от самих атомов.
ОПРЯЖЕНИЕ СВЯЗЕЙ (конъюгация связей), чередование простых и кратных связей в структурной ф-ле соед. (напр., в 1,3-бутадиене СН2=СН—СН=СН2). В широком смысле понятие сопряжение связей охватывает также гомосопряжение (в альтернирующую последовательность простых и двойных связей включается один или большее число sp3-гибридизованных атомов. например соед. ф-лы I), спиросопряжение (в ненасыщ. спирановых структурах, например II), сверхсопряжение (гиперконъюгация)-сопряжение кратных (или группы простых) связей с группой s-связей одного атомного центра; III, IV.
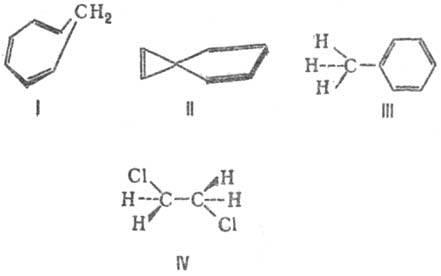
Расширение толкования С. с. связано также с представлениями о сопряжении не только неск. связей, но и кратных (или простых) связей с любым атомным центром-как обладающим одним электроном или неподеленной электронной парой(С-, О, NR2 и др., например V), так и центром с вакантной орбиталью (С+ , В, А1 и др., например VI и VII). Структурная единица, содержащая сопряженные связи, наз. сопряженной системой.
|
|
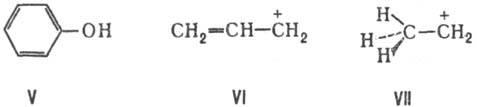
<p.Квантовая химия рассматривает сопряжение связей как взаимод. между орбиталями отдельных фрагментов молекулы, которое может осуществляться по тому или иному механизму. Напр., s-сопряжению соответствует взаимод. орбиталей простых связей, p-сопряжению - взаимод. орбиталей кратных связей. s-C. с. всегда присутствует в любой молекуле, состоящей из трех или большего числа атомов. В то же время наблюдаемые свойстваполиенови аннуленов описываются исходя из представлений как s-, так и p-сопряжения.
сопряжение связейне обязательно означает неприменимость модели локализованных связей к рассматриваемой молекуле. Так, электронная заселенность локализованных мол. орбиталей вне s-связей не превышает 1%. Так же хорошо локализованы и p-связи в сопряженных неароматич. системах (особенно когда учитывается альтернирование связей). Так, в линейных полиенах заселенность вне двухцентровых связей ок. 2%. Такие сопряженные системы описываются одной резонансной структурой со связями только между соседними атомами и без разделения формальных зарядов (см.Резонанса теория), а их коллективные свойства удается рассматривать в рамках аддитивных моделей.
В то же время в ароматич. и некоторых др. системах, которые наилучшим образом описываются суперпозицией резонансных структур и где доли локализованных мол. орбиталей имеют большие веса вне связей (напр., в бензоле ок. 13%), сопряжение связейобычно отождествляется с делокализацией связей. Экспериментально наблюдаемые коллективные свойства таких сопряженных систем в принципе нельзя представить в виде аддитивных ф-ций свойств связей.
Наиб. существенной особенностью сопряженных систем с делокализованными связями является их повыш. термо-динамич. устойчивость. В ароматич. системах теплоты образования значительно выше, чем значения, найденные с учетом аддитивности локальных параметров, а связи характеризуются полной выравненностью длин (см.Ароматичность). Количеств. мера повыш. термодинамич. устойчивости таких систем-энергия резонанса (сопряжения, дело-кализации). В сопряженных системах правилам аддитивности не подчиняются также параметры ЙК спектров, величины дипольных моментов и поляризуемости, диамагнитной восприимчивости и др. В этих случаях при расчете разл. характеристик вводят поправочные члены экзальтации и т.п.
Наличием сопряжение связейобъясняют характерное изменение геометриимолекулы- укорочение формально простых и удлинение формально кратных связей. Напр.,в полиенах длины простых связей С—С (0,151 нм) несколько укорочены по сравнению с длиной связи С—С в этане (0,154 нм). Количеств. мера изменения длин связей при сопряжении порядки связей между атомами: в 1,3-бутадиене порядки связей альтернируют (соотв., 1,894; 1,447; 1,894), а в аллильном катионе порядки связей между соседними атомами С равны.
Сопряженные системы с делокализованными связями представляют собой соед. с характсристич. электронными переходами, причем с удлинением цепи сопряжения повышается интенсивность и смещается поглощение в электронных спектрах в сторону больших длин волн (соотв. гипер-хромный эффект и батохромный сдвиг; см. Цветность органических соединений).
Понятие о сопряжение связейиспользуют при рассмотрении реакц. способности. Напр., электроф. присоединение к сопряженным диенам (см.Диеновые углеводороды)приводит к смеси продуктов 1,2- и 1,4-присоединения.
В простейшем случае сопряженные системы —
это системы с чередующимися двойными и одинарными связями. Они могут быть открытыми и закрытыми. Открытая система имеется в диеновых углеводородах (УВ).
Все атомы С находятся в состоянии sp-гибридиза-ции. Четыре негибридные р-орбитами, перекрываясь между собой, образуют единую электронную систему. Этот вид сопряжения называется p, p-сопряжением.
Происходит сопряжение р-электронов с S-электро-нами. Этот вид сопряжения называется р, р-сопряже-нием. Закрытая система имеется в ароматических УВ.
Сопряжение – процесс энергетически выгодный, энергия (Е) при этом выделяется. Энергия сопряжения бутадиена – 1,3 составляет 15 кДж/моль, энергия сопряжения бензола – 228 кДж/моль.
2. Ароматичность
Это понятие, включающее различные свойства ароматических соединений. Условия ароматичности:
1) плоский замкнутый цикл;
2) все атомы С находятся в sp2-гибридизации;
3) образуется единая сопряженная система всех атомов цикла;
4) выполняется правило Хюккеля: в сопряжении участвуют 4n + 2 р-электронов, где n = 1, 2, 3...
Простейший представитель ароматических углеводородов – бензол. Он соответствует всем четырем условиям ароматичности. Правило Хюккеля: 4n + 2 = 6, n = 1.
Нафталин – ароматическое соединение 4n + 2 = 10, n = 2.
Пиридин – ароматическое гетероциклическое соединение. Взаимное влияние атомов в молекуле
2.Коллигативные свойства – это свойства растворов, зависящие от числа частиц растворенного вещества. К коллигативным свойствам растворов относят:
1) понижение давления насыщенного пара растворителя над раствором,
2) понижение температуры замерзания и повышение температуры кипения растворов по сравнению с температурами замерзания и кипения чистых растворителей.
3) осмотическое давление.
1 закон Рауля. Давление насыщенного пара растворителя над раствором пропорционально мольной доле растворителя.
2 закон Рауля. Понижение температуры замерзания и повышение температуры кипения растворов по сравнению с таковыми для чистого растворителя пропорциональны моляльной концентрации растворенного вещества:
Закон Вант-Гоффа. Осмотическое давление раствора равно газовому давлению, которое производило бы растворенное вещество, находясь в газообразном состоянии и занимая объем, равный объему раствора.
