
Ревматоїдний артрит
Ревматоїдний артрит – захворювання інфекційно-алергічного походження з системним ураженням сполучної тканини, переважно суглобів, з характерним для аутоімунних захворювань хронічним, зазвичай, прогресуючим перебігом.
Епідеміологія. Жінки хворіють частіше, ніж чоловіки (3:1). Захворювання може розвинутись в будь-якому віці, проте пік захворюваності припадає на п’яте десятиріччя. Поширеність ревматоїдного артриту складає 5,2% для жінок і 2,5% для чоловіків. У віці понад 75 років цей показник збільшується до 16% серед жінок і 6% серед чоловіків.
Етіологія. До цих пір етіологія ревматоїдного артриту залишається остаточно не визначеною. Відсутні докази етіологічного значення травм, клімату, характеру харчування, стресових впливів, метаболічних або ендокринних впливів. Донині дискутується питання щодо можливості інфекційної етіології ревматоїдного артриту, зокрема вірусної. Особливо активно вивчають вірус Ебштейна-Барра, який персистує в В-лімфоцитах і впливає на синтез імуноглобулінів (антитіл).
В останні роки вивчають також роль генетичних факторів у розвитку ревматоїдного артриту. Доведені, зокрема, генетично обумовлені варіанти імунної відповіді. У таких хворих спостерігається підвищення частоти HLA DR4ֿ і DW4-антигенів і зниження частоти HLA DR2-антигена. Підвищення частоти HLA DR4/ DW4 може бути ознакою вродженого порушення імунорегуляції і вродженої неповноцінності імунних механізмів.
Патогенез. Ревматоїдний артрит розглядають сьогодні як аутоімунну, імунокомплексну патологію з ураженням сполучної тканини суглобів.
Основними ланками патогенезу ревматоїдного артриту є наступні:
-
дисфункція імунної системи (зниження супресорної активності Т-лімфоцитів, гіперреактивність В-лімфоцитів);
-
неконтрольований, надмірний синтез В-лімфоцитами антитіл класів IgG та IgM;
-
вироблення В-лімфоцитами антитіл класу IgG та IgM проти модифікованого IgG (такого, що набув ауто антигенних властивостей) з формуванням з участю комплемента імунних комплексів типу IgG проти модифікованого IgG (циркулюють у крові) та IgM проти модифікованого IgG (в синовіальній рідині);
-
вивільнення під впливом індукуючого агента (ретровіруса?, парвовіруса В19?) з фібробластів і Т-лімфоцитів цитокінінів (інтерлейкіни IL-1, IL-2, IL-6, IL-4, IL-10, IL-15, TNFα-фактор некроза пухлин);
-
фагоцитоз імунних комплексів нейтрофілами (феномен рагоцитозу) з вивільненням медіаторів запалення – простагландинів, гістаміна, протеолітичних лізосомальних ферментів, кінінів, серотоніна, цитокінів.
Власне запалення синовіальної оболонки (синовііт) і деструкція хряща є результатом агресії з боку цитокінів та інших медіаторів запалення.
Сьогодні вважають, що в розвитку ревматоїдного синовііта приймають участь три механізми – неімунний, апоптозний та імуно-генетичний.
Патогенез ревматоїдного синовііта представляється наступним. Під впливом невідомого індукуючого агента (наприклад, ретровіруса або парвовіруса В19) відбувається трансформація протоонкогенів (sis, myb, myc, ras) синовіальних фібробластів з їх проліферацією і адгезією (панноцити?) на суглобовому хрящі, з подальшою активацією протеінкіназ, виділенням фібробластами цитокінінів IL-1/IL-1Ra, IL-6, TNF-α/TNF-α SR, розвитком запалення і деструкції хряща і кістки.
Схема патогенезу ревматоїдного синовіїта
(адаптовано за В.М.Гнилорибовим (2000). Ревматологічний журнал, 1: 23-28)
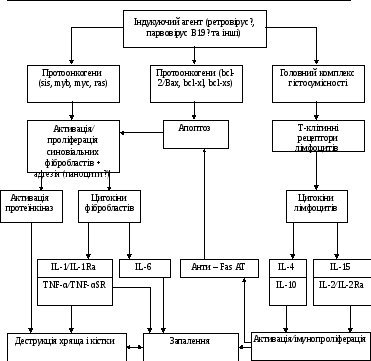
Примітка: IL – інтерлейкіни; TNFα-фактор некроза пухлин, альфа;
TNF-αSR – розчинні рецептори фактора некроза пухлин;
Анти Fas AT – антитіла до рецепторів Fas.
Цей головний клітинний сигнальний каскад, названий онкогенним мереживом (oncogene network), є свідченням Т-незалежного, тобто неімунного шляху розвитку ревматоїдного артрита.
Другий механізм – апоптозний. Апоптоз – це запрограмована клітинна смерть. Згідно концепції “засвідченого” апоптозу (bystander apoptosis) в синовіальній оболонці нагромаджується надмірна кількість апоптозних клітин.
Протоонкогени bcl-2 (інгібітор кінцевих механізмів апоптоза), bcl-xl (смертельне інгібування), bcl-xs (промоутери апоптоза) визначають подальшу долю фібробластів.
Третій механізм – імуногенетичний. Активація Т-клітин, взаємодія Т-клітинних рецепторів і подальша імунопроліферація призводять до виділення лімфоцитами цитокінінів IL-4, IL-15, IL-10, IL-2/IL-2Ra і виникнення імунного запалення, яке посилює деструкцію хряща і кістки. На жаль, не з’ясовані причини активації клітин імунної системи та їх інтенсивної міграції в синовіальну тканину.
В синовіальній оболонці і синовіальній рідині багато фібробласних і макрофагальних цитокінінів IL-1, IL-6, TNF-α і мало лімфоцитарних цитокінінів IL-2 та IL-4.
IL-1 – одна з ключових прозапальних молекул синовіальної оболонки при ревматоїдному артриті. Основна їх функція – стимуляція фібробластоподібних синовіоцитів до продукції ензимів (колагенази, стромелізина), які руйнують хрящ. Крім того, IL-1 гальмує продукцію компонентів синовіального і хрящового матриксів, а також колагена IV типу. Природнім інгібітором IL-1 в синовіальній оболонці є антагоніст рецепторів до IL-1 (IL-1Ra), однак достатньої кількості IL-1Ra медикаментозно досягти важко (це можливо шляхом переноса генів).
Цитокін TNF-α (подібний до IL-1) продукується фібробластами, макрофагами, лімфоцитами, ендотеліоцитами. Він, як і IL-1, є прозапальним цитокіном. Збільшення його кількості у синовіальній рідині є маркером активації ревматоїдного запалення.
Прозапальний IL-6 також є маркером активності ревматоїдного артриту, особливо при низькій клінічній активності процесу.
Збільшення в синовіальній рідині IL-10 (продукують Т-лімфоцити, макрофаги, моноцити) обумовлено збільшенням в ній кількості ревматоїдних факторів.
IL-15 (продукують лімфоцити і ендотеліоцити) відіграють важливу роль в міграції Т-лімфоцитів у вогнище запалення.
Таким чином, патогенез ревматоїдного артриту є результатом взаємодії неімунних, апоптозних та імунних механізмів, наслідком чого є інфільтрація синовіальної оболонки імунокомпетентними клітинами з подальшою імунопроліферацією, запаленням і деструкцією хряща і кістки. Провідне значення в імунопатогенезі належить відповіді СD4-лімфоцитів на індукуючий агент. Цитотоксичні лімфоцити і природні кіллери специфічно виділяють гранзим А і перфорин. Гранзим А викликає деградацію альфа-2-ланцюгів колагена IV типу і володіє противірусною активністю, а перфорин є одним з тригерів апоптоза. Біля 75% гранзим А-позитивних лімфоцитів є природніми кіллерами (СD16 або СD56). Гранзим А може активувати виділення IL-1-β (індуктора апоптоза). Біля 40% мононукларів, що інфільтрують синовіальну оболонку – це плазматичні клітини.
Безпосередньою причиною основних проявів ревматоїдного артриту – деградації хряща і кістки – є інфільтрація тканини хряща трансформованими пухлиноподібними синовіальними фібробластами.
Патоморфологія. Патоморфологічні зміни з боку суглобів мають стадійний характер.
У першій стадії (ексудативній) виникає набряк, повнокрів’я синовіальної оболонки, мукоїдне набухання, випотівання фібрину, гіперплазія ворсинок, формування синовііту.
Друга стадія (ексудативно-проліферативна) проявляється розвитком грануляційної тканини, яка наповзає на хрящ у вигляді рогівковиці (пануса). Відбувається руйнування хряща, утворення узур, секвестрів, які занурюються у субхондральну кістку.
Третя стадія (проліферативна) характеризується ушкодженням суглобових поверхонь, що вкриваються фіброзною тканиною, звуженням суглобової щілини, утворенням фіброзно-кісткового анкілозу.
