
БХ - 4 семестр / Разное / Б
.pdf
Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
|
|
|
|
|
|
|
16.11.2012 |
|
82 |
Пути утилизации аминокислот: |
||
|
1. |
Биосинтез белка |
|
2. |
Синтез олигопептидов (либеринов, |
|
|
статинов ) |
|
3. |
Биогенных аминов |
|
4. |
Мочевины |
АК |
5. |
Креатина, креатинфосфата |
6. |
Азотистые основания |
|
|
7. |
Аминоспирты |
|
8. |
Никотинамид |
|
9. |
Желчные кислоты |
|
10. |
Реакции обезвреживания и энергообмена |
16.11.2012 |
|
83 |
41

Кафедра биохимии ГомГМУ, 2012 |
|
|
|
|
|
16.11.2012 |
Кроме индивидуальных путей обмена, известен |
||||||
ряд превращений, общий почти для всех |
|
|
||||
аминокислот. Это реакции: |
|
|
|
|||
1.по радикалу (R)- реакции гидроксилирования |
||||||
(Про----> o-Про) |
|
|
|
|
||
разрыва радикала (образование Vit PP из ТРП); |
||||||
2.Реакции на --СООН группу – |
|
|
|
|||
декарбоксилирование (образование биогенных |
||||||
аминов, ГИС гистамин) |
|
|
|
|||
3. Реакции на группу NH2 – дезаминирование |
|
|||||
4х типов: |
|
|
|
|
|
|
16.11.2012 |
|
|
|
|
|
84 |
Виды прямого дезаминирования |
|
|
|
|||
Восстановительное дезаминирование |
|
|||||
R-CH-COOH + |
|
2H |
R-CH2-COOH |
+ |
NH3 |
|
NH2 |
|
|
|
|
|
|
Гидролитическое дезаминирование |
|
|
||||
R-CH-COOH |
+ |
H2O |
R-CH-COOH |
+ |
NH3 |
|
|
||||||
NH2 |
|
|
OH |
|
|
|
Внутримолекулярное дезаминирование |
|
|||||
R-CH-COOH |
|
|
R-CH=CH-COOH |
+ |
NH3 |
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
16.11.2012 |
|
|
|
|
|
85 |
|
|
|
|
|
|
42 |

Кафедра биохимии ГомГМУ, 2012 |
|
16.11.2012 |
Окислительное дезаминирование |
||
R-CH-COOH |
|
R-CH-COOH |
NH 2 |
|
NH |
Флавин |
Флавин-Н2 |
H2O |
|
||
|
|
NH3 |
H2O2 |
O2 |
R |
Каталаза |
|
C=O |
|
|
|
|
|
COOH |
H2O + 1/2O2 |
|
|
16.11.2012 |
|
86 |
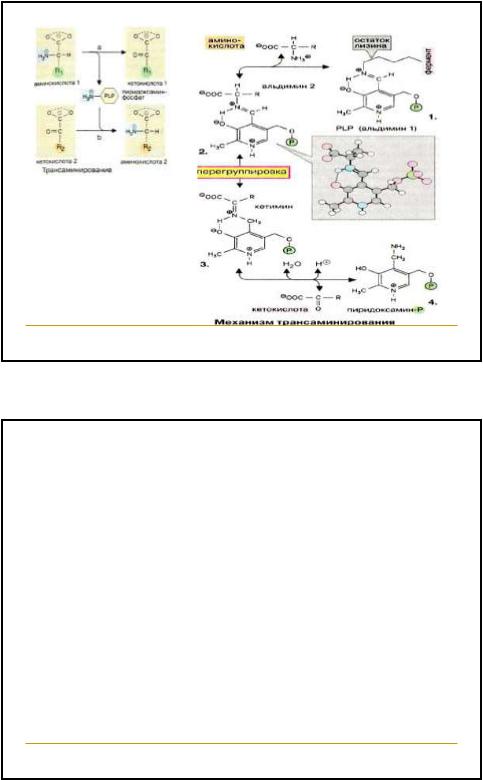
Трансаминирование аминокислот
окислительное дезаминированиепрямое
16.11.2012 |
87 |
43

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
Первая стадия является ферментативной с образованием промежуточного продуктаиминокислоты, которая спонтанно, без участия фермента, распадается на аммиак и α- кетокислоту.
Этот тип реакций наиболее распространен в тканях
16.11.2012 |
88 |
|
|
|
|
ГЛУ+NAD+---иминоглут кислота + НОН-
---α- кетоглутарат + NADH+H+ + NH3
Первая стадия катализируется ГДГ (анаэробный фермент). Вторая стадия проходит спонтанно. Реакция обратима!
16.11.2012 |
89 |
44

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
ГДГ – состоит из 6 субъединиц и
проявляет свою активность только в мультимерной форме.
При диссоциации ГДГ на субъединицы, в присутствии NADH2, ГТФ, стероидных гормонов, она теряет свою глутаматдегидрогеназную функцию, но
приобретает способность дезаминировать другие аминокислоты (аланин). ГДГ – регуляторный, аллостерический фермент.
16.11.2012 |
90 |
Все остальные аминокислоты могут окисляться и дезаминироваться только непрямым путем (т.е. через дополнительную стадию трансаминирования).
Коферментом трансаминаз является фосфорилированная форма Vit В6- пиридоксальфосфат, который в процессе реакции обратимо превращается в пиридоксаминфосфат.
16.11.2012 |
91 |
45

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
|
|
|
|
|
|
|
16.11.2012 |
92 |
Это главный путь удаления азота у аминокислот.
Выделены трансаминазы, катализирующие переаминирование большинства аминокислот.
После поступления пищевых аминокислот из воротной вены, например, значительная часть их в печени подвергается переаминированию.
16.11.2012 |
93 |
46

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
|
|
|
|
|
|
|
Исключением являются аминокислоты с разветвленным углеводородным радикалом, для которых в печени нет соответствующих трансаминаз, о чем говорит более высокая концентрация таких аминокислот в крови, оттекающей от печени по сравнению с концентрацией в крови воротной вены.
16.11.2012 |
94 |
Непрямое окислительное дезаминирование.
Почти все природные а/к сначала реагируют с α-КГК в реакции трансаминирования с образованием ГЛУ и соответствующей кетокислоты, а образовавшаяся ГЛУ затем подвергается прямому окислительному дезаминированию под действием ГДГ.
Т.е. все а/к подвергаются дезаминированию непрямым путем, только через стадию образования ГЛУ
16.11.2012 |
95 |
47

Кафедра биохимии ГомГМУ, 2012 |
|
16.11.2012 |
Любая а/к |
α- КГК |
NADH2 +NН3 |
Любая кето |
ГЛУ |
NADH+ + HOH |
кислота |
|
|
|
ГДГ |
|
трансаминазы |
|
|
16.11.2012 |
|
96 |
Поскольку обе эти реакции – и трансаминирование, и прямое дезаминированиеобратимы, то создаются условия для синтеза новой заменимой а/к, если в организме есть соответствующие кетокислоты. Организм человека не наделен способностью синтезировать углеводные скелеты (т.е. α- кетокислоты) незаменимых а/к. Этой
способностью обладают растения.
16.11.2012 |
97 |
48

Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
|
|
|
|
|
|
|
Т.о. можно сказать, что путь синтеза заменимых а/к в организме – это непрямое окислительное дезаминирование, которое запущено в обратном направлении.
Этот путь называется трансаминированием.
16.11.2012 |
98 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
16.11.2012 |
99 |
49
Кафедра биохимии ГомГМУ, 2012 |
16.11.2012 |
|
|
|
|
|
|
|
16.11.2012 |
100 |
|
|
|
|
Существует еще один механизм непрямого дезаминирования α- аминокислот, при котором ГЛУ, АСП, и АМФ выполняют роль системы переноса NН2- группы:
16.11.2012 |
101 |
50
