
- •Міністерство освіти науки
- •Лабораторна робота №1 здобування кислот, гідроксидів та солей
- •1.1 Загальні відомості
- •1.1.1 Здобування та властивості оксидів
- •1.1.2 Здобування та властивості гідроксидів
- •1.1.3 Здобування та властивості кислот
- •1.1.4 Здобування та властивості солей
- •1.2 Завдання для самостійного розв’язання:
- •1.3 Обладнання та реактиви
- •1.4 Вказівки до техніки безпеки
- •1.5 Порядок проведення лабораторної роботи
- •Лабораторна робота
- •Визначення еквівалента металу
- •2.1 Загальні відомості
- •2.1.1 Взаємозв'язок між основними фізичними величинами, що використовуються в хімії
- •2.2 Завдання для самостійного розв’язання
- •2.2.1 Розв’язати задачі
- •2.2.2 Визначити дані (?) для запропонованого варіанту
- •2.3 Обладнання та реактиви
- •2.4 Вказівки до техніки безпеки
- •2.5 Порядок проведення лабораторної роботи
- •Лабораторна робота № 3 окисно-відновні реакції
- •3.1 Загальні відомості
- •3.1.2 Метод електронного балансу
- •3.2 Завдання для самостійного розв’язання
- •3.2.1 Відповісти на запитання та виконати завдання
- •3.3 Реактиви та обладнання
- •3.4 Вказівки до техніки безпеки
- •3.5 Порядок проведення лабораторної роботи
- •Лабораторна робота №4 закономірності перебігу хімічних процесів
- •4.1. Загальні відомості
- •4.1.1. Енергетика хімічних процесів.
- •4.1.2. Основи хімічної кінетики
- •4.1.3. Хімічна рівновага
- •4.2. Завдання для самостійного розв’язання
- •4.2.1. Відповісти на запитання
- •4.2.2. Розв’язати задачі
- •4.3. Реактиви та обладнання
- •4.4. Вказівки до техніки безпеки
- •4.5 Порядок проведення лабораторної роботи
- •Лабораторна робота № 5 розчини
- •5.1 Загальні відомості
- •5.1.1. Загальна характеристика розчинів
- •5.1.2. Розчини електролітів
- •5.2 Завдання для самостійного розв'язання
- •5.2.1. Відповісти на запитання, виконати завдання
- •5.3 Реактиви та обладнання
- •5.4 Вказівки до техніки безпеки
- •5.5 Порядок проведення лабораторної роботи
- •Лабораторна робота №6 гальванічні елементи та електроліз
- •6.1 Загальні відомості
- •6.1.1 Електродні потенціали. Гальванічні елементи.
- •6.1.2 Електроліз
- •6.2 Завдання для самостійного розв’язання
- •6.3 Прилади та реактиви
- •6.4 Вказівки з техніки безпеки
- •6.5 Порядок проведення лабораторної роботи
- •Лабораторна робота №7 корозія та захист металів
- •7.1. Загальні відомості
- •7.2. Завдання для самостійного розв’язання
- •7.3. Реактиви та обладнання
- •7.4. Вказівки до техніки безпеки
- •7.5. Порядок виконання роботи
- •Загальна характеристика металів та їх сполук
- •8.1. Загальні відомості
- •8.2. Завдання для самостійного розв’язання
- •8.3. Реактиви та обладнання
- •8.4. Вказівки щодо техніки безпеки
- •8.5. Порядок виконання лабораторної роботи
- •Легкі конструкційні матеріали та їх властивості
- •9.1 Загальні відомості
- •9.2 Завдання для самостійного розв’язання
- •9.3 Вказівки до техніки безпеки
- •9.4 Реактиви та обладнання
- •9.5 Порядок проведення лабораторної роботи
- •Література
- •Додаток б Стандартні термодинамічні величини речовин
- •Додаток в Стандартні електродні потенціали е0 в при 250с
- •Додаток г Розчинність кислот, основ та солей у воді
Лабораторна робота № 5 розчини
Мета роботи:вивчити загальні властивості розчинів, дати порівняльну характеристику розчинам електролітів та неелектролітів, навчитися здобувати розчини заданої концентрації.
5.1 Загальні відомості
5.1.1. Загальна характеристика розчинів
Розчини - гомогенні системи, які складаються з двох або більше компонентів : дисперсійної фази – речовини , які рівномірно розподілені у вигляді молекул , атомів, йонів у дисперсійному середовищі – розчиннику . Розчинення речовин супроводиться зміною теплового ефекту. Цей факт та інші свідчать про хімічну взаємодію розчиненої речовини та розчинника.
При розчиненні речовини протікають процеси: руйнування хімічних зв'язків між частинками (атомами, молекулами, йонами) речовини, розчинника, що пов'язане з поглинанням теплоти; в цей час відбувається екзотермічний процес утворення сольватів (гідратів); дифузія сольватів (гідратів) між частинками розчинника (ендотермічний процес). Тепловий ефект розчинення - це сумарне значення вище вказаних процесів.
Розчинність речовини залежить від: природи речовини, температури, тиску (для газоподібних речовин) та інші. (Додаток Г).
Кількісно розчини характеризуються:
Кр- коефіцієнт розчинності, показує масу речовини, що припадає на 100 г розчинника (об'єм газоподібної речовини на 1 л розчинника)
ω- масова (об'ємна) частка розчиненої речовини
ω = (mреч./mр-ну.)·100%;
ω = (Vреч./V р-ну.) ·100%.
См- молярна концентрація, показує кількість розчиненої речовини, яка міститься в 1 л розчину
СМ = υ/ Vр-ну
СМ = m/(M· Vр-ну), моль/л
СN- еквівалентна концентрація (нормальна) показує число еквівалентів (Nекв.) розчиненої речовини в 1 л розчину.
СN = Nекв/Vрозч.; СN=m/(Mекв · Vрозч.)
Титр - відношення маси речовини до об'єму розчинника
T = mреч./Vрозч.(мл)
5.1.2. Розчини електролітів
1. При розчиненні у воді електроліти дисоціюють з утворенням йонів, тому розчини електролітів проводять електричний струм.
HCl ↔ H+ + Cl-; Al2(SO4)3 ↔ 2Al3+ +3SO42-;
NaOH ↔ Na+ + OH-; KHCO3 ↔ K+ + HCO3
2. На процес дисоціації впливає: природа речовин, природа розчинника, температура.
3. Кількісною характеристикою процесу дисоціації є:
1) ступінь дисоціації (α)
α=СM. дис. м-л /СМ заг.;
Ступінь електролітичної дисоціації визначають експериментально за величиною ізотонічного коєфіціента і -поправлення від ідеальних систем, розбавлених розчинів неелектролітів
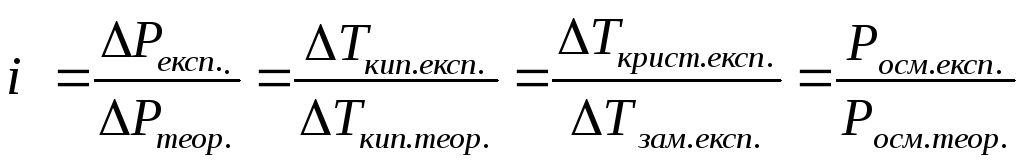
![]() ,k - число
йонів, на яке дисоціює молекула
електроліту.
,k - число
йонів, на яке дисоціює молекула
електроліту.
2) для слабких електролітів - константа дисоціації КД.
Для рівняння: aA + bB = cC + dD
KД = (Ссс·СDd)/(CAa·CBb); KД = Сα2/1-α(закон розбавлення Оствальда).
4. Дисоціація води. Йонний добуток води.
Чиста вода - слабкий електроліт.
Н2О ↔ H+ + OH- α=1,8·10-9 (22°C)
2H2O ↔ H3O+ + OH-; H3O+ - йон гідроксонію
КН2О = [H+] · [OH-]- йонний добуток води.
В 1 л води (t° = 22°С) [H+] = [OH-]=10-7 йонів
КН2О=10-7·10-7=10-14- стала величина
Кислотні властивості розчинів (С.Серенсен,1909р) характеризуються величиною водневого показника рН = -lg [H+].
рН = від 1 до 14
рН = 7 - нейтральний розчин
рН < 7- кислий
рН > 7- лужний
5. Деякі солі при розчинені у воді підлягають гідролізу - розкладаються водою з утворенням слабких електролітів.
Zn2+ + HOH → ZnOH+ + H+; pH < 7
CO32- + HOH → HCO3-+ OH-; pH > 7
Збільшення температури сприяє прискоренню гідролізу.
Розчини неелектролітів
Розчини неелектролітів не проводять електричний струм, характеризуються колегативними властивостями, тобто властивості розчинів залежать лише від їхньої концентрації і не залежать від природи розчиненої речовини.
Кількісно характеризуються:
1) осмотичним тиском (Вант-Гофф, 1885р)
Pосм.= υRT/Vр-ну
2) законами Рауля:
ΔP = P0·(υреч./ (υреч. + υр-ка)
ΔP - відносне зниження тиску пари над розчином
υ- кількість речовини
ΔТкип = Ke·Cm; ΔТкрист = Kкр · Cm
ΔТкип- підвищення температури кипіння розчину в порівнянні з температурою кипіння розчинника;
ΔТкрист.– зниження температури замерзання розчину в порівнянні з температурою замерзання розчинника;
Cm - моляльна концентрація розчину (показує кількість речовини (число молів) в 1000г розчинника)
Ке - константа ебуліоскопічна
Ккр. - константа кріоскопічна
Ке, Ккр- залежать від природи розчинника
