
- •Лабораторний практикум
- •Фізична хімія
- •Передмова
- •Оформлення результатів вимірювань
- •Складання таблиць
- •Молярна електрична провідність водних розчинів
- •Побудова графіків
- •Розділ і термохімія
- •Лабораторна робота №1 визначення теплової сталої калориметра
- •Запис вимірювання температури під час досліду
- •Лабораторна робота №2 визначення теплоти гідратоутворення купрум (II) сульфату
- •Визначення теплоти нейтралізації сильної кислоти сильною основою у воді
- •Контрольні питання
- •Будова атома і молекули, електричні та оптичні властивості Рефрактометрія
- •Визначення рефракції речовини і встановлення його структури
- •Контрольні питання
- •Хімічна рівновага
- •Визначення залежності константи рівноваги від температури в гомогенній системі
- •Послідовність виконання роботи
- •Розрахунок рівноважних концентрацій речовин
- •Експерементальні данні
- •Контрольні питання
- •Розділ іv фазові рівноваги
- •Побудова та аналіз діаграм плавкості і3 простою евтектикою
- •Типи термопар
- •Визначення кристалізації речовини 3 розчину при низьких температурах
- •Послідовність виконання роботи
- •Лабораторна робота №7 кристалізація бінарних сумішей (система NaNо3 – kno3)
- •Контрольні питання
- •Розділ V розчини
- •Лабораторна робота №8 розподіл речовини між двома рідкими фазами
- •Послідовність виконання роботи
- •Визначення ступеня асоціації оцтової кислоти в бензолі (чи хлороформі)
- •Вивчення процесу екстрагування
- •Контрольні питання
- •Кріоскопія, ебуліоскопія
- •Установка термометра Бекмана для кріоскопії.
- •Лабораторна робота №11 визначення молекулярної маси речовини кріоскопічним методом
- •Послідовність виконання роботи.
- •Визначення молекулярної маси речовини ебуліоскопічним методом (метод визначення молекулярної маси по Сиволобову)
- •Послідовність виконання роботи.
- •Завдання до лабораторної роботи
- •Контрольні питання
- •Електрохімія
- •Водневий показник як кількісна характеристика кислотності-основності розчинів
- •Потенціометрія
- •Визначення рН буферних розчинів
- •Послідовність виконання роботи
- •Контрольні питання
- •Хімічна кінетика
- •Вивчення швидкості йодування ацетону
- •Послідовність виконання роботи
- •Контрольні питання
- •Вивчення швидкості інверсії цукру
- •Теоретичні відомості
- •Послідовність виконання роботи
- •Підготовка до роботи поляриметра
- •Контрольні питання
- •Вивчення кінетики розчинення твердої кислоти у воді
- •Дифузія
- •Послідовність виконання роботи
- •Котрольні питання
- •Додатки
- •Значення деяких фундаментальних сталих
- •Знаки деяких математичних дій
- •Множники і префікси для утворення десяткових кратних і дольних одиниць
- •Густина води при різних температурах
- •Питома електрична провідність 0,01м розчину kСl при різних температурах
- •Інтегральна теплота розчинення солей, які утворюють кристалогідрати, при температурі 18°с.
- •Йонні електричні провідності при нескінченному розведені λ∞
- •Йонні електричні провідності при нескінченному розведені при температурі 25°c
- •Література
- •Періодична система елементів д. І. Менделєєва
Послідовність виконання роботи
Широку пробірку заповнюють кислотою бензойною на висоту 5-6 см, обережно нагрівають у полумۥї газового пальника до повного розплавлення кислоти і опускають у розплав майже на дно пробірки скляну паличку. Після затвердіння кислоти пробірку обережно розбивають і разом із паличкою виймають циліндр твердої бензойної кислоти.
На столик магнітної мішалки ставлять склянку місткістю 150см3, вливають в нього за допомогою мірного циліндра 100см3 дистильованої води, кладуть якір магнітної мішалки і встановлюють таку швидкість обертання, щоб вода в склянці добре перемішувалась.
Скляну паличку разом із наплавленим циліндром кислоти укріплюють у штативі над поверхнею води в центрі склянки. Занурюють циліндр кислоти у воду і фіксують час початку досліду. Через 10 хв обертання першу склянку замінити другою склянкою з водою, де обертається циліндрик протягом 15 хв, потім підставляється третю склянку на 20 хв і, нарешті, четвертий - на 30 хв. З кожної склянки беруть проби по 10 мл і титрують розчином NaОН приблизно 0,01 н. з фенолфталеїном (індикатор). Виконують 3 паралельних визначення.
Концентрацію насиченого при температурі досліду розчину бензойної кислоти визначають числом мл даного розчину NaОН, що йде на титрування 100мл насиченого при даній температурі розчину бензойної кислоти.
Для приготування насиченого розчину бензойної кислоти наважку близько 1г розчиняють при нагріванні до 50-60°С у 50 мл дистильованої води, охолоджують до температури досліду, відбирають 10мл розчину, уміщують його у конічну колбу міскістю 100 мл, додають кілька краплин розчину фенолфталеїну і титрують 0,01н. розчином NaОН до появи рожевого забарвлення розчину. Виконують 2-3 паралельних визначення.
Таким чином, в рівняння
![]()
замість Снас і С підставляють відповідне число мл даного розчину NaОН, що вельми спрощує розрахунки:
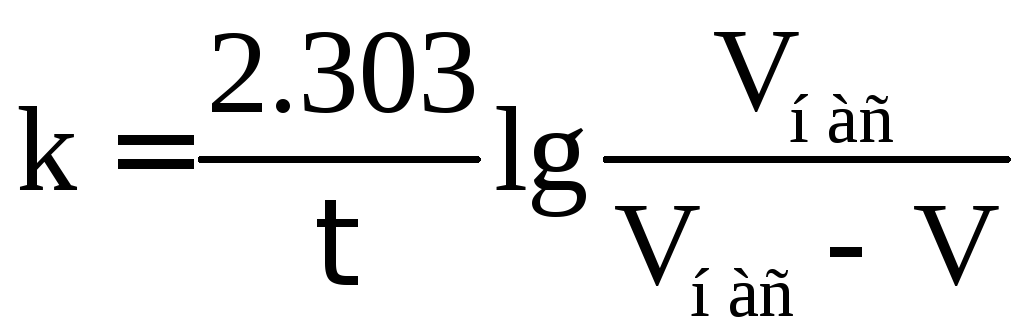 (7.25)
(7.25)
Оскільки завдання полягає тільки в перевірці сталості значень k, можна користуватися не натуральним, а десятковим логарифмом. Константа швидкості k залежить від площі поверхні циліндрика, від температури і частоти обертання. За результатами дослідів заповнюють таблицю 7.4
Таблиця 7.4
|
Час досліду t, хв |
VNaОН на 10мл розчину, мл |
Середнє значення VNaОН на 10мл розчину, мл |
Конц. бензойной кислоти, Ск-ти моль/л
|
Снас. , моль/л, при кімн.темп. |
k, с-1 | ||
|
10 |
|
|
|
|
|
|
|
|
15 |
|
|
|
|
|
| |
|
20 |
|
|
|
|
|
| |
|
30 |
|
|
|
|
|
| |
Котрольні питання
1. Які процеси називаються гетерогенними? З яких стадій складаються гетерогенні хімічні реакції?
2. Що називається дифузією?
3. Перший і другий закони Фіка.
4. Константа швидкості процесу розчинення.
5. Що називається коефіцієнтом дифузії? Від яких факторів він залежить? Яка його розмірність?
6. Що таке стаціонарна дифузія?
7. Який вигляд має кінетична рівняння стаціонарної дифузії? Який порядок цього процесу?
8. Опишіть кінетику процесу розчинення твердої речовини в рідині. Як можна прискорити цей процес?
9. Як можна встановити природу лімітуючої стадії у випадку гетерогенного хімічного процесу?
