
Глава 1. Обзор литературы.
Нейродегенерация и актиновый цитоскелет.
Ключевые структуры мозга представлены с одной стороны нервными клетками во всем их разнообразии форм, длины, количества отростков, размеров, типов распределения и числа образуемых синапсов, а с другой – поддерживающими их глиальными и сосудистыми компонентами. Некоторые изменения нервных клеток происходят в ранний период жизни. Например, первые накопления нейромеланина в пигментированных клетках ствола мозга обнаруживают в раннем детском возрасте (Джекбери и Оппенгаймер, 2003). Но есть изменения нервных клеток, которые происходят и прогрессируют в старости.
Зная ключевые структуры мозга, ученым не удалось выявить все причины, влекущие за собой изменения этих структур. Одно из таких изменений – это изменения, вызванные механизмами нейродегенерации Некрасивая фраза. Эти механизмы лежат в основе нейродегенеративных заболеваний (НДЗ). Данным термином определяется обширная группа заболеваний, для которых характерна медленно прогрессирующая гибель определенных групп нервных клеток и постепенно нарастающая атрофия соответствующих отделов мозга. НДЗ, такие как ввести сокращения болезнь Альцгеймера (БА), БХ, БП, относят к болезням цитоскелета – кофилинопатиям (Bamburg and Bloom, 2009). Одно из другого не вытекает. Почему относят к кофилинопатиям.
При нейродегенерации происходят существенные изменения в компонентах нейронального цитоскелета. Внутренний цитоскелет состоит из актина и других легко полимеризующихся белков. Актин имеет связь с мембранными белками и выполняет формообразующую и опорную функцию (рис. 1).

Рис. 1. Схематическое изображение клеточной мембраны (по: Березов и Коровкин, 1998).
Цитоскелет создает внутреннюю структуру клеток, поддерживает их форму и выполняет важную транспортную функцию. Он участвует в переносе веществ, например, ферментов и других белков, которые синтезируются в теле клетки, к дендритам и аксональным окончаниям, а также в обратном транспорте синаптических веществ это кто? Те, кто переносится из других клеток? к телу клетки. Компоненты цитоскелета сами медленно двигаются от центра к периферии (Fu et al., 2015).
Актиновый цитоскелет обеспечивает функционирование Na+/K+-АТФазы, NHE1 (sodium-hydrogen exchanger 1), Na+/Ca2+-обменника, потенциал-независимых Na+ каналов, потенциал-зависимых Ca2+ каналов, NMDAR (рецептор глутамата, селективно связывающий N-метил-D-аспартат) и AMPAR (рецептор α-амино-3-гидрокси-5-метил-4-изоксазолпропионовой кислоты) (Mills et al., 1994; Sheean et al., 2013). Оксидативный стресс приводит к накоплению Са2+ в клетке (Ruiz et al., 2014), вызывая АТФ-истощение.
Появление включений в нейритах при добавлении глутамата свидетельствует о зависимости формирования агрегатов от NMDAR. H2O2 и окись азота (NO) вызывают оксидативный стресс в нейронах за счет снижения синтеза ATФ в митохондриях. Хронически низкий уровень АТФ отмечается у пациентов с БХ (Sorolla et al., 2012). Дефицит АТФ при БХ приводит к изменению плотности шипиков дендритов, атрофии аксонов, что вызывает нейродегенерацию (Munsie et al., 2011).
Ремоделирование актина является АТФ-зависимым процессом, и для его поддержания клетка потребляет 50% от общего объема энергии в нейроне (Bernstein and Bamburg, 2003). Снижение уровня АТФ вызывает дефосфорилирование, активацию пула АДФ/кофилина и увеличение содержания АДФ-актина. При образовании актин-кофилиновых палочек происходит снижение интенсивности ремоделирования актина и сокращение потребления АТФ. Нейриты с «молодыми» актин-кофилиновыми палочками, по сравнению с нейритами без них, теряют АТФ с меньшей скоростью, нежели нейриты со «старыми» палочками (Bernstein et al., 2006).
Три основных компонента цитоскелета состоят из разных белков: микрофиламенты – в основном, из актина, микротрубочки - из тубулина, а нейрофиламенты - из нескольких белков. Также для установления связи между этими компонентами, с клеточной мембраной и экстрацеллюлярным матриксом необходимы еще и другие белки (Sunter et al., 2015).
Белок тау участвует в образовании связей между нейрофиламентами и микротрубочками. А скопления тау-белка участвуют в образовании патологических спирально извитых парных филаментов, которые формируют нейрофибриллярные клубки (НФК). Сопровождаются эти изменения образованием сенильных бляшек (СБ) – патологических скоплений бета-амилоида неправильной сферической формы, иногда с ядром в центре. В клетках выявлены сенильные бляшки двух разновидностей: с ядром, которые называют «зрелыми» (рис. 2), и без ядра, которые называют «простыми», а иногда «диффузными» (рис. 3).
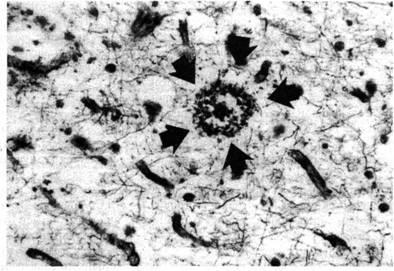
Рис. 2. Зрелая бляшка (отмечена стрелками) в коре мозга пожилого субъекта, не страдавшего деменцией (х 200). Хорошо определяется ядро бляшки в центре и конденсация окружающих отростков нейронов, формирующих венец. Окраска серебром по Von Braunmuhl (по: Джекоби и Оппенгаймер, 2001).

Рис. 3. Простая, аргирофильная бляшка (отмечена стрелками) в коре мозга пациента, страдавшего БА (х 200). Заметен реактивный астроцитоз у края бляшки (направляющие концы стрелок). Окраска серебром по Von Braunmiihl (по: Джекоби и Оппенгаймер, 2001).
Сенильные бляшки в нормальном мозге распространены шире, чем НФК. Они обнаруживаются в новой коре (находящейся снаружи от гиппокампа и обонятельной коры), в миндалине, а также гиппокампе и обонятельной коре. Нерастворимые включения не влияют на жизнеспособность клетки, но перегораживают путь в отростки нейрона, разрушают микротрубочки, что приводит к дегенерации отростков. Этот механизм лежит в основе потери синапсов и нарушении синаптической пластичности, характерной для нейродегенерации, которая не сопровождается изменением числа нейронов (Minamide et al., 2000).
Определенных и общепризнанных различий между нормальным старением и БА в том, что касается числа и распределения СБ – нет. Однако, для высших психических функций особенно важны скопления бляшек с аномальным тау-положительными нейритическими компонентами. Они присутствуют в мозге и при нормальном старении, но лишь в небольших количествах. Критерии дифференцирования нормального старения и БА основаны на выявлении более многочисленных и нейритических СБ в новой коре при БА (Mirra et al., 1991).
В исследованиях на дрозофиле и мыши показано, что нейродегенерация, инициированная тау, ассоциирована с накоплением F-актина и формированием актин-кофилиновых комплексов. Актин-кофилиновые комплексы образуются при гиперактивации кофилина. Накапливаясь в аксонах и дендритах нейронов, они блокируют везикулярный транспорт (Stokin and Goldstein, 2006). Эти комплексы встречаются либо в виде оформленных палочек, либо агреосом или цитоплазматических паракристаллических сетей (телец Хирано). Следует иметь в виду, что четкой классификации актин-кофилиновых включений пока не сформулировано.
Другая аномалия цитоскелета, которая также активно проявляется при НДЗ, - образование телец Хирано.
Тельца Хирано – эозинофильные палочковидные включения. Впервые они были описаны японским невропатологом Асао Хирано (Hirano et al., 1968). Длина телец от 20 до 30 мкм, диаметр составляет 6 мкм. На продольном срезе тельца Хирано имеют вид «палочки» (рис. 4).

Рис. 4. Тельце Хирано (стрелка) возле пирамидной нервной клетки в гиппокампе пациента, страдавшего БА (х 400). Окраска гематоксилином и эозином (по: Джекоби и Оппенгаймер, 2001).
Однако на поперечном срезе тельца Хирано выглядят округлыми. При большом увеличении видно, что часто они имеют полосчатую структуру. Также тельца Хирано, расположенные около или на месте погибших нейронов, нередко похожи на столбики эритроцитов в капиллярах (Завалишина, 2009). В состав телец Хирано входят актин, кофилин и АДФ (Maciver and Harrington, 1995). Они формируются при усилении сродства белка 34 кДа к актину и потери им чувствительности к регулирующему влиянию со стороны ионов Са2+ (Maselli et al., 2003).
Образование телец Хирано, сенильных бляшек, актин-кофилиновых палочек являются причинами нарушения функционирования цитоскелета. Несмотря на то, что причины агрегации данных образований различны, механизм действия схож, и влечет за собой процессы нейродегенерации.
