- •Зависимость скорости реакции от рН
- •Виды нуклеиновых кислот
- •Метаболизм белково-пептидных гормонов.
- •Пути экскреции гормонов и их метаболитов.
- •Биосинтез мелатонина.
- •Метаболизм аминокислотных гормонов.
- •Метаболизм тиреоидных гормонов.
- •Метаболизм мелатонина.
- •Пути экскреции гормонов и их метаболитов.
- •Регуляция обмена белков.
- •Этапы синтеза стероидных гормонов.
- •Транспорт гормонов.
- •Специфические транспортные белки плазмы крови.
- •Неспецифические белки.
- •Физиологическая роль связывания гормонов в крови.
- •Периферический метаболизм гормонов.
- •Виды метаболизма:
- •Билет 77. Регуляция обмена белков.
- •Этапы действия стг.
- •Этапы действия инсулина.
- •Половые гормоны.
- •Регуляция водно-солевого обмена.
- •Гормональная регуляция обмена кальция.
- •Функции кальция.
- •Биохимические принципы витаминотерапии
- •Белки плазмы крови.
- •Высаливание.
- •Функции белков плазмы крови.
- •Альбумины.
- •Строение гемоглобина.
- •Функция гемоглобина.
- •Производные гемоглобина.
- •Типы гемоглобинов.
- •Физиологические типы гемоглобина.
- •Аномальные типы гемоглобина
- •Патология обмена гемоглобина.
- •Порфирии.
- •Синтез гема.
- •-Глобулины.
Виды нуклеиновых кислот
|
Признаки |
ДНК |
РНК |
|
I. Химическое строение |
|
|
|
а) производные пурина |
А, Г |
А, Г |
|
б) производные пиридина |
Ц, Т |
Ц, У |
|
в) углеводы |
Дезоксирибоза-5-фосфат |
Рибоза-5-фосфат |
|
г) Фн |
Н3РО4 |
Н3РО4 |
|
д) минорные основания |
+ |
+ + + |
|
II. Локализация |
Ядро, митохондрии |
Ядро, цитоплазма |
|
III. Содержание |
Неизменно |
Изменяется |
|
IV. Метаболизм |
Инертен |
Активный |
|
V. Функция |
Хранитель информации |
Передача информации |
Виды РНК: информационная (матричная)
Рибосомальная
Транспортная
Функции: И-РНК – передача информации
Р-РНК – основа рибосом. Способствует передвижению и-РНК по рибосоме.
Т-РНК – перенос аминокислот.
Структура нуклеопротеидов.
Первичная структура – это последовательность нуклеотидов, соединенных сложноэфирной связью. При изучении структуры Чаргафом установлены закономерности:
а. Количество А=Т, Ц=Г
б. Количество пуриновых оснований = количеству пиримидиновых А+Г=Ц+Т
в.
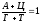
Вторичная структура – трехмерная, пространственная структура, состоящая из антипараллельных противозакрученных спиралей. Шаг спирали содержит 10 нуклеотидов. Внутри цепочки находятся азотистые основания, соединенные по принципу комплиментарности.
Образуют вторичную структуру водородные связи, вандер-вальсовы связи, гидрофобные. ДНК имеет двуцепочную вторичную структуру, РНК – одноцепочную.
Изучена в Работах Уотсона и Крика.
Третичная структура – определенная укладка спирализованной структуры. М-ДНК имеет форму восьмерки. РНК – изучена мало.
Четверичная структура – фонкционально активная, соединена с белком.
В состав нуклеопротеидов входят белки гистонового ряда, которые соединяются с НК слабой электростатической связью.
Функции гистонов:
Участвуют в пространственном построении НК;
Регулируют активность генома – репрессия гена, с которым соединен гистон и ген будет молчать.
Гистоновые белки содержат лиз, арг, мало цис.
Негистоновые белки образуют с ДНК легко разрушаемые связи и это обеспечивает регуляцию активности генома.
В процессе жизни ДНК может подвергаться под действием химических соединений (кофеин) или радиоактивного излучения изменениям, т.е. мутациям.
Виды мутаций:
Транзиция – замена пуринового основания на другое пуриновое.
Трансверсия – замена пуринового основания на пиримидиновое.
Делеция – вставка пары нуклеотидов.
Вставка пары нуклеотидов.
Тяжелые последствия наблюдаются при вставке или выпадении нуклеотидов.
В случае делеции одного мономера изменяется считывание всех последующих кодонов – это мутация со «сдвигом рамки». В результате синтезируется белок с «бессмысленной» последовательностью аминокислот. При делеции двух мономеров также происходит сдвиг рамки. При утрате трех мономеров (или число, кратное трем) сдвига рамки нет и синтезируется белок, укороченный на 1 аминокислоту.
Нуклеиновые кислоты.
Хромосомы – очерченный материал 46 пар.
Если клетка находится в покое, то хромосомы называют хроматином.
Хроматин – 60% белка, 35 ДНК, остальное РНК. Представлен в виде нитей с узелками и утолщениями (нуклеосома).
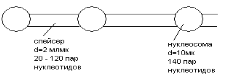
У человека в спейсере – 50 пар нуклеотидов. Нуклеосома – 90%, спейсер – 10%.
Спейсер – это активный хроматин, списывание информации (транскрипция) идет с этих участков.
Нуклеосома – это белковый + нуклеотидный компонент. Сюда входят гистоны, имеют основной характер (арг, лиз), нет цис, мало три, много гли. Молекулярная масса – 25 – 30 тысяч дальтон.
Взаимодействуют гистоны с НК за счет электрохимических взаимодействий (гистон (+), НК (-)).
5 классов гистонов:
Н1– лизин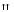
Н2b– лиз
Н2а – лиз = арг
Н3– арг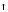 ,
есть лиз,цис!!
,
есть лиз,цис!!
Н4– арг ,
гли
,
гли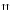
Молекулярная масса всех классов одинакова.
Н1– находится в спектре. При взаимодействии образуется октамер.
Функциональные участки ДНК – это гены.
Структурные гены – ответственны за последовательность АМК и за последовательность нуклеотидов.
Регуляторные участки – промотор
Интроны – неинформативные участки – нетранскрибируемые участки.
Билет 68.
Виды переноса генетической информации.
Перенос генетической информации в пределах одного класса нуклеиновых кислот, т.е. от ДНК к ДНК или у некоторых вирусов от РНК к РНК, называется репликацией или самоудвоением.
Перенос информации между разными классами нуклеиновых кислот: ДНК-РНК, называется транскрипцией или переписыванием.
Транскрипция бывает прямая от ДНК к РНК и обратная от РНК к ДНК. Обратная транскрипция выявлена у РНКовых опухолеродных вирусов.
Перенос генетической информации от м-РНК к белку, называется трансляцией или переводом.
Перенос генетической информации от ДНК через РНК к белку называется центральным постулатом генетики. Этот постулат был сформулирован Криком.
Репликация.
Возможны 3 типа репликации:
Консервативная – дочерняя двойная спираль ДНК образуется без разделения цепей родительской ДНК.
Полу консервативная – цепи родительской ДНК расходятся, и на каждой из родительских цепей образуются комплиментарные цепи дочерней ДНК.
Дисперсивная – происходит расщепление в нескольких местах цепей родительской ДНК и образование на ней новых цепей ДНК.
У высших организмов репликация ДНК происходит полуконсервативным путем.
Этапы биосинтеза ДНК.
Условно механизм синтеза делят на 3 этапа: инициацию, т.е. начало, элонгацию, т.е. продолжение, и терминацию, т.е. прекращение синтеза.
Первый этап – инициация – начало синтеза нуклеотидных цепей на матрице ДНК затравочного олигорибонуклеотида (праймера) со свободной гидроксильной группой у С-3’рибозы.
Второй этап – элонгация синтеза ДНК состоит из 2 стадий. На первой стадии идет репликация обеих материнских цепей ДНК, синтез одной идет непрерывно, а другой фрагментарно при помощи ДНК-полимеразы III. Вторая стадия включает связывание фрагментов друг с другом, здесь происходит отделение олигорибонуклеотидных праймеров. Процесс идет при помощи ДНК-лигаз.
Третий этап терминация синтеза ДНК наступает тогда, когда исчерпана ДНК-матрица.
Репарация
ДНК - исправление поврежденных
участков одной из цепей ДНК. Сначала
такой участок удаляется ДНКазами. Затем
при участии фрагмента ДНК-полимеразыIзаполняется фрагмента
ДНК-полимеразыIзаполняется
пробел путем синтеза участка в направлении
5’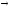 3’. Затем концы сшиваются ДНК-лигазой.
3’. Затем концы сшиваются ДНК-лигазой.
Основные этапы репликации ДНК (схема).
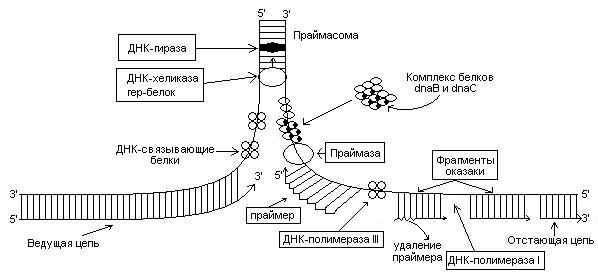
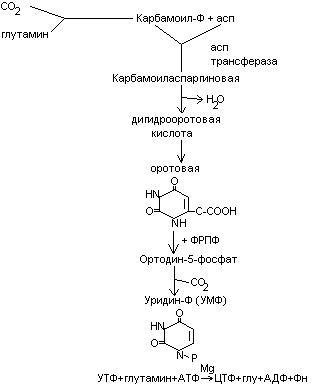
Билет 73
По химической структуре гормоны можно разделить не 3 группы:
Стероиды.
Производные аминокислот.
Белково-пептидные гормоны. Внутри каждой группы выделяют еще группы гормонов.
|
Гормоны
| ||||||||||||
|
Стероидные
|
Производные аминокислот
|
Белковопептидные гормоны
| ||||||||||
|
Кортикостероиды
|
Половые |
Трипто-фана мела-тонин (гормон эпифиза) |
Тирозина |
1.Нейрогипофи-зарные 2.Гипоталамичес-кие релизингфакторы 3.Пептиды поджелудочной железы (инсулин, глюкагон) 4.Гипофизарные (пептиды типа АКТГ) 5.Белки паращи-товидных желез (паратгормон, кальцитонин) | ||||||||
|
Глюко-корти-коиды |
Минера-локорти-коиды |
Ан-дро-гены |
Эс-тро-гены |
Катехол-амины |
Тиреоид-ные гормоны | |||||||
|
|
| |||||||||||
В составе белково-пептидных гормонов можно выделить 3 фрагмента, имеющих разное функциональное значение:
Адресный фрагмент – гаптомер – обеспечивает поиск мест специфического действия, но не вызывает биологических эффектов.
Актон – эффектомер - обеспечивает включение гормональных эффектов.
Вспомогательный (дополнительный) фрагмент стабилизирующий гормон, регулируя его активность, но не оказывает прямого влияния на реализацию гормонального эффекта.
Отличительная черта адресных фрагментов – способность в физиологических концентрациях конкурировать с цельной молекулой гормона за связывание с определенными рецепторами и неспособность в любых концентрациях воспроизводить гормональный эффект. Вместе с тем актоны практически не конкурируют в физиологических концентрациях с цельной молекулой гормона за связывание с реагирующей клеткой, но могут в сверхфизиологических концентрациях вызывать специфические гормональные эффекты.
Химической модификацией структуры гормональной молекулы можно получить производное гормона, которое будет связываться рецепторами, но не будет вызывать эффекта. Такие модифицированные соединения могут обратимо конкурировать с нативными гормонами за связи рецепторов, блокируя гормональный эффект. На этом принципе основано действие антигормонов конкурентного типа.
Синтез белково-пептидных гормонов.
Синтез полипептидного гормона складывается из 2 этапов:
Рибосомального синтеза неактивного предшественника на матрице мРНК.
Посттрансляционное образование активного гормона.
Посттрансляционная активация гормональных предшественников может происходить 2 путями:
Многоступенчатая ферментативная деградация молекул крупномолекулярных предшественников с уменьшением размера молекул.
Неферментативная ассоциация прогормональных субъединиц с укрупнением молекулы активируемого гормона.
Первая форма активации предшественников пептидных гормонов характерна для инсулина, паратгормона, ангиотензина.
Рассмотрим
этот процесс на примере инсулина. На
первом этапе на полисомах
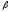 -клеток
синтезируется короткоживущий
одноцепочечный пептид, состоящий из
104 – 110 аминокислотных остатков. Этот
пептид назван препроинсулином и не
обладает биологической активностью:
-клеток
синтезируется короткоживущий
одноцепочечный пептид, состоящий из
104 – 110 аминокислотных остатков. Этот
пептид назван препроинсулином и не
обладает биологической активностью:
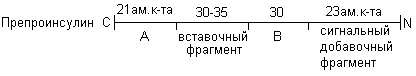
Сигнальный и вставочный фрагменты вариабельны у различных видов животных. В цистернах шероховатого ретикулума препроинсулин подвергается протеолизу с N-конца, в результате отщепляется сигнальный 23-членный пептид, «протаскивающий» прогормон через мембрану. Препроинсулин превращается в проинсулин, обладающий очень низкой биологической активностью. Затем происходит ферментативное выщепление вставочного фрагмента и проинсулин, А и В цепи соединяются дисульфидными связями.
Схема синтеза:
Ген
 мРНК
мРНК препрогормон прогормон
препрогормон прогормон
 гормон А
гормон А