- •Зависимость скорости реакции от рН
- •Виды нуклеиновых кислот
- •Метаболизм белково-пептидных гормонов.
- •Пути экскреции гормонов и их метаболитов.
- •Биосинтез мелатонина.
- •Метаболизм аминокислотных гормонов.
- •Метаболизм тиреоидных гормонов.
- •Метаболизм мелатонина.
- •Пути экскреции гормонов и их метаболитов.
- •Регуляция обмена белков.
- •Этапы синтеза стероидных гормонов.
- •Транспорт гормонов.
- •Специфические транспортные белки плазмы крови.
- •Неспецифические белки.
- •Физиологическая роль связывания гормонов в крови.
- •Периферический метаболизм гормонов.
- •Виды метаболизма:
- •Билет 77. Регуляция обмена белков.
- •Этапы действия стг.
- •Этапы действия инсулина.
- •Половые гормоны.
- •Регуляция водно-солевого обмена.
- •Гормональная регуляция обмена кальция.
- •Функции кальция.
- •Биохимические принципы витаминотерапии
- •Белки плазмы крови.
- •Высаливание.
- •Функции белков плазмы крови.
- •Альбумины.
- •Строение гемоглобина.
- •Функция гемоглобина.
- •Производные гемоглобина.
- •Типы гемоглобинов.
- •Физиологические типы гемоглобина.
- •Аномальные типы гемоглобина
- •Патология обмена гемоглобина.
- •Порфирии.
- •Синтез гема.
- •-Глобулины.
-Глобулины.
Трансферрин– связывает и транспортирует железо в различные ткани, регулирует концентрацию. М.М. 90 кД, концентрация – 2 – 3 г/л, синтезируется в печени и в макрофагальной системе. Имеет 2 активных центра, связывает 2 атома железа. Связывает и переноситZn,Cuи витаминD.
Трансферрин предотвращает избыточное накопление Fe3+в тканях и потерю его с мочой.
Уменьшение содержания трансферрина отмечается при гепатитах, опухолях, нефротическом синдроме. Повышение содержания связано с усиленным распадом эритроцитов.
Холестерин в патологии.
Холестериноз – накопление содержания холестерина в организме.
Не осложненный холестериноз – (физиологическое старение, старость, естественная смерть) проявляется накоплением холестерина в плазматических мембранах клеток в связи с уменьшением синтеза стероидных гормонов (стероидогенеза).
Осложненный – атеросклероз в форме ишемической болезни сердца (инфаркт миокарда), ишемия мозга (инсульт, тромбоз), ишемия конечностей, ишемии органов и тканей, связанный с уменьшением желчегенеза.
Изменения содержания холестерина в плазме крови.
Семейная гиперхолестеринэмия – обусловлена дефектом рецепторов для ЛНП. В результате холестерин не поступает в клетки и накапливается в крови. Рецепторы по химической природе являются белками. В результате развивается ранний атеросклероз.
Накопление холестерина в отдельных органах и тканях.
Болезнь Вольмана – первичный семейный ксантоматоз – накопление эфиров холестерина и триглицеридов во всех органах и тканях, причина дефицит лизосомальной холестеринэстеразы. Ранняя смерть.
Семейная
гиперхолестенинэмия или
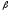 -липопротеинэмия.
Нарушается поглощение ЛНП клетками,
повышается концентрация ЛНП, а также
холестерина. При
-липопротеинэмия.
Нарушается поглощение ЛНП клетками,
повышается концентрация ЛНП, а также
холестерина. При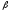 -липопротеинэмии
наблюдается отложение холестерина в
тканях, в частности в коже (ксантомы) и
в стенках артерий. Отложение холестерина
в стенках артерий главное биохимическое
проявление атеросклероза. Вероятность
заболевания атеросклерозом тем выше,
чем больше отношение концентраций ЛНП
и ЛВП в крови (ЛНП снабжает клетки
холестерином, ЛВП удаляет из них избыток
холестерина). Холестерин образует в
стенках сосудов бляшки. Бляшки могут
изъязвляться и язвы зарастают
соединительной тканью (образуется
рубец), в которую откладываются соли
кальция. Стенки сосудов деформируются,
становятся жесткими, нарушается моторика
сосудов, суживается просвет вплоть до
закупорки.
-липопротеинэмии
наблюдается отложение холестерина в
тканях, в частности в коже (ксантомы) и
в стенках артерий. Отложение холестерина
в стенках артерий главное биохимическое
проявление атеросклероза. Вероятность
заболевания атеросклерозом тем выше,
чем больше отношение концентраций ЛНП
и ЛВП в крови (ЛНП снабжает клетки
холестерином, ЛВП удаляет из них избыток
холестерина). Холестерин образует в
стенках сосудов бляшки. Бляшки могут
изъязвляться и язвы зарастают
соединительной тканью (образуется
рубец), в которую откладываются соли
кальция. Стенки сосудов деформируются,
становятся жесткими, нарушается моторика
сосудов, суживается просвет вплоть до
закупорки.
Гиперхолестеринемия – главная причина отложения холестерина в артериях. Но важное значение имеют также первичные повреждения стенок сосудов. Повреждения эндотелия могут возникать в следствие гипертонии, воспалительных процессов.
В области повреждения эндотелия в стенку сосудов проникают компоненты крови, в том числе липопротеиды, которые поглощаются макрофагами. Мышечные клетки сосудов начинают размножаться и тоже фагоцитировать липопротеиды. Ферменты лизосом разрушают липопротеиды, кроме холестерина. Холестерин накапливается в клетке, клетка гибнет, а холестерин оказывается в межклеточном пространстве и инкапсулируется соединительной тканью – образуется атеросклеротическая бляшка.
Между отложением холестерина в артериях и липопротеидами крови происходит обмен, но при гиперхолестеринемии преобладает поток холестерина в стенки сосудов.
Методы профилактики и лечения атеросклероза направлены на уменьшение гиперхолестеринемии. Для этого применяют малохолестериновую диету, лекарства увеличивающие эксткрецию холестерина или ингибирующие его синтез, прямое удаление холестерина из крови методом гемодиффузии.
Холестираминсвязывает желчные кислоты и исключает их из кишечно-печеночного кровобращения, что приводит к усилению окисления холестерина в желчные кислоты.
Билет 53
Липопротеид состоит из гидрофобного ядра, образованного триглицеридами и холестерином. Снаружи гидрофобное ядро окружено белком, это фактор стабильности липопротеида (заряд белковой молекулы и водная оболочка не позволяет частицам слипаться).
Фосфолипиды связаны с белком, а хвост фосфолипида погружен в гидрофобное ядро. Фосфолипиды выполняют функцию связывания за счет дифильности. Липопротеид – это не макромолекула, т.к. здесь есть гидрофобные взаимодействия, слабые полярные взаимодействия. Это надмолекулярная структура, она может терять или приобретать новые компоненты.
Хиломикроны – самые крупные липопротеиды. Содержат 2% белка, 98% липиды, в основном триглицериды, которые поступают с пищей.
Синтезируются в кишечнике, переносят в основном триглицериды пищи, холестерин из кишечника в жировую ткань и печень. Триглицериды в составе хиломикронов легко гидролизуются в капиллярах жировой ткани и других периферических тканях.
В составе липопротеидов обязательно есть белок. Белки липопротеидов называются аполипопротеинами. Они бывают А,В,С,Д,Е (апо А, апо Е).
Хиломикроны содержат апо-А,В,С,Е.
Плазма крови желтая, прочная, аполесцирующая жидкость. После еды плазма мутная, хилезная, из-за высокого содержания хиломикронов.
Липопротеиды очень низкой плотности – ЛПОНП (ЛОНП), Содержат 5 – 7% белка, остальные липиды (ТГ + холестерин). ЛПОНП транспортируют эндогенные триглицериды, которые синтезировались в печени, к жировой ткани. В крови ЛПОНП, обогащаясь холестерином превращаются в ЛНП.
Аполипопротеиды представлены апо В,С,Е.
Липопротеиды низкой плотности (ЛПНП = ЛНП) – содержат 10 – 15% белка, 50% холестерина. Основная транспортная форма холестерина и холестеридов. Образуется в плазме крови и обеспечивает перенос холестерина к периферическим тканям. ЛНП – апо-В
Липопротеиды высокой плотности (ЛПВП = ЛВП). 50% белка, 50% распределены между липидами. Уносят избыток холестерина от тканей к печени. Образуются в крови. ЛВП – апо-Д.
Гиперлипопротеинемии:
Тип 1: до хуя ТАГ; много ХМ
Тип 2: до хуя холестерина; много ЛНП, атерогенный
Тип 3: до хуя холестерина, много ТАГ; много ЛОНП и ЛНП, атерогенный
Тип 4: много ТАГ; много ЛОНП
Тип 5: много холестерина, до хуя ТАГ; много ЛОНП
Билет 51
Нарушение липидного обмена возникает при диабете чаще вторич- но, в результате первичных изменений в обмене углеводов. При декомпенсированном диабете часто повышается содержание в плазме СЖК, триглицеридов и холестерина. Распространенность гипер- гликемии при ИЗСД может достигать 50% (Chase P.H. et all, 1976). Увеличение концентрации СЖК является следствием их усиленного вы- свобождения из жировых депо, т.к. скорость образования новых жирных кислот у больных диабетом снижена. Таким образом, при диабете увели- чен приток СЖК из жировых депо в печень и другие ткани. Усиление ли- полиза происходит в результате выпадения нормального тормозного вли- яния инсулина на гормончувствительную липозу в жировой ткани. Кроме того снижение утилизации глюкозы приводит к уменьшению содержания глицерин-3-фосфата, необходимого для реэстерификации жирных кислот в самой жировой клетке. Механизм гиперглицеридемии при диабете более сложен. В норме богатые триглицеридами липопротеины попадают в плазму либо в виде хиломикронов, образующихся из жира, содержащегося в пище, либо в ви- де липопротеинов очень низкой плотности (ЛПОИП), синтезируемых в пе- чени и кишечнике. Высвобождение жирных кислот из триглициридов обо- их видов и их поглощение жировой тканью зависят от липопротеиновой липазы, содержащейся в эндотелии капилляров и активизирующейся ин- сулином. При не леченном или недостаточно компенсированном диабете снижение активности липопротеиновой липазы обусловливает повыше-ние уровня триглицеридов в плазме, что влияет на содержание хиломик- ронов, ЛПОНП или чаще обоих кланов липопротеинов. В повышении син- теза триглицеридов может играть роль и увеличенная доставка жирных кислот в печень, поскольку в этом органе образование эфиров между жир- ными кислотами и глицерином при диабете не нарушается. В результате у больного декомпенсированным диабетом, несмотря на практически пол- ное прекращение синтеза жирных кислот, может увеличиваться перегру- женная жирами печень и повышаться уровень триглицеридов в крови
Билет 39
Экзогенные жиры
липаза слюныpH=6,8..7,2

липаза желудка(pH=1,5..2,
поэтому малоэффективна,
срабатывает т-ко у грудных детей
в щелочной среде на молоко)

липазы тонкого кишечника
pH=7,8 +NaHCO3+желчные к-ты
{НЭЖК+глицерин+-ацилглицериды+непереваренные ТАГ}+желчные к-ты

НЭЖК+альбумин и глицерин в крови
ХМ в лимфе
ХМ в лёгких

Остатки ХМ, НЭЖК+альбумин, глицерин в крови
Липопротеидлипаза крови
ТАГ –> ЛОНП
( Печень, синтез эндогенных ТАГ)
ЛОНП в крови
Билет 40
АТФ АМФ+PPi

ЖК Ацил-КоА
(ацил-КоА-синтаза) – активация
Цитозоль Межмембранное пространство Матрикс митохондрии
Ацил-КоА Ацилкарнитин КоА-SH




КоА-SHКарнитин Ацил-КоА


Карнитин-ацилтрансфераза (перенос через митохондриальную мембрану)
-окисление
R-CH2-CH2-CH2-C(O)SKoA
ФАД

Ацил-КоА-дегидрогеназа
ФАДН2
R-CH2-CH=CH-C(O)SkoA
H2O
Енолил-КоА-гидратаза
R-CH2-CH(OH)-CH-C(O)SkoA
НАД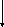

3-гидроксиацилдегидрогеназа
НАДНН
R-CH2-C(O)-CH2-C(O)SkoA
КоА-SH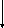

тиолаза
CH3C(O)SKoA
R1-CH2-C(O)SKoA
Если ЖК с нечётным кол-вом атомов углерода, то в конце образуется пропионил-КоА, превращающийся впоследствии в сукцинил-коа.:
CO2
CH3CH2C(O)SKoA
HOOC-CH(CH3)-C(O)SKoA
HOOC-CH2-CH2-C(O)SKoA

мутаза
B7
B12
АТФ АДФ
Связь с цитратным циклом: образование ацетил-коа при каждом цикле окисления, образование сукцинил-коа при окислении кислот с нечётным числом атомов углерода.
Билет 41
|
Митохондрии |
Цитоплазма |
|
Ацетил-КоА+ЩУК
цитрат |
ЩУК+Ацетил-КоА
цитрат |
CO2+АТФ АДФ+Pi

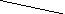
CH3C(O)SKoA
НООС-СН2-СОSКоА
Ацетил-коа-карбоксилаза(В7)
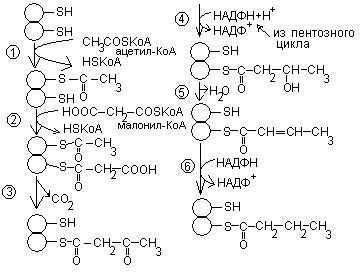
Пальмитиновая кислота служит предшественником всех жирных кислот. Удлинение углеродной цепи происходит за счет дополнительного присоединения ацетил – КоА или малонил – КоА.
Синтез ненасыщенных жирных кислот
Большинство непредельных жирных кислот образуются путем дегидрирования предельных кислот. Линолевая кислота не синтезируется в организме и должна поступать с пищей.
Наиболее интенсивно синтез жирных кислот происходит в печени, жировой ткани, молочных железах.
Для синтеза жирных кислот необходим НАДФ Н2, который образуется в пентозном цикле.
При выраженном дефиците инсулина нарушается не только накопление энергетического материала в состоянии сытости, но происходит и черезмерная мобилизация эндогенных его запасов в состоянии голода(например, гипегликемия, гипераминоацидемия, гиперлипоацидемия натощак).В большинстве случаев тяжелой формы диабета (диабетический кетоацидоз) наблюдается черезмерная продукция глюкозы, а также выраженное ускорение катаболизма( липолиза, протеолиза).