
5) Адиабатный процесс
Адиабатный процесс – это процесс, при котором рабочее тело не обменивается теплотой с окружающей средой (dq=0). Для получения графика процесса вp-vкоординатах выполним некоторые преобразования.
В соответствии с первым законом термодинамики dq=cv·dT+p·dv=c·dT, гдес– теплоёмкость термодинамического процесса. Тогда можно записать, что
![]()
Работа газа в адиабатном процессе выполняется за счёт его внутренней энергии. Так как в адиабатном процессе отсутствует обмен теплотой с окружающей средой, то в соответствии с первым законом термодинамики имеем l+Δu=0 или l=-Δu. Поэтому

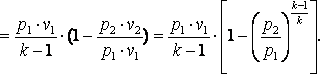
Изменение энтальпии газа в адиабатном процессе может быть определено исходя из следующих соображений:

Энтропия газа в адиабатном процессе не изменяется, так как dq=0. Поэтому в T-s координатах адиабатный процесс изображается прямой линией, параллельной оси температур.
6) При равных условиях энтальпия больше чем внутренняя энергия, потому что энтальпия есть теплота при постоянном давлении, а внутренняя энергия теплота при постоянном объеме. А из уравнения Майера известно что Ср >Сv, поэтому при равных условиях энтальпия численно больше внутренней энергии.
1) Эксергия(эксэргия; отгреч.ek,ех— приставка, означающая высокую степень, игреч.ergon— работа) — частьэнергии, равная максимальной полезнойработе, которую может совершить термодинамическаясистемапри переходе из данного состояния всостояние равновесиясокружающей средой. Эксергией иногда называетсяработоспособностьсистемы. Использование понятия эксергии даёт возможность количественно определить влияниенеравновесиятермодинамическихпроцессовнаэффективностьпреобразования энергии, то есть позволяет вычислять особенностивторого начала термодинамики: выделить ту часть энергии, которая не может быть использована из-за газодинамических явлений, трения,теплообмена. Такой подход даёт возможность анализировать степень термодинамического совершенства того или другого элемента установки и не требует предварительной оценки работоспособности всей установки в целом.
Эксергия (от греч. ex — приставка, обозначающая здесь высокую степень, и érgon — работа), работоспособность, термин, применяемый в термодинамике для обозначения максимальной работы, которую может совершить система при переходе из данного состояния в равновесие с окружающей средой. Работа, совершаемая системой в каком-либо термодинамическом процессе, оказывается максимальной лишь в том случае, если осуществляемый процесс — равновесный.
ЭКСЕРГИЯ
- термодинамич. ф-ция, определяющая
работоспособностьмассы в поточной системе; макс, кол-во
работы, к-рое может быть получено от
поточной системы в обратимом переходе
её из исходногосостоянияв состояние равновесия с окружающей
средой, имеющей пост, темп-руT0,
энтальпию H0иэнтропию S0(при отсутствии др. источников теплоты,
кроме окружающей среды). Э. является
ф-цией состояния и определяется
приращением энтальпииHи энтропии
S; она равна![]() гдеH-H0и S-S0
соответственно приращение энтальпии
и энтропии.
гдеH-H0и S-S0
соответственно приращение энтальпии
и энтропии.
2) Часть энергии системы, которая может быть преобразована в энергию организованных форм, называется эксергией. Остальная часть называется анергией. Мерой эксергии является максимальная полезная работа, которую можно получить при обратимом изменении состояния системы от заданного (при параметрах р,Т) до состояния равновесия с окружающей средой при параметрах р0 и Т0. Таким образом, в отличие от энергии, эксергия является функцией не только параметров системы, но и параметров окружающей среды. Поэтому при расчете эксергии окружающая среда должна иметь постоянную температуру и давление.
3) Параметры окружающей средыне зависят от параметров рассматриваемой системы, обычно предполагаются постоянными и, согласно указанному определению эксергии, должны находиться в термодинамич.равновесиис параметрами системы. Однако, строго говоря, это условие невыполнимо, поскольку в среде всегда существуют градиенты т-р, давлений и хим. потенциалов (что в практич. расчетах можно не учитывать). Для полной характеристики среды достаточно знать не более трех параметров (как правило, т-ру, давление, хим. состав). До тех пор пока все параметры системы не сравняются с соответствующими параметрами среды,равновесиене будет достигнуто и система может производить определенную работу, т. е. обладает эксергией. При эксергетическом анализе работы пром. установок в качестве окружающей среды принимают атм. воздух. Из самого понятия "эксергия" следует, что эксергия окружающей среды равна нулю. Эксергия систем, которые находятся в равновесии с окружающей средой равны нулю.
4)
В
соответствии со II
законом термодинамики, для работы
термодинамической системы необходим
не только подвод тепла, но и отвод тепла,
следовательно подведенное тепло
 не может быть полностью превращено в
работу.
не может быть полностью превращено в
работу.

Т – рабочая температура рассматриваемой системы.
 –эксергетическая
температурная функция. В рассматриваемом
примере она оценивает какая часть
подведенной тепловой энергии может
быть превращена в работу.
–эксергетическая
температурная функция. В рассматриваемом
примере она оценивает какая часть
подведенной тепловой энергии может
быть превращена в работу.

Покажем,
что эксергетическая температурная
функция
 равна КПД прямого цикла Карно.
равна КПД прямого цикла Карно.

5) Эксергия теплового потока - определяется максимальной работой, которая может быть получена в обратимой системе преобразования теплового потока в работу в интервале между температурой этого потока и температурой окружающей среды.
Эксергия термомеханическая - часть эксергии потока вещества, определяемая максимальной работой выравнивания давления и температуры вещества до уровня этих параметров в окружающей среде. Подразделяется на эксергию термическую, связанную с выравниванием температур, и эксергию механическую, связанную с выравниванием давлений.
Эксергия измеряется в тех же единицах, что и энергия и работа,- в Дж, эксергия потока вещества - в Вт, потока теплоты - в Дж/с. Таким образом, эксергия, характеризуя качество энергии пром. системы, т. е. способность быть превращенной в полезную работу, является универсальной мерой энергетических ресурсов.
