
- •1.2. Атомная, молекулярная и молярная масса
- •1.3 Основные газовые законы в химии
- •1.5. Эквиваленты и закон эквивалентов
- •1.6. Основные классы неорганических веществ.
- •151. Получение оксидов металлов
- •152.Получение оксидов неметаллов
- •1.7. Типы химических реакций. Составление уравнений реакций.
- •1.8 Стехиометрические расчеты
- •2.3. Химическая кинетика.
- •3.3.4. Теория гибридизации и оэпво
- •3.4. Межмолекулярное взаимодействие. Агрегатное состояние вещества.
1.3 Основные газовые законы в химии
61.Уравнение состояния газа выведено
Д.И. Менделеевым и Клайпероном. Оно
записывается:![]() ,
где Р - давление, при котором находится
газ,V- объем газа,m- масса газа, М - молекулярная масса газа,R- молярная газовая
постоянная, Т - температура системы.
Уравнение также называется уравнением
Менделеева-Клайперона. Пример: найти
объем 3-х моль газа, находящегося при
106.8 кПа и температуре 400К:
,
где Р - давление, при котором находится
газ,V- объем газа,m- масса газа, М - молекулярная масса газа,R- молярная газовая
постоянная, Т - температура системы.
Уравнение также называется уравнением
Менделеева-Клайперона. Пример: найти
объем 3-х моль газа, находящегося при
106.8 кПа и температуре 400К:![]() литра.
литра.
62.![]()
63.а)![]()
б)
![]()
в)
![]()
64. Газ называется идеальным, если газ подчиняется законам Клайперона-Менделеева и Рауля. Характеристика реального газа близка к идеальному, если форма его молекул близка к идеальному шару, если отсутствует взаимодействие между молекулами и столкновения молекул можно принять за упругое соударение.
65.![]() ,
следовательно,
,
следовательно,![]() г/моль.
г/моль.
66.![]() ,
следовательно,
,
следовательно,![]() г/моль.
г/моль.
67.![]() ,
следовательно,
,
следовательно,![]() г.
г.
68.![]() ,
=>
,
=>![]() литров.
литров.
69.![]() ,
следовательно,
,
следовательно,![]()
70.![]() ,
=>
,
=>![]() кПа
кПа
71.Уравнение Клайперона записывается:![]() ,
где Р - давление, при котором находится
газ,V- объем газа,m- масса газа, М - молекулярная масса газа,R- молярная газовая
постоянная, Т - температура системы. Оно
используется при нахождении неизвестного
параметра состояния газа (давления,
массы, температуры, молярной массы,
объема) по известным параметрам, входящим
в уравнение. Пример: найти объем 3-х моль
газа, находящегося при 106.8 кПа и температуре
400К:
,
где Р - давление, при котором находится
газ,V- объем газа,m- масса газа, М - молекулярная масса газа,R- молярная газовая
постоянная, Т - температура системы. Оно
используется при нахождении неизвестного
параметра состояния газа (давления,
массы, температуры, молярной массы,
объема) по известным параметрам, входящим
в уравнение. Пример: найти объем 3-х моль
газа, находящегося при 106.8 кПа и температуре
400К:![]() литра.
литра.
72.Нормальными условиями для газов
являются 298 К, 101,3 кПа.![]() =>
=>![]() литра
литра
73.Нормальными условиями для газов
являются 273 К, 101,3 кПа.![]() =>
=>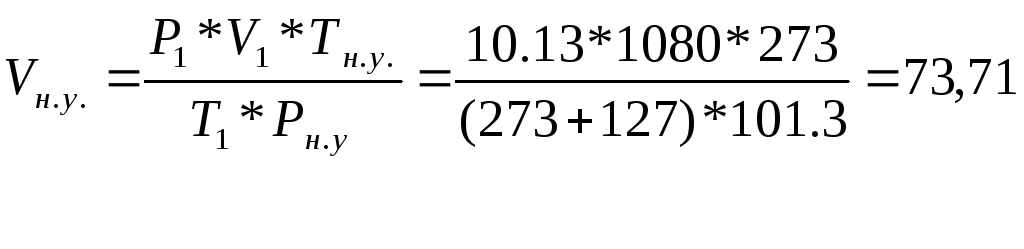 литра.2986729,2/40520=73,71
литра.2986729,2/40520=73,71
74. Парциальное давление газа пропорционально объемной доле газа в смеси газов.Р’(N2)= Р(общ)*w%(N2) / 100% = 101325*78.1 / 100 = 79135 Па.Р’(О2)= Р(общ)*w%(О2) / 100% = 101325*20.9 / 100 = 21177 Па.Р’(Ar)= Р(общ)*w%(Ar) / 100% = 101325*0.93 / 100 = 942 Па. .Р’(СО2)= Р(общ)*w%(СО2) / 100% = 101325*0.03 / 100 = 30.4 Па.
75.Парциальное давление газа пропорционально объемной доле газа в смеси газов:w%(NO)=P(NO) * 100% /P(общ) = 39990*100 / (39990 + 66630) = 37,5%;w%(NO2)=P(NO2) * 100% /P(общ) = 66630*100 / (39990 + 66630) = 62,5%;
76.
|
Дано V(CH4) = 0.03 м3 Р(СН4) = 96.0 кПа V(H2) = 0.04 м3 Р(Н2) = 84.0 кПа V(CО) = 0.01 м3 Р(СО) = 108.8 кПа |
Найдем количество каждого вещества из закона Клайперона-Менделеева: n = PV/RT n(CH4) = 96*30/(8.31*298) = 1.163 моль. Доля газа х1 = 1.163*100%/2.959 = 39,3% n(H2) = 84*40/(8.31*298) = 1.357 моль. Доля газа х1 = 1.357*100%/2.959 = 45,9% n(CО) = 108.8*10/(8.31*298) = 0.439 моль. Доля газа х1 = 0.439*100%/2.959 = 14,8% Vобщ = 30 + 40 + 10 = 80 литров, n(общ) = 1.163+1.357+0.439 = 2.959 моль, следовательно, Робщ = nRT/V = 2.959*8.31*298/80 = 91.6 кПа Парциальные давления: П(СН4) = 91.6*0.393 = 36 кПа, П(Н2) = 91.6*0.459 = 42 кПа, П(СО) = 91,6*0.148 = 13,6 кПа |
77.V1(N2)
= 120мл = 0.120 л; Т = 200С = 293 К; Р(общ) =
100 кПа, Р(Н2О) = 2.3 кПа.Vн.у.(N2)
= ?. Найдем парциальное давление
азота: Р1(N2)= Р(общ)
- Р(Н2О) = 100 - 2.3 = 97.3 кПа.![]() =>
=>![]() литра.
литра.
78.V1(Н2) = 250мл =
0.250 л; Т = 260С = 299 К; Р(общ) = 98.7 кПа,
Р(Н2О) = 3.4 кПа.Vн.у.(Н2)
= ?. Найдем парциальное давление водорода:
Р1(Н2)= Р(общ) - Р(Н2О) = 98.7 - 3.4 =
95.3 кПа.![]() =>
=>![]() литра.
литра.
79. Закон Авогадро: В равных объемах различных газов при одинаковых температуре и давлении содержится одинаковое число молекул.
Следствие 1. Объемы, занимаемые 1 моль газа, должны быть одинаковыми для всех газов.
Следствие 2. Один моль любого газа содержит 6,02*1023соответствующих молекул.
Число Na= 6.02*1023носит название постоянной Авогадро и выведено с использованием его закона. Из закона Авогадро следует, что два газа одинаковых объемов, хотя и содержат равное число молекул, имеют неодинаковые массы: масса одного газ во столько же раз больше массы другого газа, во сколько раз относительная молекулярная масса первого больше, чем относительная молекулярная масса второго. Закон Авогадро имел фундаментальное значение в истории развития атомно-молекулярного учения.
80. Закон Авогадро: В равных объемах различных газов при одинаковых температуре и давлении содержится одинаковое число молекул.m(O2) = 8.0 г.n(O2) =m/M= 8 / 32 = 0.25 моль.V(O2) =n*Vм = 0.25 * 22.4 = 5.6 литров.
81.V(H2) = 280 литров.n(H2) =V/Vм = 280 / 22.4 = 12.5 моль.m(Н2) =n(H2)*M(Н2) = 12.5*2 = 25 грамм.
82.V(газа) = 600 мл.n(газа)=V/Vм = 0.6 / 22.4 = 0.0268 моль.M(газа)=m(газа) /n(газа) = 1.714 / 0.0268 = 64 грамм/моль.
83.n(СО2) = 10 моль.V(СO2)=n*Vм = 10 * 22.4 = 224 литра.m(СО2)=n(СО2)*M(СО2) = 10*44 = 440 грамм.
84.V(газа) = 2 л.n(газа) =V/Vм = 2 / 22.4 = 0.089 моль.а)Молярная масса газа:M(газа) =m(газа) /n(газа) = 2.5 / 0.089 = 28 грамм/моль.б)Молекулярная масса газа = 28.в) абсолютная масса одной молекулыm= 28 / 6,02*1023= 4,65 *10-23грамм.
85. а) Даны равные количества азота и водорода:n(H2) =n(N2). Согласно закону Авогадро, «в равных объемах различных газов при одинаковых температуре и давлении содержится одинаковое число молекул», т.е. отношение объемов азота и водорода равно 1.
б) Даны равные массы азота и водорода:
m(H2)
=m(N2).=> V(H2)
= n(H2)/Vм
= =![]() =>
=>![]()
86.Газ называется идеальным, если газ подчиняется законам Клайперона-Менделеева и Рауля. Характеристика реального газа близка к идеальному, если форма его молекул близка к идеальному шару, если отсутствует взаимодействие между молекулами и столкновения молекул можно принять за упругое соударение. Молекулы водорода по свойствам более близки к идеальному газу, чем молекулы азота. Поэтому молярный объем водорода ближе к идеальному значению, чем молярный объем азота.
87.Относительная плотность газа вещества А по веществу B - отношение относительной молекулярной массы А к относительной молекулярной массе вещества B.DB(A)=M(A)/MB).Dвоздуху(Cl2) =M(Cl2)/M(воздуха) = 71/29 = 2.45;Dкислороду(С2Н4) =M(C2Н4)/M(О2) = 28/32 = 0.875.
88.Dвоздуху(Ацетона)=2.DB(A)=M(A)/MB), следовательно, М(ацетона) =Dвоздуху*М(воздуха) = 2*29 = 58 г/моль.
89.Dкислороду(Sx)=8.DB(A)=M(A)/MB), следовательно, М(Sx)=Dкислороду*М(кислорода) = 8*32 =256 г/моль. х = М(Sx)/ М(S) = 256/32 = 8 атомов.
90.Dводороду(N2+O2)=15.DB(A)=M(A)/MB). Средняя молекулярная масса смеси азота и кислорода равна М(N2+O2) =Dводороду*М(водорода) = 15*2 = 30 г/моль. Пусть х и у - соответственно объемные доли азота и кислорода в смеси. Составим систему:
х*М(N2) + у*М(O2) = 30
х + у = 1, следовательно у = 1 - х
х*М(N2) + (1 - х)*М(O2) = 30 => 28x+ 32 - 32x= 30 =>x = 0.5=>y =1 - 0.5= 0.5
91.Валентностью данного элемента называется число атомов соединяющегося с ним другого элемента. К элементам переменной валентности относятся: азот:B=1 -N2O,B=2 -NO,B=3 -N2O3; железо: В=2 -FeO,B=3Fe2O3, и многие другие элементы.
92.Валентностью данного элемента называется число атомов соединяющегося с ним другого элемента, т.е. валентность - это число связей с другими элементами, которые образует данный элемент. Постоянная валентность = 1: К,Li, Na, Rb - KCl, LiF, NaOH, RbF. Постоянная валентность = 2:Ca,Mg,Be-CaS,Mg(OH)2,BeCl2, Постоянная валентность = 3:Al,Ga,In-AlPO4,Ga(OH)3,InCl3, К элементам переменной валентности относятся: азот:B=1 -N2O,B=2 -NO,B=3 -N2O3; железо: В=2 -FeO,B=3Fe2O3, и многие другие элементы.
93.Валентностью данного элемента называется число атомов соединяющегося с ним другого элемента, т.е. валентность - это число связей с другими элементами, которые образует данный элемент. Соответственно, максимальная валентность - это максимальное число связей, которые может образовать элемент в соединении. Максимальная валентность:P= 5 -H3PO4,Cl= 7 -HClO4,S= 6 -SO3,Xe= 8 -XeF8.
94.Максимальная валентность:Sn=4 -H2SnO3,Sb=5 -SbCl5,Se=6 -SeO3,Br=7 -HBrO4.
95.Максимальная валентность:V=5 -HVO3,Cr=6 -K2CrO4,Mn=7 -KMnO4,Ru=8 -RuO4.
96. Значения валентности различаются на 2 у:серы-SO2/SO3,хлора-HClO/HClO2,таллия-TlCl/TlCl3.
97. Значения валентности различаются на 1 у:меди-Cu2O/CuO,железа-FeO/Fe2O3,титана-Ti2O3/TiO2.
98.
|
Соединение |
H2S |
SO3 |
H2SO3 |
SO2 |
H2SO4 |
CS2 |
|
Валентность серы |
2 |
6 |
4 |
4 |
6 |
2 |
99.
|
Соединение |
NH3 |
N2O |
NO |
N2O3 |
HNO2 |
NO2 |
N2O5 |
HNO3 |
NH4NO3 |
NH4NO2 |
N2H4 |
Na3N |
|
Валентность азота |
3 |
1 |
2 |
3 |
3 |
4 |
5 |
5 |
3,5 |
3,3 |
2 |
3 |
|
Соединение |
NaCl |
CaCl2 |
Cl2O |
HClO |
HClO2 |
KClO3 |
Cl2O7 |
HClO4 |
|
Валентность хлора |
1 |
2 |
1 |
1 |
3 |
5 |
7 |
7 |
101.По периоду максимальная валентность химических элементов увеличивается в связи с добавлением валентных электронов.Si: В=4 - SiO2, P: В=5 - PCl5, S: В=6 - SO3, I: В=7 - HIO4.
102. Максимальная валентность химического элемента совпадает с номером группы в ПС.Ge: В=4 -GeO2,P: В=5 -PCl5,Se: В=6 -SeO3,Cl: В=7 -HClO4.
103.Максимальная валентность химического элемента совпадает с номером группы в периодической системе, поэтому по периоду с увеличением атомного номера максимальная валентность увеличивается. По группе, в связи с уменьшением притяжения ядром валентных (внешних) электронов максимальная валентность с увеличением атомного номера уменьшается. Максимальная валентностьSn=4 -H2SnO3,Sb=5 -SbCl5,Тe=6 - ТeO3,Br=7 -HBrO4,Xe=8 -XeF8.
104.Максимальная валентность химического элемента совпадает с номером группы в ПС. Третий период -Na:B=1 -NaCl,Mg:B=2 -MgS,Al:B=3 -AlN,Si: В=4 -SiO2,P: В=5 -PCl5,S: В=6 -SO3,Cl: В=7 -HClO4.
105.Максимальная валентность химического элемента совпадает с номером группы в ПС. Четвертый период -K:B=1 -KCl,Ca:B=2 -CaS,Ga:B=3 -GaN,Ge: В=4 -GeO2,As: В=5 -AsCl5,Se: В=6 -SeO3,Br: В=7 -HBrO4.
106. Это переходныеd- ,f-металлы. Например, Co, Rh, Tb, Cm: Co(OH)3, RhCl3, TbCl3, CmBr3.
107. AlH3, Al2O3, AlN, Al4C3, Al2S3, AlF3
108. PH3, P2O5, AlN, Na3P, P2S5, PF5
109. Хлориды: BCl3,SiCl4, PCl5, SnCl2, MgCl2, Сульфиды: B2S3, SiS2, P2S5, SnS, MgS.
110. Оксиды азота: I - N2O, II - NO, III - N2O3, IV - NO2, V - N2O5; Марганца: II - MnO, III - Mn2O3, IV - MnO2, VI - MnO3, VII - Mn2O7; Хрома: II - CrO, III - Cr2O73, IV - CrO2.
111. Структурная формула не отражает реального строения молекулы или элементарной кристаллической решетки, однако позволяет рассчитать кратность связей в молекуле и валентность атомов.Al2O3 - O=Al-O-Al=O,
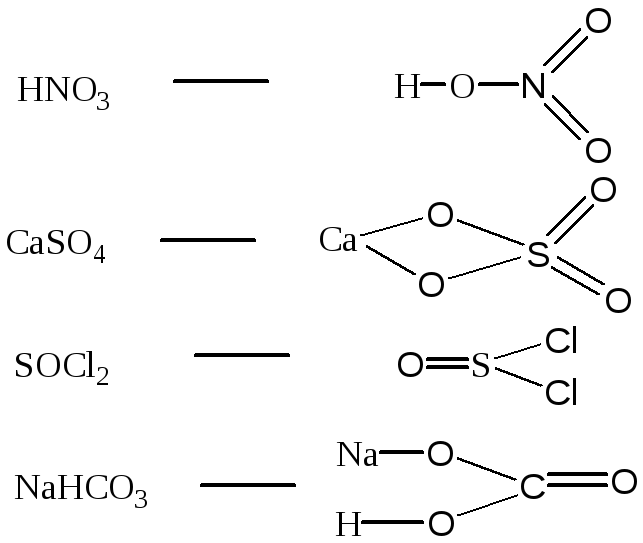
112.Структурная формула позволяет рассчитать кратность связей в молекуле и валентность атомов.
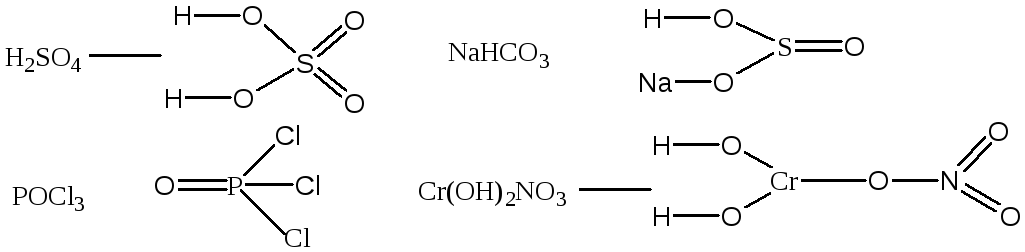
113. Структурная формула позволяет рассчитать кратность связей в молекуле и валентность атомов.
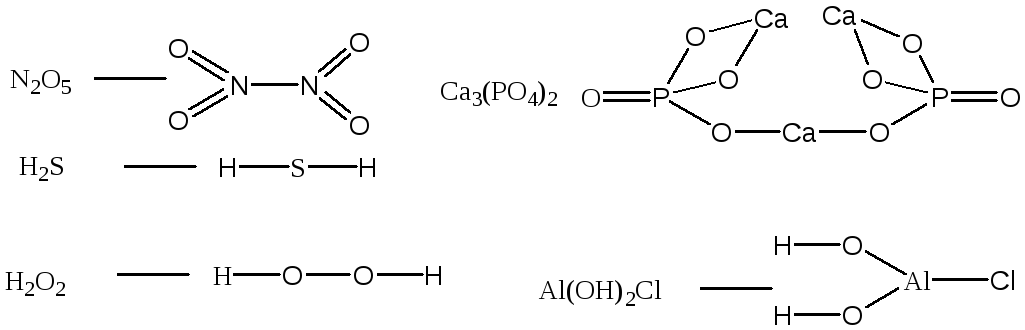
115.Валентность элементов совпадает с количеством связей между атомами в молекуле:
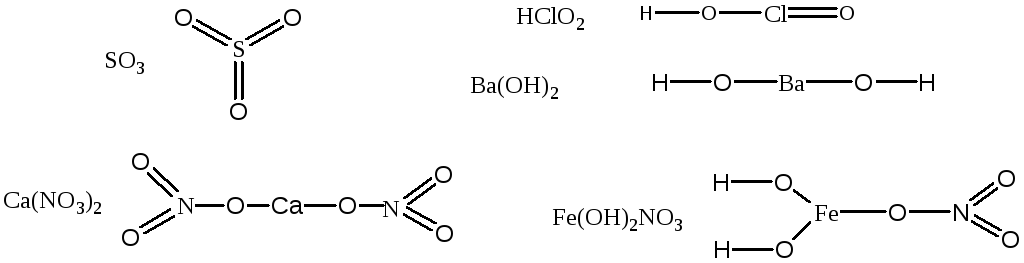
Структурная формула не отражает реального строения молекулы или элементарной кристаллической решетки.
116.Фосфорная кислота - трехосновная, фосфористая - двухосновная, фосфорноватистая - одноосновная (по числу атомов водорода, связанных с атомами кислорода).
117.Номер группы, в которой элемент расположен, совпадает с валентностью элемента по кислороду. Номер группы минус 8 - валентность элемента по водороду.Углерод(4 группа) - по кислороду В=4, по водороду В=8-4=4,азот(5 группа) - по кислороду В=5, по водороду В=8-5=3.сера (6 группа) - по кислороду В=6, по водороду В=8-6=2,хлор(7 группа) - по кислороду В=7, по водороду В=8-7=1.
118.В соединениях с кислородом валентность элемента совпадает с количеством валентных электронов, т.к. кислород притягивает электроны, а в соединении с водородом - с числом вакантных мест для электронов на валентном уровне, т.к. водород отдает электроны. Сумма вакантных мест и валентных электронов равна восьми, что объясняет наблюдаемую закономерность.
119. Электронная валентность кислорода одинакова, а стехиометрическая разная в соединениях: Н2О (Вэ=2, Вс=2) и Н2О2- (Вэ=2, Вс=1).
120.Хлорид аммония:NH4Cl- электронная валентность =3, стехиометрическая = 4; перекись водорода: Н2О2- электронная валентность =2, стехиометрическая = 1.
