
Климанов Дозиметрическое планирование лучевой ч2 2008
.pdfпервого полномасштабного ускорителя протонов с гантри [59] для клинического применения НЗБТ.
3.5. Методы расчета доз в нейтрон-захватной терапии
В настоящее время практическое применение находит пока лишь НЗТ с использованием реакции захвата на боре. Поэтому рассмотрим методы расчета доз, главным образом, для НЗБТ.
Ионизирующее излучение, воздействующее на пациента при НЗБТ, является сложным смешанным полем с компонентами, имеющими высокие и низкие ЛПЭ. Соотношение между компонентами зависит от пространственного, спектрального и углового распределения падающих нейтронов, а также от геометрии и элементного состава мишени. При планировании облучения и дозиметрии поле излучения в общем случае делится на четыре первичных дозовых компоненты: доза от тепловых нейтронов, доза от быстрых нейтронов, доза от фотонов и доза 10В (доза от реакции захвата на 10В). Доза от тепловых нейтронов Dp создается, в основном, за счет реакции захвата 14N(n,p)14C. Для ткани мозга вклад этой реакции в керму тепловых нейтронов составляет 96 %. Основной вклад в керму быстрых нейтронов Dn вносит упругое рассеяние нейтронов на ядрах водорода 1H(n,n′)1H. Для ткани мозга взрослого человека этот вклад для нейтронов в энергетическом интервале 600 эВ ÷ 3 МэВ равняется 90 %. Другие нейтронные реакции на ядрах 12С, 16O и 12Р создают вклад в пределах 4 ÷ 8 %. Фотонная доза Dγ обусловлена двумя источниками: фотоны “загрязняющие” нейтронный пучок за счет различных реакций захвата нейтронов в мишени и системе коллимирования; фотоны, рождающиеся при реакции захвата водородом ткани 1H(n,γ)2H. Доза DB от реакции на 10В(n,α)7Li создается преимущественно тепловыми нейтронами. Она зависит также от микрораспределения борного препарата [60], времени после введения препарата [61] и индивидуальных особенностей пациента [62]. Таким образом, полная доза при НЗТ равна
DT = Dp + Dn + Dγ + DB . |
(3.31) |
Расчет всех четырех дозовых компонент является значительно более сложной задачей, чем определение доз в традиционной лучевой терапии, которое обычно опирается на полуэмпирические алгоритмы и измерения в водном фантоме. Ввиду большой сложности проблемы ее решение требует строгого рассмотрения транспорта нейтронов в
231
трехмерной геометрии облучения. Поэтому в настоящее время для аккуратного планирования НЗБТ, в основном, применяется вероятностный метод Монте-Карло. Вместе с тем, в литературе имеются публикации, посвященные применению для планирования НЗБТ детерминистских методов, в частности, Sn-метода [63,64]. Продолжается также работа по разработке эмпирических алгоритмов для расчета дозы при планировании НЗБТ [65], однако на сегодня пока еще нет алгоритма, адекватного для клинического применения.
В настоящее время возможности сравнения программного обеспечения для планирования НЗБТ ограничено, фактически, только тремя кодами, которые используются клинически в США и Европе: MacNCTPlan [66], созданный в Массачузеттском Технологическом Институте (США), BNCT_rtpe [67] и их приемник SERA [68]. Два последних кода разработаны в Национальной Лаборатории Инженерии и Окружающей Среды (г. Идахо, США). Результаты сравнения результатов планирования для одного клинического теста BNCT, проведенные в работе [69] с использованием кодов MacNCTPlan и BNCT_rtpe, показали хорошее согласие между ними. Разнообразные сравнения [70] для задач расчета доз в НЗБТ были выполнены между SERA и известной программой MCNP, которая является расчетным модулем в MacNCTPlan. Они также дали вполне удовлетворительные результаты. В литературе были сообщения о разработке систем планирования НЗТ в Австралии [71], Италии [72], Японии [73] и России [74,75]. Однако о клиническом применении этих систем сообщений пока не имеется.
Системы дозиметрического планирования (СДП) для НЗТ, как правило, опираются на транспортные программы, проводящие расчет пространственно-энергетических распределений нейтронов и фотонов в конкретной геометрии облучения пациента. Величина поглощенной дозы определяется как сумма поглощенных доз, создаваемых четырьмя первичными компонентами. Значения поглощенной дозы, обычно, аппроксимируются кермой отдельных компонентов поля излучения [76]. Зависимость кермы нейтронов и фотонов от энергии изучалась в ряде работ [77 – 80]. В приложении в табл…….приводятся численные данные по керме нейтронов для отдельных элементов и некоторых биологически важных материалов. На рис. 3.38 показан вклад в нейтронную керму от отдельных элементов, входящих в состав мозга взрослого человека, а на рис. 3.39 – зависимость кермы от энергии нейтронов для реакции на 10В.
232

Рис. 3.38. Вклад в нейтронную керму от отдельных элементов, входящих в состав мозга взрослого человека, на основе данных работ [78,79]
Если известны пространственно-энергетические распределения плотности потока нейтронов ϕn (r , E) и фотонов ϕγ (r , E) в
облучаемом объеме, то полная мощность поглощенной дозы (в приближении кермы) определяется из выражения:
r |
|
r |
|
r |
r |
|
|
+ |
D&T (r ,t) = ∫dE ϕ |
γ (r , E) ∑ ni (r )kγ,i (E) + ∑n j (r ,t)kγ, j (E) |
|||||||
|
|
|
i Tissue |
|
j Drug |
|
|
|
r |
|
|
r |
|
r |
|
, (3.32) |
|
∫dE ϕn (r , E) |
∑ ni (r )kn,i (E) + |
∑n j (r ,t)kn, j (E) |
|
|||||
|
i Tissue |
|
j Drug |
|
|
|
||
где ni ( rr) – весовая доля i-элемента в ткани в окрестности точки r ; |
||||||||
nj( rr,t) – весовая доля j-элемента, входящего в состав препарата – |
||||||||
нейтрон-захватного |
агента, в |
окрестности точки |
|
r в момент |
||||
времени t; kγ,i(E) и kn,i(E) – керма фотонов и керма нейтронов для i-элемента соответственно.
233
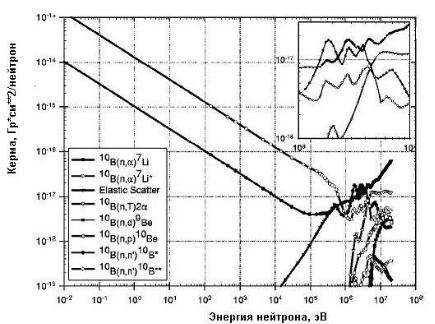
Рис. 3.39. Зависимость кермы от энергии нейтронов для различных реакций захвата на 10В при концентрации бора 1 мкг/г ткани [79]
Формулу (3.32) можно преобразовать, выделив в ней постоянную и переменную по времени составляющие [81]:
& |
r |
& |
r |
& |
|
r |
(3.33) |
D |
(r |
,t) = D |
(r ) + ∆D |
A |
(r ,t), |
||
T |
|
Tissue |
|
|
|
|
|
где
D&Tissue (rr) = ∫dE ∑ni (rr)[ϕγ (rr, E)kγ,i (E) + ϕn (rr, E)kn,i (E)]; (3.34)
i Tissue
∆D&(rr,t) = ∫dE ∑n j (rr,t)[ϕγ (rr, E)kγ, j (E) + ϕn (rr, E)kn, j (E)].
j Drug
(3.35)
Значения полной дозы определяются интегрированием выражения (3.33) по времени.
Введем дополнительно величину относительного весового содержания в ткани нейтрон-захватного препарата (агента) – wA (r,t) . Для нее имеет место соотношение:
wA (rr,t) = ∑n j (rr,t) . |
(3.36) |
j Drug
234

Концентрация нейтрон-захватных агентов в опухоли и окружающих ее тканях является определяющим параметром для расчета доз при планировании НТЗ. Относительное содержание нейтрон-захватного препарата в опухоли и окружающих ее тканей измеряется экспериментально или рассчитывается с помощью фармокинетических моделей миграции препаратов для различных путей их введения – интратуморальном или внутривенном. Для количественных оценок концентрации Gd в опухоли при интратуморальном способе введения препарата “Дипентаст” в работе [82] на основе диффузионной модели получена следующая формула:
|
|
|
erf (r + R0 |
) − erf (r − R0 ) + |
4Dt × |
|
|
||||
|
C |
|
|
|
4Dt |
|
4Dt |
r π |
|
|
|
wA (r,t) = |
0 |
|
|
|
|
, (3.37) |
|||||
|
|
|
|
(r + R0 )2 |
|
(r − R0 )2 |
|
||||
|
2ρtissue |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
) − exp(− |
|
|
|
|
|
|
× exp(− |
|
4Dt |
4Dt |
) |
|
|||
|
|
|
|
|
|
|
|
|
|
||
где R0 = 3 |
3V0 |
; С0 |
= M0/V0; D – коэффициент диффузии; V0 – объем |
||||||||
|
4π |
|
|
|
|
|
|
|
|
|
|
препарата, см3; M0 – масса препарата в растворе, г.
Коэффициент диффузии, определенный для препарата “Дипентаст” радиоизотопным методом, оказался равным D = 0,58 ·10-7 см2/c. На рис. 3.40 приводятся результаты расчета по формуле (3.37) динамики распределения гадолиния в биологической ткани.
Для внутривенного введения препарата расчет динамики концентрации нейтрон-захватного агента (10В) проводится на основе камерных моделей фармакокинетики (рис. 3.41) [33,35,83,84]. Пример расчета по такой модели с использованием фармакокинетических коэффициентов, определенных по экспериментальным данным динамики концентрации нейтрон-захватных агентов в биологических тканях и физиологических жидкостях экспериментальных животных
[83, 84], показан на рис. 3.42.
235

Рис. 3.40. Динамика пространственного распределения Gd в ткани для глубины инжекции 2 см, массы препарата Gd-DTPA М0 = 0,0137 г и объема введенного раствора V0 = 0,1 см3 [83]
Рис. 3.41. Камерная модель миграции препарата при внутривенном введении [83]
236
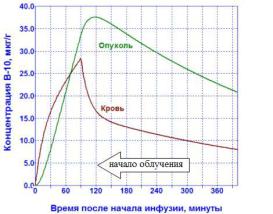
Рис. 3.42. Временная зависимость концентрация 10В в крови и опухоли (инфузия препарата 10BPA в дозе 350 мг/кг животного в течение 1,5 ч. [83]
Выше отмечалось, что так как разные первичные компоненты дозы при НЗТ имеют разные значения ЛПЭ и, следовательно, разные значения ОБЭ, то международные организации рекомендуют [85,86] регистрировать и публиковать поглощенные дозы отдельно для каждого из четырех компонентов. Однако для внутреннего использования и качественных сравнений характеристик пучков при оценке влияния разной фильтрации те же рекомендации не препятствуют применению так называемой “биологически взвешенной дозы”. Хотя по поводу этого термина в литературе (например, [87]) имеются обоснованные возражения (см. ниже) и предлагается термин “взвешенная доза”. Эта характеристика Dw определяется суммированием значений четырех первичных дозовых компонент, умноженных на весовые множители. Расчетное выражение имеет вид:
Dw = wγ Dγ + wn Dn + wp Dp + wB DB ; Гр-экв, (3.38)
где wi – весовые множители; Di выражены в Гр. Во многих работах множители wγ , wn , wp называют коэффициентами относительной
биологической эффективности (ОБЭ), а множитель wB – компаунд-
зависимый фактор (ОБЭ и микрораспределение бора).
Весовые множители, строго говоря, зависят от многих факторов, в том числе и от микродозиметрических распределений. В литературе имеется ряд работ (например, [34,86,89]), в которых предлагаются свои варианты численных значений для этих множителей. В настоящее
237
время условно приняты следующие значения весовых множителей [90]: wγ =1; wn = 3,2 ; wp = 3,2 ; wB =1,3 для нормальной ткани и
wB = 3,8 для опухоли.
3.6. Базовые расчеты пространственного распределения кермы
Для определения корректности результатов расчета дозовых распределений в различных системах планирования важное значение имеет наличие некоторого базового набора данных по этим распределениям, полученным с высокой точностью в типичной для НТЗ геометрии облучения. Ранее попытки получить набор стандартизованных данных ограничивались геометрией прямоугольных водных фантомов. Такие данные полезны для тестирования транспортных программ, например, реализующих метод Монте-Карло. Однако для тестирования систем дозиметрического планирования больше подходят данные, полученные для более реалистических моделей, таких как фантом Снайдера для головы с его кривыми поверхностями, гетерогенной композицией и соответствующими биологическими материалами. Именно в подобной геометрии были проведены базовые расчеты глубинных распределений мощности кермы для пучков нейтронов разных энергий, падающих на голову модифицированного фантома Снайдера [90]. Расчеты выполнялись методом Монте-Карло по программе MCNP4B. Для пересчета спектров нейтронов и фотонов в керму использовались данные работы [78], а для таких элементов, как 10B, Na, S, Cl и K керма факторы были рассчитаны авторами [90].
Оригинальный фантом Снайдера для головы [91] состоит из двух эллипсоидов, разделяющих голову на область черепа и область мозга. В модифицированном фантоме добавлена третья область толщиной 5 мм, моделирующая кожу [92]. Приводимые ниже уравнения специфицируют эти области:
x 2 |
y |
|
2 |
|
z −1 2 |
|
|
|
|
||||||||
|
|
|
+ |
|
|
+ |
|
|
|
|
|
=1; |
(3.39) |
||||
|
9 |
6,5 |
|
||||||||||||||
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
x |
2 |
|
|
|
y |
2 |
z −1 |
2 |
|
|||||||
|
|
|
|
+ |
|
|
|
|
+ |
|
|
|
|
|
=1; |
(3.40) |
|
6,8 |
|
|
|
|
8,3 |
|
|||||||||||
|
|
|
|
9,8 |
|
|
|
|
|
|
|||||||
238

|
x |
2 |
|
|
y |
2 |
z −1 |
|
2 |
|
||
|
|
|
+ |
|
|
|
+ |
|
|
|
=1. |
(3.41) |
7,3 |
10,3 |
8,8 |
|
|||||||||
|
|
|
|
|
|
|
|
|
||||
На рис. 3.43 показаны поперечные сечения фантома, описываемого уравнениями (3.39) – (3.41).
Дополнительно было сгенерировано три воксельных модели фантома головы для связи с КТ, от которых передаются данные в системы планирования. Все три модели состоят из кубических вокселей со сторонами 16, 8 и 4 мм. Каждый воксель заполнен смесью четырех первичных материалов (воздух, кожа, кость и мозг) с 10 %-ными инкрементами (воздух окружает фантом снаружи). Более подробные детали генерации моделей и заполнения вокселей приводятся в электронной базе данных EPAPS [93]. На рис. 3.44 проводится сравнение воксельных моделей с аналитической.
Рис. 3.43. Поперечные сечения модифицированного фантома Снайдера для головы в плоскостях y
= 0 (слева) и x = 0 (справа) [90]
Рис. 3.44. Геометрия облучения фантома головы и сравнение воксельных моделей с аналитической [90] . Ось пучка направлена вдоль оси z на рис. 3.43
239
Расчет глубинных распределений мощности кермы проведен для моноэнергетических пучков нейтронов с энергиями 0,0253 эВ, 1, 2, 10, 100 и 1000 кэВ и моноэнергетических пучков фотонов с энергиями 0,2, 0,5 1, 2, 5 и 10 МэВ. Кроме того, выполнены расчеты для пучка эпитепловых нейтронов, смешанных с 1 %-ным вкладом быстрых нейтронов (10 кэВ – 2 МэВ) и 10 %-ным вкладом тепловых нейтронов (0,001 – 0,5 эВ). Такой пучок близок по составу нейтронов к клиническим пучкам при НЗБТ. Внутри отдельных энергетических интервалов эпитеплового пучка принимался спектр ~ 1/E. В каждом расчете моделировали 50 млн. историй. Статистическая погрешность результатов была меньше 1 % в максимуме распределений. Все пучки имели диаметр равный 10 см и разыгрывались равномерно по площади. Интенсивность всех пучков нормировалась на 1010 частиц/(см2·с) как для нейтронов, так и для фотонов. Концентрация 10В в ткани принималась равной 1 мкг/г. Результаты расчетов для отдельных компонент поля с использованием аналитической модели представлены на рис.3.45. При использовании воксельных моделей результаты близки (различие в пределах 2 – 3 %) к аналитической модели только при размере стороны 4 мм (рис. 3.46). Авторами [90] получено также существенное различие в мощности дозы, создаваемой тепловыми нейтронами, при использовании в расчетах модели свободного газа и функций S(α,β).
240
