
Карцев В.Г. - Избранные методы синтеза и модификации гетероциклов. Том 2 (2003)(ru)
.pdf
OH
Het
R O
O  O
O
16
Het = 5-карбэтокси-2-фурил, 2-бензофурил
Часто в качестве синтонов используют различные производные кумаринов. Одним из них является 3-(бромацетил)кумарин 17, конденсация которого с веществами, содержащими группу CSNH2, при кратковременном нагревании в спирте приводит к 3-(2-X-тиазол-4-ил)кумаринам 18, причем если X = CH2CN, то такие соединения реагируют по Кневенагелю с салициловыми альдегидами, образуя 2,4-(дикумарин-3-ил)тиазолы [22] (схема 5).
|
|
|
|
|
|
Схема 5 |
|
O |
|
|
|
|
S |
|
|
|
|
|
X |
|
|
Br |
|
|
S |
|
|
|
|
|
|
N |
||
|
+ |
|
|
|
|
|
R |
H |
N |
|
X |
R |
|
|
|
O O |
||||
|
O O |
2 |
|
|
|
|
|
17 |
|
|
|
|
18 |
R = H, 5,6-бензо, 7-Et2N;
X= NH2, NHNH2, CSNMe2, CH2CN, N(CH2)4, Ph, 4-MeC6H4, 3,4-MeOC6H3, 4-(Me2N)C6H4, 4-ClC6H4, 4-[N(CH2)4]C6H4
Аналогичная методика получения 3-(тиазол-4-ил)кумаринов приводится в работах [4, 23–28].
Нагреванием соединений 17 с эквимолярным количеством Me2N-CS-X в уксусном ангидриде в присутствии Mg(ClO4)2 получены замещенные перхлораты 5-(кумарин-3-ил)оксатиолия 19 [22] (схема 6).
Схема 6
|
|
|
|
|
|
|
|
|
|
S |
X |
|
|
S |
|
|
|
|
|
+ |
|||
|
|
|
|
|
|
|
|
||||
17 + |
|
|
|
|
|
Mg(ClO4)2 |
R |
|
|
O |
|
|
|
|
|
|
|
|
|||||
N |
|
|
|
X |
|
O |
O ClO−4 |
|
|||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
19 |
|
|
||
|
R = H, 5,6-бензо, 7-Et2N; X = Me2N, Ar |
|
|
||||||||
3-(Индол-3-ил)кумарины получаются при взаимодействии ацилкумаринов 17 |
|||||||||||
с фенилгидразином [29]. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Избранные методы синтеза и модификации гетероциклов, том 2 |
521 |
||||||||||


имидазо[2,1-b]-1,3,4-тиадиазолы и 6-(кумарин-3-ил)-7Н-1,2,4-триазоло[3,4-b]-1,3,4-
тиадиазины соответственно [33].
3-Ацетилкумарин также использовался как исходное соединение для построения 3-гетарилкумаринов; его обработка дигидробромидом формамидиндисульфида и затем нейтрализация реакционной смеси приводила к 3-(2-аминотиазол- 4-ил)кумарину 24, а нагревание с фенилгидразином в присутствии ZnCl2 – к 3-(индол-2-ил)кумарину 25 [34] (схема 9).
Схема 9
|
|
|
NH |
2HBr |
|
|
|
H2N |
S |
|
|
|
|
|
|
S |
NH2 |
|
N |
NH2 |
|||
|
NH |
|
|||||
|
|
|
|
|
|||
|
|
|
|
R |
|
||
O |
|
|
|
|
|
S |
|
|
|
|
|
|
|
||
|
|
|
|
|
24 |
|
|
R |
|
|
|
|
|
|
|
PhNHNH2 |
|
|
|
|
|||
|
|
R |
|
|
|||
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
R = |
|
|
|
|
H |
25 |
|
|
|
|
O O |
|
|
|
|
|
|
|
|
|
|
|
3-(Тиазол-4-ил)кумарины из 3-ацетилкумарина получают при обработке последнего тиомочевиной в присутствии N-бромсукцинимида и бензоилпероксида; при взаимодействии с тиомочевиной и Br2 (катализaторы – комплексы LaIII и SmIII) [35, 36]; в результате нагревания на водяной бане с алкилтиомочевиной [33].
3-Ацетил-4,7-дигидроксикумарин по реакции Кляйзена с этилацетатом в присутствии этилата натрия дает 3-ацетоацетил-4,7-дигидроксикумарин, который под действием соответствующих реагентов превращается в различные 3-гетарил- кумарины [37] (схема 10).
|
|
|
H2N O2N |
|
|
|
Схема 10 |
|
|
|
NO2 |
|
O2N |
|
|
|
|
|
N |
R N |
|
||
|
|
|
H |
|
|
N |
NO2 |
|
|
|
|
|
|
||
|
|
|
|
|
|
26 |
|
O |
R |
O |
|
|
|
|
|
AcOEt |
NH2OH·HCl |
O |
27 |
|
|||
|
|
|
|||||
R |
EtONa |
|
|
|
N |
|
|
O |
|
|
|
|
|||
|
|
|
|
|
R |
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
NH2 |
|
N |
|
|
|
|
|
|
|
||
R = |
|
|
|
|
|
N |
R |
HO |
O |
O |
|
|
|
28 |
|
|
|
|
|
||||
Избранные методы синтеза и модификации гетероциклов, том 2 |
523 |
||||||

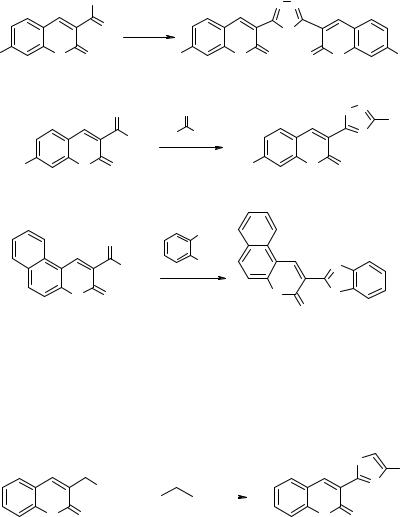
Важными синтонами для построения гетероциклического заместителя в положении 3 системы кумарина являются 3-карбоксикумарин 31 [10], хлорангидрид 32 [45], а также сложный эфир 33 − производное бензо[f]кумарина [46–48] (схема 13).
|
|
|
|
|
|
|
Схема 13 |
|
OH |
|
|
N N |
|
|
|
2 |
|
O N2H4·HCl |
|
O |
|
|
|
|
|
|
|
|
|
|
|
Et2N |
O O |
|
Et2N |
O |
O O |
O |
NEt2 |
|
31 |
|
|
|
[10] |
|
|
|
|
O |
NOH |
|
|
O |
N |
|
|
|
Ph NH2 |
|
|
|
Ph |
|
|
Cl |
|
|
|
N |
|
AlkO |
O |
O |
|
AlkO |
O |
O |
|
|
32 |
|
|
|
[45] |
|
|
|
|
O |
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OEt |
NH2 |
|
|
N |
|
|
O |
O |
ПФК |
|
O |
N |
|
|
|
|
|
|
O |
H |
|
|
33 |
|
|
|
|
|
|
|
|
|
[46−48] |
|
|
||
3-Тиокарбамоилкумарин использовался для синтеза 4-R-2-(кумарин-3-ил)тиа- золов 34 [4–6] (схема 14).
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Схема 14 |
|
|
S |
O |
|
|
|
S |
R' |
|||||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
R |
|
O Y |
NH2 + R' |
|
|
|
R |
|
O |
Y |
|||||
|
|
|
|
|
|
||||||||||
|
|
|
|||||||||||||
|
|
|
|
||||||||||||
|
|
|
|
Br |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
34 |
|
|
||
|
|
R = H, 7-OH, Alk, OAlk, 7-Et2N, 5,6-бензо; |
|
|
|
|
|
||||||||
|
|
R' = H, Alk, Ph, Bn, PhS, 4-PhC6H4, CO2R, CONH2; |
|
|
|||||||||||
|
|
Y = O, NH |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Избранные методы синтеза и модификации гетероциклов, том 2 |
|
525 |
|||||||||||||

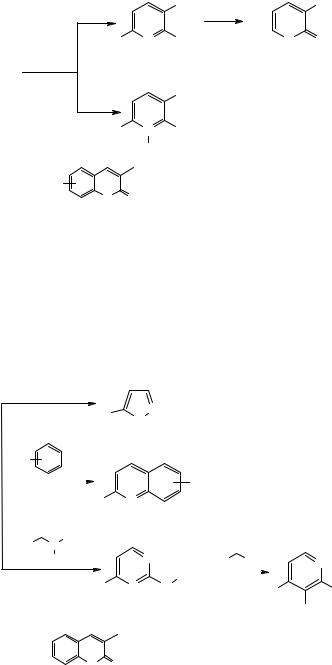


Схема 20
O
|
|
NH2 |
|
|
N |
|
|
|
|
R |
|
||
R" |
O |
N |
−NH3 |
X |
R" |
|
|
|
|
||||
|
|
XH |
|
|
|
|
HX |
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
R" |
|
|
|
|
|
O |
SO2NH2 |
O |
O |
|
|
R |
NH2 |
NH2 |
|
HN S |
|
|
|
|
|
|
|
|
|
|
O NH |
|
R |
N |
|
|
NH2 |
O |
|
|
O |
|
|
Y |
|
|
|
|
|
|
|
|
NH2 |
Ac2O |
|
O |
|
|
|
|
|
|
|
|
|
O |
N |
|
R |
N |
|
|
|
|
O |
|
||
|
Y |
|
|
|
|
|
|
|
|
|
|
|
|
|
R' |
|
AcOH |
HN |
|
|
R = |
|
|
R |
N |
|
|
|
O O |
|
|
|
||
R' = H, 5,6-бензо, 6-Br, 7-OH, 7-OMe, 7-Alk2N; R" = H, Cl;
X = NH, O, S; Y = CO2H, CONH2
N(1)-Бензоиламидразоны кумарин-3-карбоновых кислот 49 (получены реакцией 2-иминокумарин-3-карбоксамида с гидрохлоридом бензгидразида при кипячении в бутаноле вследствие рециклизации) циклизуются в кумаринилзамещенные триазолы 50, оксадиазолы 51 и тиадиазолы 52 [9] (схема 21).
Схема 21
|
|
|
ДМФА |
N N |
|
|
|
|
|
или p-хлортолуол |
|
||
|
|
|
|
|
||
|
|
|
R |
N |
Ph |
|
|
|
|
|
H |
|
|
NH2 |
|
|
50 |
|
||
R |
N |
|
AcOH |
N N |
|
|
|
R |
O |
Ph |
|||
HN |
Ph |
|||||
|
|
|||||
|
|
|
|
51 |
|
|
49 |
O |
|
P2S5 |
N N |
|
|
|
R = R' |
R |
S |
Ph |
||
|
|
52 |
|
|||
O O
R' = H, 6-OMe, 7-Alk2N
Избранные методы синтеза и модификации гетероциклов, том 2 |
529 |


 O O
O O