
Мальханов - Общая Физика
.pdf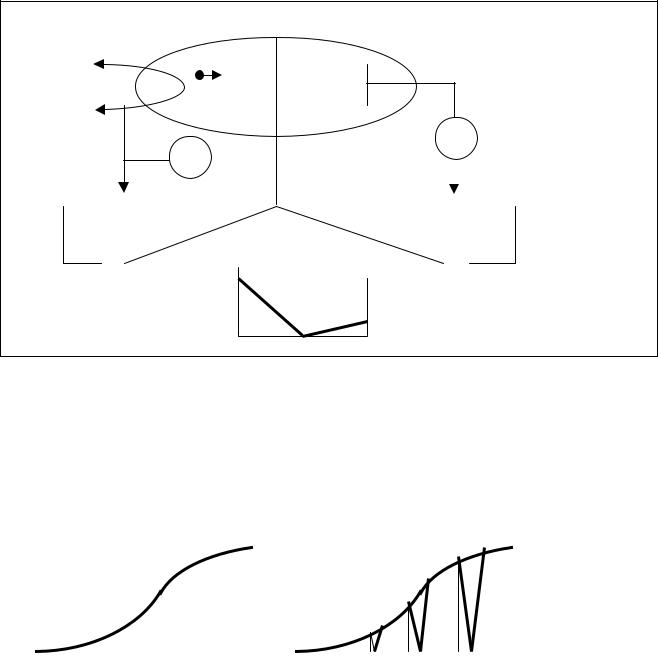
Если заполнить лампу парами какого-либо (парами ртути, например, как это было у Франка и Герца или аргоном). На гладкой кривой появятся провалы. Наличие провалов на вольтамперной характеристике, объясняется тем, что при энергиях, соответствующих минимумам происходит неупругое взаимодействие электронов с атомами, сопровождающееся возбуждением атомов. В этом случае электрон останавливается (в том и только в том случае, если он передает всю свою энергию атому без остатка) и ток в цепи резко падает. Заметим, что возбужденная ртуть при этом "светиться" в ультрафиолетовой области спектра λ = 253,7 нм . Сдвиг и наличие ширины у минимумов объясняются наличием проекций скоростей электронов (а следовательно и для энергий) на преимущественное направление от катода к аноду.
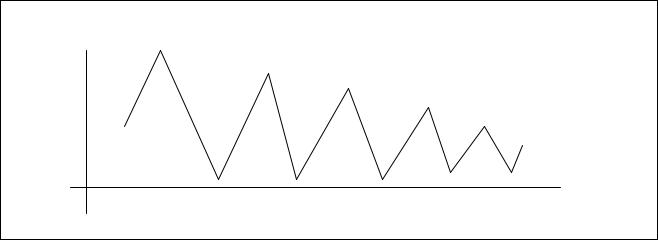
Понятно, что атомы с одним электроном на внешней оболочке ионизовать (то есть оторвать у них этот электрон) легче, чем, например у инертных газов, поэтому график зависимости потенциалов ионизации имеет характерный вид.
Потенциал
ионизации
He |
Ne |
Ar |
Xe Rn |
Li Na K Rb Cs
Атомный номер (число электронов у атома)
Таким образом опыт доказывает, что стационарные состояния обусловлены переходами электронов с одних орбит на другие.
( Различие потенциала ионизации и энергии возбуждения состоит в том, что в первом случае происходит полный отрыв электрона от атома, а во втором электроны внутри атома переходят на более удаленную орбиту).
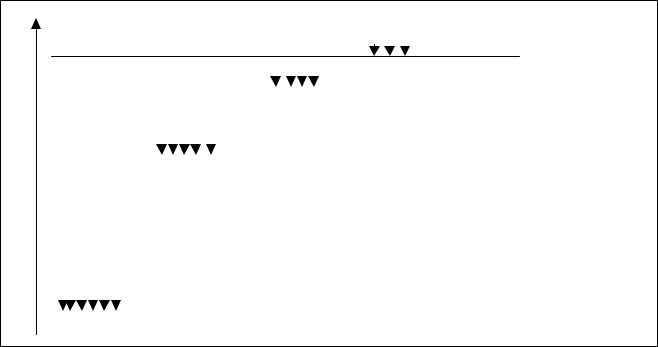
Тогда схематически энергетическую структуру атома можно представить в виде:
391
E |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
n=4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
k=4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
k=3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
и т.д. |
n=3 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
серия Пашена (ИК) |
|
|||||||||
|
|
|
|
|
|
|
k=2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
n=2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
серия Бальмера |
|
||||||||||||||||||||
|
|
|
|
|
|
|
(видимая) |
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
n=1 |
|
|
|
|
серия Лаймана (УФ) |
(основное состояние) |
||
На уровне основного состояния (n=1) электрона обладает минимальной потенциальной энергией по отношению к положительно заряженному ядру.
Иногда схему представляют в виде концентрических окружностей увеличивающегося радиуса, символизирующих орбиты электрона, между которыми осуществляются электронные переходы, чтобы подчеркнуть сферическую симметрию атома.
Можно резюмировать, что таким образом была получена феноменологическая теория, то есть теория логическим образом объясняющая явления, происходящие с объектами природы. В данном случае с атомами вещества, а следовательно и с веществом в целом. Квантовый характер природы – явление всеобщее, что доказывают опыты и к чему приводят логические умозаключения.
§ 3 Квантование по Бору
3.1 Квантование момента импульса
Согласно гипотезе Планка энергия квантуется
En = n ħ ω = n h ν.
392

Если рассматривать атом как гармонический осциллятор – систему, в которой совершается периодическое движение заряженных частиц, то его полную энергию можно выразить в виде
En = p2 /2m + m(ωq)2/2 = n ħ ω.
Здесь p – импульс, q – координата, ω - частота. Разделим равенство на правую часть.
p2 /2mnħω + mωq2/2nħ = 1.
В координатах p и q получили уравнение эллипса с полуосями
a2 = 2nħ/nω, b2 = 2mnħω
p
S = p dq
b
dq |
a |
q |
Отступление. Вычислим площадь эллипса как удвоенную площадь криволинейной трапеции.
a |
a |
x2/a2 + y2/b2 = 1 y2 = b2(1 – x2/a2), S = ∫ f(x) dx = 2 ∫ [b2(1 – |
|
-a |
-a |
a |
a |
- x2/a2)]1/2dx = 2b/a ∫ (a2 – x2)1/2 dx = b/a[x(a2 – x2)1/2 + a2 Sin – 1x/a]| = -a табличный интеграл -a
ba (Sin – 11 + Sin – 1(-1)) = 2ba Sin – 11 = π a b.
393

Вычислим площадь эллипса в обобщенных координатах p и q .
Sn = πab = 2π ħ n.
Получилось, что площадь такого эллипса квантуется, то есть прямо пропорциональна натуральному числу n . Чтобы распространить это правило на другие физические величины проведем вслед за Бором сравнение.
|
Обобщенные координаты (по- |
|
Угловые координаты (вращатель- |
|||||
|
ступательное движение) |
|
ное движение) |
|||||
|
p: (p = m dq/dt) – обобщенный |
|
M |
(M = r p) – момент импульса |
||||
|
импульс |
|
(M |
= mr2ϕ = Iϕ) |
||||
|
q |
– обобщенная координата |
|
ϕ |
- угловая координата |
|||
|
|
|
|
|
|
|
||
|
|
|
|
r |
|
– линейная координата |
||
|
|
|
|
p |
– обычный импульс (p = mrϕ) |
|||
Заметим, что площадь эллипса можно получить, если проинтегрировать по эллипсу как по замкнутому контуру (как это сделал Бор). Результат при этом будет тот же самый.
Sn = ∫ p dq = 2π ħ n.
Для электрона, движущегося по эллиптической орбите, в одном из фокусов которого находится ядро атома (или по окружности), сила, с которой ядро действует на электрон, является центральной. Следовательно, для этого электрона выполняется закон сохранения момента импульса, а M = cst, тогда
∫ p dq = ∫ M dϕ = M 2π 2π M = 2π ħ n M = n ħ n= 1,2,3,… .
То есть момент импульса квантуется. M = me v r = n ħ v = n ħ / me r (*)
394

 v
v
r
dϕ me
me
3.2 Боровский радиус и квантование внутренней энергии
Вычислим радиус, с которым электрон обращается вокруг атома, исходя из классических представлений и выражения (*) .
mv2/r = e2/4πε0r2 (nħ/m)2m/r = e2/4πε0 r = 4πε0 ħ2n2/e2m.
Вычислим радиус самой маленькой орбиты n = 1 (основное состояние) r1 = 5 10 – 11 м = 0,5 Å. Его называют Боровским радиусом и обычно при расчетах используют значение
r B = 0,529 Å.
Внутренняя энергия атома водорода складывается из кинетической и потенциальной энергии электрона. Последняя берется с отрицательным знаком, ее отсчет ведется таким образом, что на бесконечности она равна 0 .
E вн = E кин - E пот = mv2/2 - e2/4π ε0 r.
Преобразуем используя классические выражения для сил и Боровского радиуса с учетом его квантуемости.
mv2/r = e2/4πε0r2 mv2/2 = e2/8π ε0r, E вн = e2 /8πε0 rn - e2 /4π ε0 rn =
= - m e4 / 2 (4π ε0)2 ħ2 n2 = R*H (-1/n).
Пусть совершается переход из состояния с квантовым числом n в состояние с квантовым числом k
E k - En = R*H (1/n2 - 1/k2) = ħω = hν = hc/λ 395

k
n
k>n
1/λ = m e4 (1/n2 - 1/k2) / 2 (4πε0)2 2πc ħ3 = RH (1/n2 - 1/k2).
RH = 107 м– 1 = 10 5 см– 1 называют постоянной Ридберга.
Таким образом, замечательным является тот факт, что элементарная теория атома Бора приводит к той же формуле, что и экспериментально измеренные спектры. Численное значение постоянной Ридберга: R = 109678 см– 1.
§ 4 Волновое уравнение Шредингера
4.1 Электрон-волна
Для наглядного толкования "таинственного" правила квантования Бора – де Бройль ( Луи де Б., французский физик 1923-1924) предложил такой способ: на орбите электрона как волнового объекта укладывается целое число волн – n,
итакая электрон-волна, возвращаясь в исходную точку, будет иметь ту же фазу
иамплитуду, что и первоначально. Такая орбита и является стационарной орбитой в смысле Бора. С нее электрон не излучает, а волна обязана быть стоячей.
2πR / λ = n (*)
При этом де Бройлю пришлось предположить, что все частицы (из числа элементарных) обладают волновыми свойствами (сами являются волнами), а следовательно им можно приписать длину волны. Реализуем связь длины волны с импульсом частицы через волновое число.
p = E/c = hν / c = h/λ = ħk, 2πR/λ = k R = n.
Умножим обе части равенства k R = n на ħ
396
ħ k R = ħ n p R = ħ n M = ħ n.
Таким образом в этом месте смыкаются волновые и квантовые свойства и можно говорить о волнах-частицах.
Найдем длину волны электрона в этой модели и сравним ее с Боровским радиусом.
λe = h/p = h / mv ≥ 2 10 – 12 м = 0,02 Å, rB / λe = 0,53 / 0,02 26.
Боровский радиус в 26 раз больше, следовательно предположения вполне разумны, то есть длина волны электрона может укладываться в Боровский радиус много раз.
Если говорить об экспериментальном подтверждении волновых свойств электрона, то они мало принципиально отличаются от опытов по интерференции и дифракции света, хотя с другой стороны они чрезвычайно трудоемки технически, так как потребовали высокой степени точности и изобретательности. Отметим одно: размеры регулярных препятствий должны были составлять
~0,02 Å. Описание самих опытов мы опускаем. Характерные дифракционные картины для электронов экспериментально были получены К. Дж. Дэвиссоном и Дж. П. Томсоном в 1927-1928 годах.
Итак электрон можно описывать волной, то есть электрон подчиняется волновому уравнению. Свободный электрон можно описать с помощью решения уравнения плоской волны. Так как данное решение содержит косинус фазы, то обобщив косинус до экспоненты можно считать интенсивность такого волнового процесса пропорциональной этой экспоненте
~e i (kr - ωt).
Заметим, что для обозначения электрона-волны (и других частиц) используются термины: фазовые волны, либо – волны вещества, либо – волны де Бройля. Об электрон волне можно сказать, что это специальное волновое образование, соответствующее свободному равномерному движению частицы в определенном направлении с определенным импульсом
p = ħ k.
Однако, как правило, частицы не свободны, но находятся в условиях воздействия на них различных полей. Для начала разберем случай свободного электрона.
397

Здесь ħ так же как и С некая обобщенная координата (подобно использованной нами ранее ξ ), о физическом смысле которой необходимо в дальнейшем поговорить.
Разделив время и координату способом
ψ (r, t) = ϕ (r) e - iωt.
Получим стационарное (не зависящее от времени) уравнение Шредингера
iħ ( - iω) ϕ(r) = ( - ħ2 2/2m + U(r)) ϕ (r) (ε = ħω)
ε ϕ (r) = ( - ħ2 2/2m + U (r)).
Таким образом, имеем уравнение Шредингера для электрона в зависимости от времени и координат, учитывающее корпускулярно-волновой дуализм электрона и с учетом внешнего потенциального силового поля произвольного вида
- ħ2 2ψ/2m + U(r)ψ = iħ ∂ψ/∂t.
Если отбросить зависимость от времени у ψ - функции относительно которого записано уравнение – получится стационарное уравнение Шредингера
- ħ2 2ϕ/2m + U(r)ϕ = εϕ.
4.3 Конструирование уравнения Шредингера способом Энрико Ферми
Заметим, что электрон (или вообще частицу с корпускулярно-волновыми свойствами) часто представляют в виде волнового пакета.
|
2 |
2 |
|
|
|
|
|
|
|
|
|
cos( λ |
1.5 ) .cos( 40 λ) |
0 |
1 |
2 |
3 |
|
|
||||
|
2 |
2 |
|
|
|
|
|
0 |
|
λ |
3 |
|
|
модель волнового пакета |
|
||
399


