
методичка по Химии
.pdfНа практике после заряда ЭДС у НКА может достигать 1,34В и у НЖА – 1,48В; через некоторое время эти значения снижаются: у НКА до 1,3-1,33В, у НЖА - до 1,32-1,35В. Разряжаются они до 1В, заряд ведется 1,2−кратным количеством электричества для НКА и 1,5 – для НЖА их емкости (ток заряда ≈ 10% от емкости). При этом наблюдается выделение Н2 и О2. Из-за малого перенапряжения на железе заряд НЖА с самого начала сопровождается выделением водорода. Выделение же водорода на кадмиевом электроде наблюдается к концу заряда, из-за большого перенапряжения.
По основным характеристикам НК и НЖ аккумуляторы практически не отличаются. НЖ аккумуляторы дешевле, но обладают высоким саморазрядом. Оба щелочных аккумулятора, в сравнении со свинцовым, характеризуются высокой механической прочностью, устойчивостью к вибрациям, большим сроком службы, простотой в обслуживании (не боятся перезаряда, коротких замыканий, хранения в разряженном состоянии). НЖ аккумуляторы применяются в пассажирских вагонах, локомотивах, электрокарах, погрузчиках. НК аккумуляторы наряду с перечисленным, широко используются в различной переносной аппаратуре: связи, радио, телефонах, видео и другой электронной технике.
1.3. Основные электрохимические характеристики аккумуляторов
1.3.1. Электродвижущая сила
ЭДС аккумулятора (Е) - это разность его электродных потенциалов в отсутствии внешнего тока, что соответствует напряжению разомкнутой цепи
(Uр.ц.):
E = Uр.ц. = Е(+) – Е(–) , |
(1) |
где Е(+) и Е(–) – равновесные потенциалы электродов, В. Электродные потенциалы измеряют при помощи вспомогательного электрода сравнения, например, хлорсеребряного (Ехс = 0,2В) и катодного вольтметра с большим внутренним сопротивлением (более 106 Ом).
При прочих равных условиях при работе ХИТ предпочтительней источник тока с большей ЭДС. Для водных растворов ЭДС свинцового аккумулятора 2,1В одно из наиболее высоких. У щелочных ЭДС существенно мень-
ше – 1,3В.
1.3.2. Разрядное напряжение, поляризация и внутреннее сопротивление
Разрядное напряжение (Uр) – это напряжение на клеммах аккумулятора при токе разряда I. Оно соответствует разности потенциалов между электродами под током (ЕI )
Uр = ЕI(+) – ЕI(−) = Uр.ц. − Е(+) − Е(−) − IRвн. , |
(2) |
80
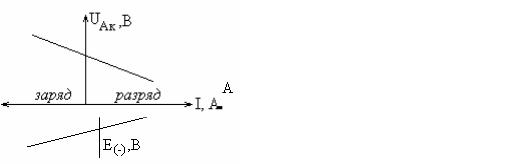
где − Е(+), Е(−) − поляризация соответствующего электрода, В; Rвн. − внутреннее сопротивление аккумулятора (сумма сопротивлений электролита и электродов), Ом.
Поляризация – это отклонение потенциалов электродов от их равновесных значений:
Е(+) = Е(+) − ЕI(+) |
(3) |
Е(−) = ЕI(−) −Е(−) |
(4) |
Е(+) и Е(−) – равновесные потенциалы (при I = 0).
Увеличение Uр, а следовательно, и разрядного тока достигается за счет уменьшения Е (создаются условия, при которых скорость электродных реакций протекает быстро) и уменьшения Rвн. (за счет применения электролитов с высокой электропроводностью и конструктивных особенностей аккумулятора).
Свинцовый аккумулятор характеризуется очень низким Rвн. (менее 0,01 Ом), т.е. более высокими разрядными токами, чем щелочной.
Зависимость между Uр и I называется вольтамперной характеристикой, а зависимость между ЕI и I – поляризационной диаграммой. Это важнейшие характеристики источника тока (рис. 1, 2).
|
|
|
|
|
|
|
|
|
|
Рис. 2 Вольтамперная характери- |
|
Рис. 1 Поляризационная диаграмма |
|||
аккумулятора |
стика аккумулятора |
||
1.3.3. Емкость
Емкость – это количество электричества, которое источник тока может отдать при разряде до конечного напряжения
Q = I · τ , |
(5) |
где Q - емкость, А·ч; I – разрядный ток (I = const), А; τ - продолжительность разряда, ч.
81
Емкость определяют по кривым разряда (зависимость между Uр и τ при I = const). Q зависит от массы активных веществ (по закону Фарадея), а также от конструкции, температуры (с уменьшением температуры Q снижается), тока разряда. На определенный период эксплуатации емкость аккумулятора гарантируется изготовителем и входит в обозначение источника тока. Например, для щелочных КН-100 (100 А·ч), для кислотных СТ-54 (54 А·ч).
Эффективность зарядно-разрядного цикла оценивается коэффициентом отдачи по емкости (%)
КQ = |
Qp |
100%, |
(6) |
|
|||
|
Qз |
|
|
где Qp – емкость, отданная при разряде, Qз - емкость, сообщенная аккумулятору при заряде. При заряде, часть тока всегда теряется на побочное газовыделение, что снижает Кq . У свинцовых аккумуляторов отдача по емкости составляет до 85%, а у щелочных – до 69%.
1.3.4. Энергия и мощность
Энергией аккумулятора называется количество энергии, которое при разряде передается во внешнюю цепь
W = Q · Uср, |
(7) |
где W – энергия, Вт·ч; Uср – среднее напряжение разряда, В.
Для сравнительной энергоемкости различных аккумуляторов служит
величина удельной энергии (Вт·ч/кг) |
|
Wуд = W/m, |
(8) |
где m – масса аккумулятора, кг. У свинцовых аккумуляторов Wуд составляет до 40 Вт·ч/кг, у щелочных она больше.
Мощность аккумулятора – это количество энергии, отдаваемое в еди-
ницу времени (ВТ) |
|
Р = W/τ = Iср· Uср. |
(9) |
1.3.5. Саморазряд
Саморазряд – уменьшение емкости источника тока при хранении с разомкнутой цепью. Выражается в % от емкости в сутки или месяц.
Наибольший саморазряд у НЖ аккумуляторов 30-40% в месяц. Причина в том, что порошкообразное железо отрицательного электрода заметно реагирует с водой с выделением водорода (в отличие от кадмия). У НК и свинцового аккумуляторов саморазряд невелик и составляет 3-5% в месяц. Саморазряд увеличивается при повышении температуры и при использовании загрязненных электролитов.
82
1.3.6. Срок службы
Продолжительность использования аккумулятора определяется числом циклов заряда и разряда, а также условиями эксплуатации. У старторных свинцовых аккумуляторов он самый низкий – до 4 лет (250-300 циклов); у тяговых до 6 лет (300-400 циклов). Щелочные аккумуляторы служат 10 и более лет (свыше 1000 циклов). Признаком негодности аккумулятора считается снижение емкости до 40%.
ПРАКТИЧЕСКАЯ ЧАСТЬ
2.1. Подготовка к измерениям
Для определения характеристик аккумуляторов подготовьте установку. Она включает: нагрузочное переменное сопротивление (реостат), вольтметр (для измерения Uр.ц., Uр и Uз), амперметр, выпрямитель и 3 тумблера (1-й - для переключения режимов заряд-разряд, 2-й - для измерения потенциалов положительного или отрицательного электрода, 3-й - для размыкания внешней цепи).
К установке необходимо подключить аккумулятор, катодный вольтметр (для измерения потенциалов электродов) и хлорсеребряный электрод сравнения, предварительно опущенный в электролит аккумулятора.
2.2. Измерение ЭДС и равновесных потенциалов
Измерения производят при разомкнутой внешней цепи (3-й тумблер в положении – выкл.). Значение эдс (Uр.ц.) считывают на вольтметре, встроенном в установку. Вольтметром с высоким входным сопротивленим измеряют напряжение между электродами аккумулятора и хлорсеребряным (ХС) электродом сравнения (при положении 2-го тумблера «-» для отрицательного
электрода – UPb/хс, при «+» для положительного электрода – UPbO2/хс ). Затем вычисляют равновесные потенциалы:
Е(–)= 0,2 − UPb/хс |
(10) |
Е(+) = 0,2 + UPbO2/хс |
(11) |
где 0,2 – потенциал хлорсеребряного электрода, В.
Используя данные раздела 1.2 и 1.3, можно оценить, в каком исходном состоянии находится аккумулятор: в заряженном или разряженном. Для чего сравнить измеренное значение ЭДС с теоретическим (для свинцового аккумулятора в разряженном состоянии Uр.ц. < 2В, для НЖ и НК < 1,3В). Исходя из этого, дальнейшие измерения начинать с режима разряда или заряда.
83

2.3. Снятие вольтамперной характеристики и поляризационной диаграммы
2.3.1. Разряд аккумулятора
При разряде (1-й тумблер в положении разряд, 3-й – вкл.) увеличивают реостатом силу тока через определенные интервалы (0,1-0,3 А). При каждом значении силы тока измеряют разрядное напряжение аккумулятора (Uр) и потенциалы электродов под током (ЕI). Разряд проводить у свинцового аккумулятора до Uр = 1,8 – 1,85В, а для щелочных до Uр = 0,9 – 1,0В. Результаты опыта сводятся в табл. 1.
|
|
Результаты измерений при разряде |
Таблица 1 |
||||||
|
|
|
|
|
|||||
|
|
|
|
|
Положительный электрод |
|
|||
I, А |
Uр, В |
Отрицательный электрод |
|
||||||
UPb/хс, В |
ЕI(−), В |
Е(−), В |
UPbO2/хс, В |
ЕI(+), В |
|
Е(+), В |
|
||
|
|
|
|
|
|
|
|
|
|
Е(−) и Е(+) – поляризация электродов (рассчитывается по формулам 3 и 4.).
По данным табл. 1 построить два графика: вольтамперную характеристику (зависимость U от I) и поляризационные диаграммы (зависимость Е от I).
Из графических данных найти для исследуемого аккумулятора:
1)область рабочих разрядных токов (разрядные токи могут достигать и больших значений в режиме короткого замыкания, но при этом резко снижается UP);
2)как изменяется поляризация отрицательного и положительного электродов с ростом I?
3)какой из электродов лимитирует (больше поляризуется) работу аккумулятора, т.е. в итоге ограничивает емкость источника тока?
4)рассчитать Rвн (формула 2) для нескольких значений I и усреднить.
2.3.2. Заряд аккумулятора
Снятие зарядных кривых провести при тех же значениях силы тока, как при разряде (предварительно включить выпрямитель и 1-й тумблер в положение - заряд). Результаты занести в табл. 2, аналогичную табл. 1 (при этом величину UP заменить на Uз ) и построить поляризационную диаграмму. Сделать вывод, какой из электродов больше поляризуется при заряде. Составить электрохимические побочные реакции газовыделения на положительном и отрицательном электродах.
84

2.4. Определение емкости
Перед измерением емкости аккумулятора следует иметь ввиду, что данный опыт довольно продолжительный по времени (30-60 минут на лабораторном аккумуляторе и несколько часов на промышленных). Причем аккумулятор предварительно должен быть полностью заряжен: 1,1 кратным количеством электричества от емкости для кислотного и 1,2 - 1,5 - кратным количеством для щелочных. Поэтому, по согласованию с преподавателем, исследуемый аккумулятор или сначала подзаряжают или сразу после опыта 2.3.2 проводят разряд при постоянной силе тока.
Сила разрядного тока в амперах составляет обычно 10% от емкости (как и сила зарядного тока). Можно проводить разряд и повышенными токами (для сокращения времени разряда), но при этом можно занизить фактическую емкость источника тока.
В начале опыта включить аккумулятор в режим разряда, установив разрядную силу тока. В ходе опыта силу тока поддерживать постоянной реостатом и записывать через каждые 10-15 минут величину UP. в табл. 3.
Таблица 3
Результаты определения емкости
Время разряда (τ), ч |
UP, В |
|
|
Разряд закончить при падении напряжения на свинцовом аккумуляторе до 1,8 – 1,85В и на щелочных до 0,9 – 1,0В, построить график разрядной кривой (зависимость UP от τ).
Рассчитать емкость по формуле (5). Если на опытном аккумуляторе присутствует маркировка, то рассчитать величину снижения емкости от номинальной. Сделать вывод о целесообразности дальнейшего использования данного аккумулятора.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Какие электрохимические процессы протекают на отрицательном и положительном электродах свинцового и никель-кадмиевого аккумулятора: а) при разряде; б) заряде? В каком случае электроды служат катодом и в каком анодом?
2. Как измерить равновесный потенциал электродов? Почему он отличается от токового значения потенциала?
3. Какой вид имеет принципиальная электрическая схема при заряде и разряде аккумулятора?
4. Какие основные применения у свинцового аккумулятора и почему? Какие аккумуляторы целесообразней использовать в пассажирских вагонах?
85
5. Какие аккумуляторы не боятся хранения в разряженном состоянии, перезарядки, вибрации и почему?
ЛИТЕРАТУРА
1.Зубрев Н.И. Инженерная химия на железнодорожном транспор-
те. – М.: УМК МПС РФ, 1990. – 291 с.
2.Варапаев Н.В., Дасоян М.А., Никольский В.А. Химические источники тока. – М.: Высшая школа. 1990. – 240 с.
86
ЛАБОРАТОРНАЯ РАБОТА № 33В
ИЗГОТОВЛЕНИЕ ТЕКСТОЛИТА И ГЕТИНАКСА МЕТОДОМ ПРЕССОВАНИЯ
Тема: методы получения деталей из сложных пластмасс.
Цель работы: ознакомление с методом получения листового текстолита и гетинакса.
СВЕДЕНИЯ ИЗ ТЕОРИИ
Пластмассами называют материалы, изготовляемые на основе органических высокомолекулярных веществ. Эти материалы способны формоваться при определенных условиях вследствие их пластичности. Пластмассы при обычных условиях являются твердыми веществами.
Высокомолекулярные вещества, используемые для получения пластмасс, часто называют смолами или полимерами.
Простые пластмассы состоят только из полимера, например, полиэтилен, полипропилен и др. Но чаще состав пластмасс бывает более сложный. В них входят: связующее вещество – смола, составляющая основу пластмассы; наполнители – древесная мука, ткань, асбест и т.п., повышающие механическую прочность пластмассы; пластификаторы – органические малолетучие жидкости (например, некоторые высококипящие сложные эфиры), придающие материалу большую пластичность и устраняющие его хрупкость; красители, сообщающие материалу требуемую окраску и другие вещества. Примером таких сложных пластмасс являются фенолформальдегидные пластмассы.
По отношению к нагреванию смолы делятся на две группы: термопластичные и термореактивные.
Термопластичные смолы при нагревании размягчаются, становятся пластичными. При охлаждении они снова затвердевают, сохраняя при этом прежние свойства. Такие смолы можно использовать при производстве изделий неоднократно путем нагревания до пластического состояния, последующего формования и охлаждения. К термопластичным смолам относятся полимеры с линейной структурой молекул, например, полиэтилен, полихлорвинил, другие полимеризационные смолы. Их линейные цепи из атомов углерода не связаны химически. Поэтому при нагреве молекулы приобретают возможность относительного перемещения, пластмассы становятся пластичными.
Термореактивные смолы при нагревании утрачивают пластичность, они становятся неплавкими и нерастворимыми. Это объясняется тем, что при нагревании происходит химическая реакция образования пространственной
87
структуры из линейных молекул. К термореактивным смолам относится, например, фенолформальдегидная резольная смола.
Термопластичные материалы часто перерабатываются в изделия способом литья под давлением и путем непрерывного выдавливания материала через отверстия соответствующего профиля (метод экструзии).
Термореактивные материалы перерабатываются преимущественно способом горячего прессования.
Сущность литья под давлением состоит в следующем. В цилиндр литьевой машины поступает из бункера необходимое количество пластмассы в виде порошка или зерен. Так как цилиндр обогревается, то пластмасса размягчается и под давлением плунжера поступает через отверстие в охлаждаемую пресс-форму. В пресс-форме изделие быстро затвердевает и при обратном ходе плунжера, когда происходит разъединение пресс-формы, автоматически выталкивается из нее; затем цикл литья под давлением начинается снова. Длительность одного цикла всего 20-30 сек; за один цикл может быть отлито несколько изделий по числу гнезд в форме. Поэтому производительность литьевых машин очень высокая.
При переработке по методу экструзии твердый полимер непрерывно подается шнеком через участки высоких температур и давлений, где он плавится и превращается в компактную массу, а затем материал выдавливается, образуя требуемое изделие.
Методом экструзии могут быть изготовлены самые разнообразные изделия: трубы и шланги, листы, имеющие ширину свыше 1 м и толщину более 6 мм, пленки такой же ширины, но меньшей толщины – вплоть до нескольких сотых долей миллиметра.
При горячем прессовании в нижнюю половину формы (матрицы), закрепленную на нижней плите пресса, загружается определенное количество пластмассы. Чтобы обеспечить заполнение формы, в нее загружают пластмассу с небольшим избытком. Этот избыток выдавливается через зазор между плитами формы в виде тонкой, легко удаляемой пленки. После этого опускается вторая половина пресс-формы (пуансон) и создается сильное давление на формуемый материал. Пресс-форма одновременно нагревается электрическим током (рис. 2 , с. 86).
Под влиянием нагрева и давления пластмасса хорошо заполняет форму и переходит постепенно в твердое неплавкое состояние. После этого плунжер пресса поднимают, извлекают готовое изделие и форму загружают новой порцией материала.
Если прессуют изделие из термопластичного полимера, то после окончания процесса форму охлаждают, давление снимают, из формы извлекают изделие.
Если полимер термореактивен, то форму можно не охлаждать, т.к. вследствие происшедшего структурования изделие из полимера уже не может течь или изменять полученную конфигурацию.
88
Метод горячего прессования уступает по производительности литью под давлением, т.к. требуется выдерживать изделие в пресс-форме до тех пор, пока оно не затвердеет.
Фенолформальдегидные пластмассы
Фенолформальдегидные пластмассы производятся промышленностью в наибольшем количестве. Основу их составляет фенолформальдегидная смола. Это высокомолекулярное вещество получается реакцией поликонденсации фенола с формальдегидом. Реакция идет при нагревании смеси в присутствии катализатора-кислоты или щелочи. В зависимости от условий реакции поликонденсации можно получить три типа смол: новолачные, резольные, резиты.
В бензольном кольце атомы углерода нумеруются по часовой стрелке, начиная с того, у которого есть заместители вместо атомов водорода.
Положение 2, 6 называется орто-положением, 4 – пара и 5, 3 – метаположением. Атомы водорода в орто и пара-положении подвижны и вступают в реакцию поликонденсации.
Новолачные смолы получают при следующих условиях: берется избыток фенола и кислый катализатор. Реакция протекает ступенчато.
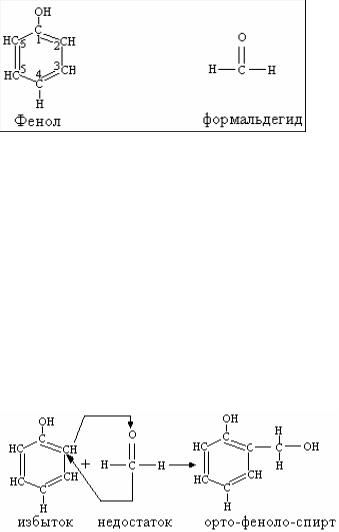
При первой ступени происходит присоединение молекул формальдегида к молекулам фенола преимущественно по орто-положению. При этом атом водорода из орто-положения переходит к атому кислорода формальдегида. Его двойная связь (С=О) разрывается и освободившейся связью атом углерода присоединяется по орто-положению к бензольному кольцу. В результате первой ступени присоединения образуются орто-феноло-спирты
1)
По второй ступени происходит конденсация молекул орто-феноло- спиртов. Спиртовая гидроксо-группа соединяется с атомом водорода по орто-
89
