
- •Тема 1: химия как наука и её значение в жизни человека
- •Тема 2: периодический закон и периодическая система химических элементов д.И. Менделеева
- •Большие и малые периоды
- •Тема 3: строение атома. Ядерные превращения
- •Тема 4: строение электронной оболочки атомов
- •Тема 5: периодическое изменение свойств химических элементов
- •Оэо по Полингу
- •Тема 6: химическая связь и строение молекул (I часть)
- •Энергии (Есв) и длины (св) галогеноводородных соединений
- •Заключение по материалу «Химическая связь и строение молекул»
- •Тема 8: межмолекулярное взаимодействие
- •Тема 9: основные закономерности протекания химических процессов
- •Тема 10: направленность химических реакций
- •Тема 12: электрохимические процессы
- •Тема 13: электролиз
- •Основные понятие и особенности электролиза.
- •Отдельные примеры электролиза растворов и расплавов солей.
- •Применение электролиза
- •Закон Фарадея. Решение задач.
- •Тема 14: химия металлов и электротехнические материалы Металлическое состояние вещества
- •Тема 14: химия металлов и электротехнические материалы Физические свойства металлов
- •Тема 14: химия металлов и электротехнические материалы химические свойства металлов
- •Взаимодействие металлов с кислотами
- •Действие хлороводородной кислоты на металлы
- •Действие серной кислоты на металлы
- •Действие азотной кислоты на металлы
- •Действие щелочей на металлы
- •Действие серной кислоты на металлы
- •Действие азотной кислоты на металлы
- •Действие щелочей на металлы
- •Тема 14: химия металлов и электротехнические материалы способы получения металлов
- •Получение металлов
- •Тема 14: химия металлов и электротехнические материалы зонная теория внутреннего строения металлов
- •I. Теория электронного газа.
- •II. Зонная теория кристаллов.
- •Выводы:
- •Тема 14: химия металлов и электротехнические материалы электротехнические материалы.
- •Сверхпроводники
Тема 14: химия металлов и электротехнические материалы зонная теория внутреннего строения металлов
Электропроводимость объясняется двумя теориями металлического состояния.
I. Теория электронного газа.
Основные положения теории:
1. В
узлах кристаллической решетки находится
ионы, образующие плотную упаковку и
окруженные электронами: Ag ![]()
![]() Ag+ + ē
Ag+ + ē
2. Электроны в металле не закреплены за отдельными атомами, а свободно перемещаются по всему объему металла, образуя «электронный газ».
3. Все электроны «электронного газа» являются переносчиками тепла и электричества.
II. Зонная теория кристаллов.
Эта теория объясняет электропроводимость на основе квантовой теории строения кристаллических тел. Химическая связь в металле описывается с позиции ММО. В процессе образования кристалла происходит перекрывание внешних электронных облаков атомов по аналогии с образованием химической связи в молекулах. Согласно ММО при сближении двух атомных электронных орбиталей идет расщепление энергии АО на орбиталь с более высоким уровнем энергии (МО – разрыхляющая) и орбиталь с более низким уровнем энергии (МО – связывающая). При последовательном увеличение числа взаимодействующих атомов увеличивается число МО. Если в кристалле число атомов будет равно N = 1023 , то из МО будет образована целая энергетическая зона, у которой разность между энергиями соседних орбиталей будет ничтожно мала.
Например: В кристалле натрия разность энергий двух соседних орбиталей равна 10-28 кДж. Таким образом, образуется почти сплошная энергетическая зона.
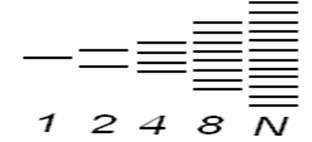
Выводы:
1. Энергетическая зона состоит из очень близко расположенных МО. Она создается за счет орбиталей внешнего энергетического уровня и заполняется электронами этого уровня.
2. Разность энергии самой «нижней» и самой «высокой» МО равна ∆Е/N (N = 6,02 ∙ 1023), т.е. она очень мала и электроны легко переходят с одной МО на другую МО (при затрате минимальной энергии). Электроны двигаясь в объеме металла, являются переносчиками электричества и тепла.
3. Заполнение МО идет в порядке возрастания энергии и в соответствии с принципом Паули – на каждой МО размещается по два электрона с ↑↓.
Тема 14: химия металлов и электротехнические материалы электротехнические материалы.
По электрическим свойствам материалы делятся на проводники, диэлектрики, полупроводники и сверхпроводники. Они отличаются друг от друга по механизму проводимости, по величине удельного сопротивления и другими свойствами.
Зонная структура металла (проводника).
Совокупность уровней занятых валентными электронами называются валентной зонной. Уровни, оставшиеся незаполненными, составляют зонупроводимости в металлах. Эти зоны в металле перекрываются. Электроны с валентной зоны, под действием приложенной разности напряжений переходят в зону проводимости и обуславливает электропроводимость металла.
Например, у натрия перекрываются 3s и 3р орбитали (3s1 – валентная зона, занята на 1/2 валентными электронами, 3р – зона проводимости пустая).
Зонная структура диэлектрика (изоляторы). В отличие от металлов кристаллы неметаллов обычно не обладают электропроводностью. Они представляют собой диэлектрики (изоляторы). В этих кристаллах между энергетическими зонами – валентной и зоной проводимости возникает область запрещенных энергий, называемая запрещенной зоной с энергетическим промежутком ∆Е > 4эВ. Энергия электрического поля или теплового движения оказывается недостаточной для преодоления этого энергетического промежутка и электрон не переходит из валентной зоны в зону проводимости, т.е. электроны не могут свободно передвигаться по кристаллу и служить переносчиками электрического тока.
Например,
∆Еалмаза = 5,4эВ, ∆Екварца = 5,2эВ.
Зонная структура полупроводника.
Если ширина запрещенной зоны относительно невелика (в приделах 0,1-4эВ), то при сообщении твердому телу определенного количества энергии (тепло, освещение, облучение, усиление тока), часть его электронов может перейти из полностью заполненной валентной зоны в зону проводимости и принять участие в переносе тока. Такие вещества называются полупроводниками. Например, у собственных полупроводников Ge ∆Е = 0,75эВ, Si ∆Е = 1,21эВ (собственные полупроводники – проводимость обусловлена ионизацией атомов чистого вещества). Особенность собственных полупроводников состоит в том, что при переходе части электронов в зону проводимости в валентной зоне проявляется эквивалентная количество положительных ионов или «дырок», которые так же участвуют в переносе тока. То есть проводимость в полупроводниках может осуществляться как электронами зоны проводимости (n – проводимость), так и «дырками» валентной зоны (р – проводимость). Электроны движутся в зоне проводимости, как это происходит в металле, а «дырки» движутся в валентной зоне (от + к -) в направлении противоположном движению электронов, т.е. собственные полупроводники имеют электронно-дырочную проводимость.
|
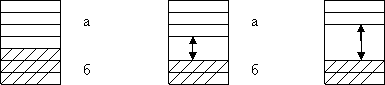
Схема расположения энергетических зон в проводнике, полупроводнике, изоляторе.
а – зона проводимости; б – валентная зона.
Наряду с собственными полупроводниками большое значение имеют также полупроводники примесного типа. В них основное количество переносчиков тока – электронов или дырок – поставляют введенные в собственные полупроводники специальные добавки (примеси), энергетические уровни которых располагаются между валентной зоной и зоной проводимости полупроводника.
В примесных полупроводниках путем соответствующего подбора добавок можно искусственно создать электронный или дырчатый механизм проводимости. В соответствии с этим добавки подразделяются на две категории: электронно-донорные и электронно-акцепторные.
Полупроводники с донорной примесью обладают электронной n – проводимостью, т.к. примеси дают электроны в зону проводимости (примеси – доноры электронов). Например, добавка к Ge…….4s24p2 (IVгр) атомов Р, As, Sb (из V группы) с электронной конфигурацией наружного уровня …..s2 p3 (имеет на наружном уровне на один электрон больше) будет являться донором электронов. Так из пяти электронов наружного уровня – четыре электрона идут на связь с соседними атомами в кристаллической решетке Ge, а пятый электрон становится как бы лишнем, т.к. оказывается вне сферы действия ковалентных связей. Достаточно лишь незначительная затрата энергии (порядка 0,01эВ), чтобы этот электрон перешел из валентной зоны в зону проводимости.
Акцепторные примеси сообщают полупроводнику дырочную проводимость. Например, к тому же Ge…4s24p2 (полупроводник) добавляют атомы элементов III группы Al, Ga, Zn с электронной наружной конфигурацией ….. s2 p1 , т.е на наружном уровне на один электрон меньше. Примеси на наружном уровне имеют три валентные электрона и входя в состав кристаллической решетки Ge, атомы этих примесей стремятся захватить недостающий ему четвертый электрон у соседнего атома Ge , у которого возникает на этом месте «дырка» (электрон переходит на уровни зоны примесей), т.е. полупроводник имеет р - проводимость.
Из изложенного можно сделать вывод: донорными являются все примеси, атомы которых содержат больше валентных электронов, чем атомы основного вещества, а акцепторными – это примеси, атомы которых содержат меньше валентных электронов, чем атомы основного вещества.
Чтоб представить себе размер добавок, необходимых для изготовления полупроводника приведем пример: если на 100 млн. атомов Ge ввести 1 атом As, то Ge приобретет характер n- проводника. Введение такого же количества атомов В переводит Ge в полупроводник р- типа, в весовых соотношениях это составляет: на 700m Ge – 1г В (бора).
