
pg_met_pr2
.pdfМіністерство освіти і науки України Сумський державний університет
МЕТОДИЧНІ ВКАЗІВКИ до практичних занять та самостійної роботи
з дисципліни “Загальна фізика”
для студентів напрямів підготовки 0908 „Електроніка”, 0914 „Комп’ютеризовані системи, автоматика і управління”, 0906 „Електротехніка” усіх форм навчання
ЧАСТИНА 2
“Молекулярна фізика та термодинаміка”
Суми Вид-во СумДУ
2008
Методичні вказівки до практичних занять та самостійної роботи з дисципліни “Загальна фізика” /Укладачі: О.В.Лисенко, М.Ю.Ромбовський. — Суми: Вид-во СумДУ, 2008. – 94 с.
Кафедра теоретичної фізики
|
ЗМІСТ |
|
|
|
С. |
ВСТУП........................................................................................... |
4 |
|
ТЕМА 1 РІВНЯННЯ ГАЗУ. ПРОЦЕСИ....................................... |
5 |
|
1.1 |
Приклади розв’язання задач............................................... |
5 |
1.2 |
Задачі для самостійного розв’язання ............................... |
21 |
ТЕМА 2 ПЕРШИЙ ЗАКОН ТЕРМОДИНАМІКИ. |
|
|
ТЕПЛОЄМНІСТЬ........................................................................ |
28 |
|
2.1 |
Приклади розв’язання задач............................................. |
28 |
2.2 |
Задачі для самостійного розв’язання ............................... |
48 |
ТЕМА 3 ДРУГИЙ ЗАКОН ТЕРМОДИНАМІКИ. |
|
|
ЕНТРОПІЯ................................................................................... |
57 |
|
3.1 |
Приклади розв’язання задач............................................. |
57 |
3.2 |
Задачі для самостійного розв’язання ............................... |
76 |
ВІДПОВІДІ ДО ЗАДАЧ ДЛЯ САМОСТІЙНОГО |
|
|
РОЗВ’ЯЗАННЯ............................................................................ |
84 |
|
СПИСОК ЛІТЕРАТУРИ ............................................................. |
93 |
|
3
ВСТУП
У цих методичних вказівках наведені приклади розв’язання найбільш типових задач із розділу “Молекулярна фізика та термодинаміка”, а також подані задачі для самостійного розв’язання. Автори мають на меті сформувати у студентів методологію розв’язання задач, допомогти засвоїти фізичні закони, навчити деяких математичних прийомів, що широко використовуються у фізиці. При роботі над кожною темою варто дотримуватися таких рекомендацій:
1Детально опрацювати теоретичний матеріал за підручником з курсу загальної фізики (наприклад, [1-2]).
2Уважно вивчити приклади розв’язання розібраних задач з даної теми. З’ясувати всі не зрозумілі для себе моменти у розв’язанні задачі, записати розв’язки в зошит. За необхідності ще раз звернутися до підручника для більш глибокого опрацювання теоретичного матеріалу або ж звернутися за консультацією до викладача. Пам’ятайте, необхідно домогтися повного розуміння розв’язання наведених задач. Перехід до самостійного розв’язання задач варто проводити тільки після повного розуміння прикладів поданих у даній темі.
3Перейти до самостійного розв’язання задач даної теми. При
цьому варто керуватися загальною |
методологією |
|
розв’язання, |
що подана в розібраних задачах, а саме: |
|
а) зробити |
рисунок до задачі, якщо |
це необхідно; |
б) з’ясувати сутність процесів, про які йдеться мова в задачі; в) установити закони, які слід використати для розв’язання задачі, записати відповідні рівняння; г) провести математичні перетворення, отримати розв’язок у загальному вигляді, шукана величина повинна бути виражена через величини, що наведені в умові задачі; д) виконати аналіз отриманого розв’язку щодо його відповідності фізичному змісту.
Пам’ятайте! Щоб зрозуміти, як розв’язується задача, від вас потрібні серйозні міркування. Бажаємо Вам успіху!
4
ТЕМА 1 РІВНЯННЯ ГАЗУ. ПРОЦЕСИ
Основні формули
Рівняння стану ідеального газу
pV = mm RT ,
де μ - молярна маса (маса моля). Барометрична формула
p = p0 exp(-mgh / RT ) ,
де p0 - тиск на висоті h = 0.
Рівняння стану Ван-дер-Ваальсівського газу
æ |
n |
2 |
ö |
ç |
|
×a ÷ |
|
ç p + |
V |
2 ÷(V - n ×b) = nRT , |
|
è |
ø |
||
де ν - кількість молей газу.
1.1 Приклади розв’язання задач
(2.1а)
(2.1б)
(2.1в)
Приклад 1.1
Балон об’ємом 20 л містить суміш водню й азоту при температурі 270С і тиску 25 атм. Маса суміші газів – 0,3 кг. Визначити масу водню, яка міститься в балоні.
|
|
|
Розв’язання |
|
|
|
m1 -? |
|
|
Для розв’язання задачі викорис- |
|||
|
|
|
таємо закон Дальтона та рівняння стану |
|||
V = 20 л= 20×10−3 |
м3, |
|
||||
t = 27°C , |
|
|
ідеального |
газу. |
Також використаємо |
|
|
|
інформацію |
про |
масу суміші |
газів. З |
|
p =25атм= 25×105 |
Па |
|
||||
|
отриманої |
системи рівнянь знайдемо |
||||
, |
|
|
||||
|
|
шукані величини. |
|
|
||
m =0,3 кг. |
|
|
Позначимо |
через m1 |
та m2 |
|
|
|
|||||
відповідно масу водню |
та масу азоту в |
балоні, T = t + 273 - |
||||
абсолютну температуру газів.
5
Згідно із законом Дальтона тиск суміші ідеальних газів дорівнює сумі парціальних тисків цих газів. Тобто
p = p1 + p2 , (1)
де p1 - парціальний тиск водню; p2 - парціальний тиск азоту.
Як відомо, під парціальним тиском розуміють тиск, який створює компонента суміші в даному об’ємі за умови відсутності інших газів. Парціальні тиски для водню та азоту знайдемо за допомогою рівняння Менделєєва-Клапейрона
(2.1а):
p V = m1 |
RT , |
p V = m2 |
RT . |
(2) |
||
1 |
m1 |
|
2 |
m2 |
|
|
|
|
|
|
|
||
У цих рівняннях m1 - молярна маса водню; m2 - молярна маса азоту. Далі із співвідношень (2) знаходимо парціальні тиски p1 , p2 , підставляємо їх у (1) і отримуємо
|
RT |
æ |
|
m2 |
ö |
|
|
|
ç m1 |
|
÷ |
|
|||
p = |
V |
ç m |
+ |
|
|
÷ . |
(3) |
m |
2 |
||||||
|
|
è 1 |
|
|
ø |
|
|
Також використаємо інформацію про загальну масу суміші
m = m1 + m2 . (4)
Систему рівнянь (3) та (4) розв’язуємо відносно невідомих m1 та m2 і знаходимо шукану масу водню m1 . З (4) виразимо
m2 і підставимо в (3):
|
RT |
æ |
|
m - m1 |
ö |
|
|
ç m1 |
|
÷ |
|||
p = |
V |
ç m |
+ |
m |
2 |
÷ . |
|
|
è 1 |
|
|
ø |
|
Звідси |
|
|
|
|
|
|
|
|
|
|
|
m1m2 |
æ |
pV |
|
m |
ö |
|
|||
|
ç |
|
÷ |
(5) |
||||||
|
|
|
- m |
|
||||||
m1 = m |
2 |
- m |
ç RT |
2 |
÷ . |
|||||
|
|
1 |
è |
|
|
|
ø |
|
||
Аналіз отриманого результату
1 Перевіримо, чи дає розрахункова формула (5) правильну одиницю вимірювання шуканої фізичної величини. Для цього в
6
праву й ліву частини цього співвідношення замість символів фізичних величин підставимо їх одиниці вимірювання.
Зрозуміло, що [m1] =кг.
|
|
|
З іншого боку, |
|
|
|
||||||
é m m |
æ |
pV |
|
m |
öù |
|
é |
|||||
|
|
|
1 2 |
ç |
|
- |
|
|
÷ |
|
= |
ê |
êm |
|
-m |
RT |
m |
|
|
||||||
2 |
ç |
|
2 |
÷ú |
|
|||||||
ë |
|
1 |
è |
|
|
|
ø |
û |
|
ê |
||
|
|
|
|
|
|
|
|
|
|
ë |
||
кг |
æ |
Па ×м3 |
|
кг |
ö |
ù |
|
|
ç |
|
- |
|
÷ú |
= кг . |
|
|
|
|
|||||
моль ç Дж ×К/(К ×моль) |
|
кг/моль ÷ |
ú |
|
|||
|
è |
|
|
|
|
|
|
|
|
|
|
øû |
|
||
Тобто кг = кг . Таким чином, розрахункова формула (5) дає правильні одиниці вимірювання.
2 Запишемо фізичні величини, що входять в розрахункову формулу (5), в одиницях СІ й виконаємо обчислення:
|
m1m2 |
æ |
pV |
|
m |
ö |
|
2×10 |
−3 |
×28×10 |
−3 |
|
|||
m1 = |
ç |
- |
÷ |
= |
|
|
´ |
||||||||
m |
2 |
- m |
ç |
RT |
m |
2 |
÷ |
28×10−3 - 2×10−3 |
|||||||
|
|
1 |
è |
|
|
|
ø |
|
|
|
|
|
|
||
æ |
25×105 ×20×10−3 |
|
0,3 |
|
ö |
|
´ç |
|
- |
|
|
÷ |
кг=0,02 кг. |
|
|
−3 |
||||
ç |
8,3×300 |
|
28×10 |
÷ |
|
|
è |
|
|
ø |
|
3 Проведемо дослідження розрахункової формули у граничних випадках.
Розглянемо уявний випадок, коли маса однієї молекули газу, який позначаємо індексом «1», буде дорівнювати нулю. Тоді і їх молярна маса також буде дорівнювати нулю m1 ® 0. З
фізичних міркувань випливає, що в цьому випадку будь-яка кількість молекул цього сорту газу буде мати масу таку, що
дорівнює |
нулю, |
|
тобто m1 ® 0 . |
З розрахункової формули |
||||||||||||||||
випливає такий самий результат. Коли m1 ® 0, то |
||||||||||||||||||||
|
m1m2 |
|
æ |
pV |
|
|
m |
ö |
|
|
|
|
|
|
|
|
||||
|
|
ç |
|
|
÷ |
~ m1 ® 0. |
|
|
||||||||||||
|
|
|
|
|
- m |
|
|
|
||||||||||||
m1 = m |
2 |
- m |
ç RT |
2 |
÷ |
|
|
|||||||||||||
|
|
|
1 |
è |
|
|
|
|
|
ø |
|
|
|
|
|
|
|
|
||
Отже, розрахункова формула не суперечить фізичним |
||||||||||||||||||||
міркуванням. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
m1m2 |
æ |
pV |
|
m |
ö |
|
||||||
|
|
|
|
|
|
|
|
|
ç |
|
÷ |
=0,02 кг. |
||||||||
|
|
|
|
|
|
|
|
|
|
|
- m |
|
||||||||
Відповідь: m1 = m |
|
- m |
|
ç RT |
|
÷ |
||||||||||||||
|
|
|
|
|
|
|
|
|
2 |
|
|
1 |
è |
|
|
|
2 |
ø |
|
|
7
Приклад 1.2
Швидкість відкачування роторного масляного насоса Q =1,5×10−4 м3/с. Який час τ потрібен для того, щоб посудину
місткістю V = 5 л відкачати від нормального повітряного тиску до тиску p = 1,33 Па?
Примітка. Швидкістю відкачування називають об’єм газу, який відкачується за одиницю часу. Зазначимо, що цей об’єм вимірюється при тиску газу в даний момент часу.
|
|
|
Розв’язання |
|
|
|
||
τ - ? |
Розв’язання цієї задачі зводиться до |
|||||||
Q =1,5×10−4 м3/с, |
аналізу |
процесу |
відкачування |
повітря |
||||
V = 5 л=5×10-3 м3, |
насосом |
з |
використанням |
рівняння |
||||
p |
|
= 1×105 Па, |
ідеального газу. |
процес |
відкачування |
|||
|
0 |
|
Розглянемо |
|||||
p = 1,33 Па, |
повітря, |
|
молярна |
маса |
якого |
|||
μ =29×10-3 кг/моль. |
m = 29×10−3 |
кг/моль, роторним насосом. |
||||||
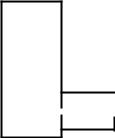
V ,
dV1 = Qdt
K1  K 2
K 2 

Рисунок 1.1
Нехай у деякий момент часу t в посудині об’ємом V міститься повітря, що характеризується тиском p та масою m .
З часом завдяки роботі насоса маса газу m в посудині зменшується. Через це зменшується і тиск p газу в посудині.
Насос працює таким чином. За малий час dt через систему клапанів K1 та K2 (див. рис. 1.1) з посудини видаляється газ, що міститься в об’ємі dV1 = Qdt . Зрозуміло, що зменшення маси
8
газу в посудині dm дорівнює масі газу, який міститься в об’ємі dV1 . Це зменшення газу дорівнює
dm = −ρdV1 = −ρQdt . (1)
Знак «–» у цій формулі означає, що маса газу в посудині об’ємом V зменшується, ρ - густина газу в системі в даний момент часу.
Цю густину газу можна знайти за допомогою рівняння Менделєєва-Клапейрона
pV = |
m RT , |
|
||
|
μ |
|
|
|
звідси |
|
|
|
|
ρ = m |
= |
pμ |
. |
(2) |
|
||||
V |
|
RT |
|
|
Зменшення тиску в посудині |
об’ємом V |
у зв’язку зі |
||
зменшенням маси газу також знаходимо за допомогою рівняння Менделєєва-Клапейрона
pV = m RT |
, => |
dp = dm RT . |
(3) |
|||
μ |
|
|
μV |
|
|
|
Зазначимо, під час відкачування об’єм посудини V |
та |
|||||
температура T не змінюються. |
Далі в |
співвідношення |
(3) |
|||
підставляємо (1) та (2) і отримуємо |
|
|
|
|
|
|
dp = − ρQdt |
RT = − |
pμ |
Qdt |
RT |
|
|
|
|
|||||
μV |
|
|
RT μV |
|
|
|
або |
|
|
|
|
|
|
dp |
= − Qdt . |
|
(4) |
|||
p |
|
V |
|
|
||
Інтегруємо праву і ліву частини співвідношення (4) і знаходимо шуканий час τ :
9

p |
dp |
τ |
æ |
|
Qdt ö |
p |
|
Q |
|
|
V |
|
p |
0 |
|
|
||
ò |
p |
= òç |
- |
V |
÷ , ln |
|
|
= - |
|
t , |
t = |
Q |
ln |
|
. |
(5) |
||
p |
|
V |
|
|
||||||||||||||
p0 |
0 |
è |
|
ø |
0 |
|
|
|
|
p |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Аналіз отриманого результату
1 Перевіримо, чи дає розрахункова формула (5) правильну одиницю вимірювання шуканої фізичної величини. Для цього в праву й ліву частини цього співвідношення замість символів фізичних величин підставимо їх одиниці вимірювання.
Зрозуміло, що [τ] = кг.
|
|
З іншого боку, |
|
||||||
éV |
|
p |
0 |
ù |
é |
м3 ù |
|
||
ê |
|
ln |
|
ú |
= ê |
|
ú |
= с . |
|
|
p |
|
|||||||
ëQ |
|
û ë |
(м3 / с)û |
|
|||||
Тобто с = с . Таким чином, розрахункова формула (5) дає правильні одиниці вимірювання.
2 Запишемо фізичні величини, що входять в розрахункову формулу (5), в одиницях СІ й виконаємо обчислення:
|
V |
|
p |
0 |
|
|
5×10−3 |
æ |
1×105 |
ö |
|
|
t = |
|
ln |
|
= |
|
|
|
lnç |
|
÷ |
с=374 с. |
|
|
|
|
|
|
−4 |
|
||||||
|
Q |
|
p |
|
1,5×10 |
ç |
1,33 |
÷ |
|
|||
|
|
|
|
è |
ø |
|
||||||
3 Проведемо дослідження розрахункової формули у граничних випадках.
Розглянемо випадок, коли швидкість відкачування насоса буде наближатись до нуля Q → 0 . У цій ситуації відкачування
практично не буде відбуватись. Тобто час відкачування буде
зростати |
до |
нескінченності |
τ → ∞ . З |
розрахункової формули |
|||||
випливає |
такий |
|
самий |
результат. |
Коли Q → 0 , то |
||||
t = V ln |
|
p0 |
~ |
1 |
® |
1 |
= ¥ . |
|
|
|
p |
|
0 |
|
|
||||
Q |
|
Q |
|
|
|
||||
Отже, розрахункова формула (5) не суперечить фізичним міркуванням.
Відповідь: t = VQ ln pp0 =374 с.
10
