
pg_met_pr2
.pdfЗрозуміло, що молярна теплоємність [C] =Дж/(моль·К). Також, виходячи з умови задачі p = p0eaV , T = T0eaV , неважко з’ясувати, що коефіцієнт a у системі СІ вимірюється в 1/м3.
З іншого боку, |
|
|
|||
é |
R ù |
|
|
|
|
êCV + |
|
ú |
=Дж/(моль·К). |
|
|
|
|
|
|||
ë |
aV û |
|
|
|
|
Тобто |
Дж/(моль·К)=Дж/(моль·К). |
Таким |
чином, |
||
розрахункова формула (5) дає правильні одиниці вимірювання. Зрозуміло, що молярна теплоємність [C] =Дж/(моль·К).
З іншого боку,
é |
R ù |
|
|
êCV + |
|
ú |
=Дж/(моль·К). |
|
|||
ë |
aV +1û |
|
|
Тобто Дж/(моль·К)=Дж/(моль·К). Таким чином, розрахункова формула (7) дає правильні одиниці вимірювання.
2 Проведемо дослідження розрахункової формули у граничних випадках.
Розглянемо випадок (а), коли в співвідношенні T = T0 ×eaV стала a дорівнює нулю ( a = 0 ). Це означає, що процес є
ізотермічним, тому що T = T ×eaV = T ×e0×V |
= T = const . Як |
|
0 |
0 |
0 |
відомо, при ізотермічному процесі теплоємність дорівнює
нескінченності |
C = dQ / dT = dQ / 0 = ∞ . З |
розрахункової |
|||||||
формули (5) |
випливає такий самий результат. Коли a = 0 , то |
||||||||
C = C + |
R |
|
= C + |
R |
= ¥ . |
|
|
||
|
|
|
|
||||||
V |
aV |
|
V |
0×V |
|
|
|
||
|
|
|
|
|
|
||||
Отже, розрахункова формула (5) не суперечить фізичним |
|||||||||
міркуванням. |
|
|
|
|
|
p = p0 ×eaV |
|||
Розглянемо випадок (б), коли в співвідношенні |
|||||||||
стала a дорівнює |
нулю |
( a = 0 ). Це означає, |
що |
процес є |
|||||
ізобаричним, |
тому |
що |
p = p0 ×eaV = p0 ×e0×V = p0 = const . Як |
||||||
відомо, молярна теплоємність для процесу при постійному тиску відповідно до рівняння Маєра дорівнює Cp = CV + R . З
41

розрахункової формули (7) випливає такий самий результат.
Коли a = 0 , то C = CV + |
R |
|
= CV + |
R |
|
= CV + R . |
|
aV +1 |
0×V +1 |
||||||
|
|
|
|||||
Отже, розрахункова формула (7) не суперечить фізичним міркуванням.
Відповідь: а) C = CV + R / aV ; б) C = CV + R /(1+ aV ) .
Приклад 2.5
Дві теплоізольовані посудини місткістю V1 =1л та V2 = 3л з’єднані трубкою з краном. До відкриття крана у першій
посудині міститься |
азот |
під |
тиском |
p = 5×104 Па при |
|||||
|
|
|
|
T1 = 273К , |
|
|
1 |
|
|
температурі |
|
а в |
другій – |
аргон під |
тиском |
||||
p |
2 |
=1,5×105 |
Па |
при |
температурі |
T = 373К . Якими |
стануть |
||
|
|
|
|
|
|
2 |
|
|
|
рівноважні значення тиску та температури, якщо відкрити кран?
Розв’язання
Після відкриття крана азот та аргон рівномірно розподіляться в системі двох посудин. При цьому завдяки перемішуванню газів установлюються рівноважна температура T та рівноважний тиск p . Цей
рівноважний тиск p згідно з законом Дальтона буде дорівнювати сумі парціальних тисків азоту p1¢ та аргону p¢2 :
¢ |
¢ |
(1) |
p = p1 |
+ p2 . |
Для знаходження рівноважної температури T слід взяти до уваги, що система двох посудин теплоізольована. Це означає, що теплообмін з навколишніми тілами відсутній ( Q = 0 ). Об’єм
системи двох посудин не змінюється. Це означає, що робота газів над зовнішніми тілами дорівнює нулю ( A = 0 ). Тому, виходячи з першого закону термодинаміки, можемо записати для системи газів
Q = DUсист + А , Q = 0 , A = 0 ,
42
де DUсист - зміна внутрішньої енергії системи. Звідси знаходимо
DUсист = 0 або Uсист = const . |
(2) |
Тобто внутрішня енергія системи газів в умовах даної задачі не змінюється.
Таким чином, для розв’язання задачі необхідно використати умову збереження внутрішньої енергії газів, закон Дальтона та рівняння ідеального газу (2.1а).
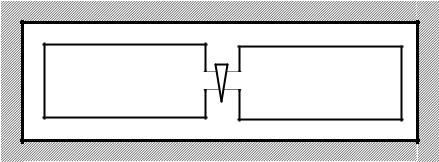
A |
B |
|
T1 p1 V1 m1 μ1 g1 |
T2 p2 V2 m2 |
μ2 g2 |
Рисунок 2.3
Перейдемо до безпосереднього розв’язання задачі. Знайдемо рівноважний тиск p , виходячи з співвідношення (1).
Позначимо через m1 та m1 відповідно масу та молярну масу азоту, а через m2 та m2 відповідно масу та молярну масу аргону.
Тоді парціальні тиски газів у кінцевому стані будуть дорівнювати
p1¢ = |
|
1 |
× m1 |
RT , |
|
|||
(V1 |
+V2 ) |
|
||||||
|
|
|
m1 |
|
|
|||
¢ |
|
|
1 |
|
m2 |
|
||
p2 |
= |
|
|
× |
|
RT . |
(3) |
|
(V1 |
+V2 ) |
m2 |
||||||
|
|
|
|
|
||||
Тут використали рівняння ідеального газу (2.1а), а також те, що обидва гази рівномірно розподілились в об’ємі двох посудин V1 +V2 , через T позначили рівноважну температуру. Щоб
43
знайти m1 / m1 та |
m2 / m2 , застосуємо рівняння |
Менделєєва- |
|||||||||
Клапейрона до початкового стану газів: |
|
||||||||||
p V = m1 |
RT , |
p V = m2 RT . |
|
||||||||
1 |
1 |
m1 |
1 |
|
|
2 |
2 |
2 |
|
||
|
|
|
|
|
|
|
m2 |
|
|||
Звідси |
|
|
|
|
|
|
|
|
|
|
|
|
m1 |
= |
|
p1V1 |
, |
m2 |
= |
p2V2 |
. |
(4) |
|
|
|
|
|
||||||||
|
m |
|
|
RT |
m |
2 |
|
RT |
|
||
|
1 |
|
|
1 |
|
|
|
2 |
|
|
|
Тоді рівноважний тиск p знайдемо, підставляючи в (1) формули (3) та (4):
p = |
|
1 |
|
× |
p1V1 |
|
RT + |
|
|
1 |
|
× |
|
p2V2 |
RT |
|||
(V |
+V ) |
RT |
(V |
+V |
|
RT |
||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
1 |
2 |
|
|
1 |
|
|
|
|
1 |
2) |
|
|
|
|
2 |
|
|
або |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
æ |
p1V1 |
|
|
p2V2 |
ö |
|
|
|||||
|
|
|
|
|
ç |
|
|
÷ |
|
|
||||||||
|
|
p = |
|
|
×ç |
|
|
+ |
|
|
|
÷ . |
(5) |
|||||
|
|
V +V |
|
T |
|
|
T |
|
||||||||||
|
|
|
|
1 |
2 |
è |
1 |
|
|
2 |
|
ø |
|
|
||||
Знайдемо рівноважну температуру T . Для цього використаємо те, що повна внутрішня енергія газів згідно з (2) не змінюється. Вона однакова в початковому та кінцевому станах:
Uсист =U1 +U2 =U1¢ +U2¢ = const . |
(6) |
Тут через U1 та U2 позначено внутрішні енергії азоту та аргону в початковому стані, U1¢ та U2¢ –внутрішні енергії азоту та
аргону в кінцевому стані. Внутрішні енергії в початковому стані азоту та аргону відповідно дорівнюють
U |
1 |
= |
m1 |
× |
RT1 |
, |
U |
2 |
= |
m2 |
× |
RT2 |
. |
(7) |
|||||
|
|
||||||||||||||||||
|
|
m |
|
g |
1 |
-1 |
|
|
|
m |
2 |
|
g |
2 |
-1 |
|
|||
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Внутрішні енергії азоту та аргону в кінцевому стані відповідно дорівнюють
44
¢ |
|
m1 |
|
RT |
|
¢ |
|
m2 |
|
RT |
|
||||
U1 |
= |
|
× |
|
|
|
, |
U2 |
= |
|
|
× |
|
. |
(8) |
m |
g |
1 |
-1 |
m |
2 |
g -1 |
|||||||||
|
|
1 |
|
|
|
|
|
|
|
1 |
|
|
|||
Для отримання співвідношень (7), (8) використали формулу (2.2в). У формулах (7) та (8) g1 та g2 - сталі адіабати для азоту
та аргону відповідно. Як відомо, ці сталі пов’язані з кількістю ступенів вільності молекули газу такими співвідношеннями:
g1 |
= |
i1 + 2 |
, g2 |
= |
i2 + 2 |
. |
|
|
|||||
|
|
i1 |
|
i2 |
||
Азот – двоатомний газ, для якого кількість ступенів вільності i1 = 5 . Аргон – одноатомний газ, для якого кількість ступенів
вільності i2 = 3. Тому
g1 |
= |
5 + |
2 |
=1,4, |
g2 |
= |
3+ |
2 |
=1,67. |
5 |
|
3 |
|
||||||
|
|
|
|
|
|
|
|
Далі підставляємо (7), (8) в (6) і знаходимо
m1 × |
|
RT1 |
|
+ m2 |
× |
RT2 |
|
= |
m1 × |
|
|
RT |
|
|
+ m2 |
× |
|
|
RT |
|
, |
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
g |
|
-1 |
|
g |
|
-1 |
|
|
|||||||||||||||||||||||||||
m |
g |
1 |
-1 |
|
|
m |
2 |
|
g |
2 |
|
-1 |
|
|
m |
|
1 |
|
m |
2 |
|
|
2 |
|
|
|
||||||||||||||||
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
ém1 |
|
|
|
RT1 |
|
m2 |
|
|
|
RT2 ù |
ém1 |
|
|
R m2 |
|
|
R |
ù |
. (9) |
|||||||||||||||||||||||
T = êm |
|
× |
|
|
|
+ m |
|
× |
|
|
|
ú |
/ê m |
× |
|
|
|
+ m |
|
|
× |
|
|
|
ú |
|||||||||||||||||
|
g |
1 |
-1 |
|
2 |
g |
2 |
-1 |
g |
1 |
-1 |
2 |
g |
2 |
-1 |
|||||||||||||||||||||||||||
ë 1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
û |
ë |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
û |
|
|||||||||
Тепер у (9) підставимо (4) і отримуємо розрахункову формулу рівноважної температури T у кінцевому стані
æ |
p1V1 |
|
p2V2 |
ö |
æ |
p1V1 |
|
p2V2 |
ö |
|
||||||||
ç |
|
÷ ç |
|
÷ |
|
|||||||||||||
T = ç |
|
|
|
+ |
|
|
|
÷ |
/ç |
|
|
|
+ |
|
|
|
÷ . |
(10) |
g |
1 |
-1 |
g |
2 |
-1 |
T (g |
1 |
-1) |
T (g |
2 |
-1) |
|||||||
è |
|
|
|
|
|
ø |
è |
1 |
|
2 |
|
ø |
|
|||||
Тиск газів у кінцевому стані знаходимо, підставивши в (5) знайдену рівноважну температуру (10):
45
æ |
|
p1V1 |
+ |
p2V2 |
ö |
æ |
p1V1 |
+ |
p2V2 |
ö |
|
|
||||||||||
ç |
|
÷ |
×ç |
÷ |
|
|
||||||||||||||||
ç |
|
T |
|
|
|
T |
÷ ç |
g |
1 |
-1 |
|
g |
2 |
-1 |
÷ |
|
|
|||||
p = |
è |
1 |
|
|
|
2 |
|
ø è |
|
|
|
|
|
|
ø |
. |
(11) |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ö |
|
|
|
|
||||
æ |
|
p1V1 |
|
|
|
|
p2V2 |
|
|
|
|
|
|
|
|
|||||||
ç |
|
|
|
|
|
|
|
÷ |
|
|
|
|
|
|
||||||||
ç |
|
|
|
|
+ |
|
|
|
|
÷(V1 +V2 ) |
|
|||||||||||
T (g |
1 |
-1) |
T (g |
2 |
-1) |
|
|
|||||||||||||||
è |
|
1 |
|
|
|
|
2 |
|
|
|
|
ø |
|
|
|
|
|
|
||||
Аналіз отриманого результату
1 Перевіримо, чи дають розрахункові формули (10) та (11) правильні одиниці вимірювання шуканої фізичної величини. Для цього в праву й ліву частини цих співвідношень замість символів фізичних величин підставимо їх одиниці вимірювання.
Зрозуміло, що [T] = К.
|
|
|
|
З іншого боку, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
éæ |
|
p V |
p V |
ö æ |
|
|
p V |
|
|
|
|
|
|
p V |
|
öù |
Па ×м3 ×К |
|
|||||||||||||||||||
êç |
|
|
1 1 |
|
+ |
|
|
2 2 |
|
÷ |
/ç |
|
|
1 1 |
|
|
+ |
|
|
|
|
2 2 |
÷ú = |
Па ×м3 |
= К . |
||||||||||||
|
|
|
|
g |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
ç g |
1 |
-1 |
|
2 |
-1÷ ç T (g |
1 |
-1) |
|
T (g |
2 |
-1) |
÷ |
|
|||||||||||||||||||||||
ëè |
|
|
|
|
|
|
|
|
|
|
ø è |
|
1 |
|
|
|
|
2 |
|
|
|
|
øû |
|
|
||||||||||||
|
|
|
|
Тобто К=К. Таким чином, розрахункова формула (10) дає |
|||||||||||||||||||||||||||||||||
правильні одиниці вимірювання. |
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
Зрозуміло, що [ p] = Па. |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
З іншого боку, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
é æ |
|
p V |
p V |
|
|
ö æ |
|
p V |
|
|
|
p V |
|
|
ö ù |
|
|
|
|
|
|
|
|||||||||||||||
ê |
ç |
|
|
1 1 |
+ |
|
2 2 |
|
÷× |
ç |
|
|
1 1 |
|
|
+ |
|
2 2 |
|
÷ |
ú |
|
|
|
Па ×м3 |
/ К Па ×м3 |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
g |
|
|
|
|
|
||||||||||||||||||||||
ç |
|
|
T |
T |
|
|
|
÷ ç g |
1 |
-1 |
|
2 |
-1 |
÷ |
|
|
|
|
|||||||||||||||||||
ê |
è |
|
|
|
1 |
|
|
|
|
2 |
|
|
ø |
è |
|
|
|
|
|
|
|
|
|
|
ø |
ú |
= |
|
|
|
× |
= Па . |
|||||
êæ |
|
|
|
p V |
|
|
|
|
|
|
p V |
|
ö |
|
|
|
|
|
|
ú |
|
Па ×м3 |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
/ К м3 |
|
|||||||||||||||||
|
ç |
|
|
|
1 1 |
|
|
|
|
|
|
|
|
2 |
|
2 |
|
÷ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
ê |
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
ç T (g -1) |
T (g |
|
|
-1) |
|
|
(V +V )ú |
|
|
|
|
|
|
|
|||||||||||||||||||||||
ê |
|
|
2 |
|
÷ |
1 2 |
|
ú |
|
|
|
|
|
|
|
||||||||||||||||||||||
ë |
è |
|
|
1 1 |
|
|
|
|
|
|
|
2 |
|
|
|
|
ø |
|
|
|
|
|
|
û |
|
|
|
|
|
|
|
||||||
Тобто Па=Па. Таким чином, розрахункова формула (11) дає правильні одиниці вимірювання.
2 Запишемо фізичні величини, що входять в розрахункові формули (10) та (11), в одиницях СІ й виконаємо обчислення:
æ |
p1V1 |
|
p2V2 |
ö |
æ |
p1V1 |
|
p2V2 |
ö |
|
||||||||
ç |
|
÷ ç |
|
÷ |
|
|||||||||||||
T = ç |
|
|
|
+ |
|
|
|
÷ |
/ç |
|
|
|
+ |
|
|
|
÷ |
= |
g |
1 |
-1 |
g |
2 |
-1 |
T (g |
1 |
-1) |
T (g |
2 |
-1) |
|||||||
è |
|
|
|
|
|
ø |
è |
1 |
|
2 |
|
ø |
|
|||||
46
æ |
5×104 ×1×10−3 |
|
|
1,5×105 |
|
×3×10−3 ö |
|
||||||||||||||||||||
ç |
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
÷ |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
ç |
|
|
|
1,4 -1 |
|
|
|
|
|
|
|
1,67 -1 |
|
|
÷ |
|
|
||||||||||
= |
è |
|
|
|
|
|
|
|
|
|
|
|
|
ø |
|
К = 353 К. |
|||||||||||
|
5×104 ×1×10−3 |
|
|
1,5×105 |
|
×3×10−3 ö |
|||||||||||||||||||||
æ |
+ |
|
|
||||||||||||||||||||||||
ç |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
÷ |
|
|
||||
ç |
273×(1,4 -1) |
|
|
|
373×(1,67 -1) |
÷ |
|
|
|||||||||||||||||||
è |
|
|
|
ø |
|
|
|||||||||||||||||||||
|
|
æ |
|
p1V1 |
+ p2V2 |
ö |
æ |
p1V1 |
+ |
p2V2 |
ö |
|
|||||||||||||||
|
|
ç |
|
÷ |
×ç |
÷ |
|
||||||||||||||||||||
|
|
ç |
|
T |
|
|
|
T |
|
÷ ç |
g |
1 |
-1 |
|
g |
2 |
-1 |
÷ |
|
||||||||
p = |
è |
1 |
|
|
2 |
|
ø è |
|
|
|
|
|
|
ø |
= |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ö |
|
|
|
|
|||||||
|
|
æ |
|
p1V1 |
|
|
|
p2V2 |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
ç |
|
|
|
|
|
|
÷ |
|
|
|
|
|
|
|
|||||||||||
|
|
ç |
|
|
|
|
+ |
|
|
|
|
÷(V1 +V2 ) |
|
||||||||||||||
|
|
T (g |
1 |
-1) |
T (g |
2 |
-1) |
|
|
||||||||||||||||||
|
|
è |
|
1 |
|
|
|
|
2 |
|
|
|
|
|
ø |
|
|
|
|
|
|
|
|||||
æ |
5×104 ×10−3 |
+ |
1,5×105 ×3×10−3 öæ |
5×104 |
×10−3 |
+ |
1,5×105 ×3×10−3 ö |
||||||||||
ç |
|
|
|
|
|
|
֍ |
|
|
|
|
÷ |
|
||||
ç |
273 |
|
|
|
|
373 |
|
֍ |
1,4 |
-1 |
|
1,67 -1 |
÷ |
|
|||
= |
è |
|
|
|
|
|
øè |
|
ø |
Па = |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
æ |
5×10 |
4 |
×10 |
−3 |
|
5 |
×3 |
×10 |
−3 |
ö |
|
|
|
|||
|
|
|
|
|
|
|
|||||||||||
|
|
ç |
|
|
+ 1,5×10 |
|
|
÷(1×10 |
−3 |
+ 3×10−3 ) |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
ç |
273 |
×(1,4 -1) |
373×(1,67 -1) |
÷ |
|
|
|
|
|||||||
|
|
è |
ø |
|
|
|
|
||||||||||
=1,23×105 Па.
3 Проведемо дослідження розрахункової формули у граничних випадках.
Розглянемо випадок, коли тиски та температури газів у вихідному стані є однаковими ( p1 = p2 , T1 = T2 ). Зрозуміло, що
в цьому випадку після відкриття крана тиск та температура змінюватись не будуть. Тобто в кінцевому стані рівноважні тиск та температура будуть такими самими, як і у вихідному стані ( p = p1 = p2 ). З розрахункової формули випливає такий самий
результат. Коли p1 = p2 , T1 = T2 , то
æ |
|
p1V1 |
|
|
p2V2 |
ö |
æ |
|
p1V1 |
|
|
|
|
|
p2V2 |
|
|
ö |
|
|
|
||||||||||||||
ç |
|
|
|
÷ ç |
|
|
|
|
|
|
|
|
÷ |
= |
|
||||||||||||||||||||
T = ç |
|
|
|
+ |
|
|
|
|
|
|
÷ |
/ç |
|
|
|
|
|
+ |
|
|
|
÷ |
|
||||||||||||
g |
1 |
-1 |
|
g |
2 |
-1 |
|
T (g |
1 |
-1) |
T (g |
2 |
-1) |
|
|||||||||||||||||||||
è |
|
|
|
|
|
|
|
|
|
ø |
è |
1 |
|
|
|
|
|
|
2 |
|
|
|
|
ø |
|
|
|
||||||||
|
æ |
|
V |
|
|
|
|
V |
ö |
æ |
|
p |
æ |
|
|
V |
|
|
p V |
|
|
öö |
|
||||||||||||
= p |
ç |
|
|
1 |
|
+ |
|
|
|
|
2 |
|
÷ |
/ç |
|
1 |
ç |
|
|
|
1 |
|
+ |
|
|
2 2 |
|
|
÷÷ |
= T . |
|||||
|
|
|
|
|
g |
|
|
|
T |
|
|
|
-1) |
|
|
|
|
|
|||||||||||||||||
1 |
ç g -1 |
|
|
2 |
-1÷ |
ç |
|
ç (g |
1 |
|
T (g |
2 |
-1) |
÷÷ |
1 |
||||||||||||||||||||
|
è |
|
1 |
|
|
|
|
|
|
|
|
ø |
è |
1 |
è |
|
|
|
|
|
|
2 |
|
|
|
|
øø |
|
|||||||
47
æ |
|
p1V1 |
|
p2V2 |
ö æ |
p1V1 |
|
p2V2 |
ö |
|
|
p1 |
|
|
|
|
|
æ |
|
V1 |
|
|
V2 |
ö |
|
|||||||||||
ç |
|
|
÷ ç |
|
÷ |
|
|
|
|
|
|
|
ç |
|
|
|
÷ |
|
||||||||||||||||||
ç |
|
|
|
+ |
|
|
|
÷×ç |
|
|
|
|
+ |
|
|
|
÷ |
|
|
|
(V1 |
+V2 )× p1ç |
|
|
+ |
|
|
|
÷ |
|
||||||
T |
|
T |
g |
1 |
-1 |
g |
2 |
-1 |
T |
g -1 |
g |
2 |
-1 |
|||||||||||||||||||||||
p = |
è |
1 |
|
|
2 |
|
ø è |
|
|
|
|
|
|
ø |
= |
|
1 |
|
|
|
|
|
è |
|
1 |
|
|
|
|
ø |
= p . |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
æ |
|
p1V1 |
|
|
|
p2V2 |
|
|
ö |
|
|
|
|
|
|
p1 |
æ |
|
V1 |
|
|
V2 |
ö |
|
|
|
1 |
|||||||||
ç |
|
|
|
|
|
|
÷ |
|
|
|
|
|
|
ç |
|
|
|
÷ |
|
|
|
|
|
|||||||||||||
ç |
|
|
|
+ |
|
|
|
|
÷(V1 |
+V2 ) |
|
ç |
|
|
|
+ |
|
|
|
|
÷(V1 |
+V2 ) |
||||||||||||||
T (g |
1 |
-1) |
T (g |
2 |
-1) |
|
T |
(g |
1 |
-1) |
(g |
2 |
-1) |
|
||||||||||||||||||||||
è |
|
1 |
|
|
|
|
2 |
|
|
|
ø |
|
|
|
|
|
|
1 |
è |
|
|
|
|
|
|
ø |
|
|
|
|
|
|||||
Отже, розрахункові формули не суперечать фізичним
міркуванням. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
æ |
p1V1 |
|
|
|
p2V2 |
|
ö |
æ |
|
|
p1V1 |
|
|
p2V2 |
ö |
|
|||||||||||||
Відповідь: |
T = |
ç |
|
+ |
|
÷ ç |
|
|
+ |
|
÷ |
= 353 К, |
|||||||||||||||||||||||||||
ç |
|
|
|
|
|
|
|
÷ |
/ç |
|
|
|
|
|
|
|
|
÷ |
|||||||||||||||||||||
g |
1 |
-1 |
g |
2 |
-1 |
T (g |
1 |
-1) |
T (g |
2 |
-1) |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
è |
|
|
|
|
|
|
|
|
|
|
|
ø |
è |
|
1 |
|
|
|
2 |
|
ø |
|
|||||||
æ |
|
p1V1 |
+ |
|
p2V2 |
ö |
|
æ |
p1V1 |
+ |
p2V2 |
ö |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
ç |
|
|
÷ |
×ç |
÷ |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
ç |
|
T |
|
|
|
|
T |
|
|
÷ |
|
ç |
g |
1 |
-1 |
|
|
g |
2 |
-1 |
÷ |
|
|
|
|
|
|
|
|
|
|
||||||||
p = |
è |
1 |
|
|
|
2 |
|
|
ø |
|
è |
|
|
|
|
|
|
|
|
|
|
ø |
=1,23×105 |
Па. |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ö |
|
|
|
|
|
|
|
|
|
|
|
|||||||||
æ |
|
p1V1 |
|
|
|
|
|
|
p2V2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
ç |
|
|
|
|
|
|
|
|
|
|
÷ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
ç |
|
|
|
|
+ |
|
|
|
|
÷(V1 |
+V2 ) |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
T (g |
1 |
-1) |
T (g |
2 |
-1) |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
è |
|
1 |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
ø |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
2.2 Задачі для самостійного розв’язання
2.1Обчислити питомі теплоємності сv і сp газів: 1) гелію; 2) водню; 3) вуглекислого газу.
2.2Різниця питомих теплоємностей cV - cp деякого
двоатомного газу дорівнює 260 Дж/(кг×К). Знайти молярну масу
μгазу та його питомі теплоємності cV і cp .
2.3Які питомі теплоємності сv і сp суміші газів, що містить кисень масою m1=10 г і азот масою m=20 г?
2.4Визначити питому теплоємність сv суміші газів, що містить V1=5 л водню і V2=3 л гелію. Гази знаходяться в однакових умовах.
2.5Визначити питому теплоємність сp суміші кисню і азоту,
якщо кількість речовини n1 |
першої компоненти дорівнює |
||
2 |
молям, |
а кількість речовини |
n2 другої компоненти дорівнює |
4 |
молям. |
|
|
48
2.6У балоні містяться аргон і азот. Визначити питому
теплоємність сv суміші цих газів, якщо масові частини аргону (ω1) і азоту (ω2) однакові і дорівнюють ω=0,5.
2.7Суміш газів складається з хлору і криптону, взятих в однакових умовах і в однакових об'ємах. Визначити питому теплоємність сp суміші.
2.8Визначити питому теплоємність сv суміші ксенону і кисню, якщо кількості речовини газів у суміші однакові і дорівнюють ν .
2.9Знайти показник адіабати γ для суміші газів, що містить гелій масою m1=10 г і водень масою m2=4 г.
2.10Суміш газів складається з аргону і азоту, взятих в однакових умовах і в однакових об'ємах. Визначити показник
адіабати γ такої суміші.
2.11Знайти показник адіабати γ суміші водню і неону, якщо масові частини обох газів у суміші однакові і дорівнюють ω=0,5.
2.12Знайти показник адіабати γ суміші газів, що містить кисень і аргон, якщо кількості речовини того й іншого газу в суміші однакові і дорівнюють ν .
2.13 На нагрівання кисню масою m=160 г на T=12 К було витрачено кількість теплоти Q=1,76 кДж. Як проходив процес: при постійному об'ємі або постійному тиску?
2.14 При адіабатному стисканні газу його об'єм зменшився в n=10 разів, а тиск збільшився в k=21,4 разів. Визначити відношення Cp /CV теплоємностей газів.
2.15Водень масою m=4 г був нагрітий на T=10 К при постійному тиску. Визначити роботу А, яку виконує газ під час розширення.
2.16Газ, що займав об'єм V1=12 л під тиском p=100 кПа, був ізобарно нагрітий від температури T1=300 К до T2 =400 К. Визначити роботу розширення газу А.
2.17Яка робота А виконується при ізотермічному розширенні водню масою m=5 г, узятого при температурі T=290 К, якщо об'єм газу збільшується в три рази?
49
2.18 При адіабатному стисканні кисню масою m=1 кг здійснена робота А =100 кДж. Визначити кінцеву температуру T2 газу, якщо до стискання кисень знаходився при температурі
T1=300 К.
2.19 Визначити роботу А адіабатного розширення водню масою m=4 г, якщо температура газу зменшилась на T=10 К.
2.20 Азот масою т=2 г, мав температуру T1=300 К, був адіабатично стиснутий так, що його об'єм зменшився в n=10 разів. Визначити кінцеву температуру T2 газу і роботу А на стискання газу.
2.21Кисень, що займав об'єм V1=l л під тиском p1=1,2 МПа, адіабатично розширився до об'єму V2=10 л. Визначити роботу розширення газу А.
2.22Азот масою m=5 кг нагріли на T=150 К при постійному об'ємі. Знайти: 1) кількість теплоти Q, що надана
газу; 2) зміну U внутрішньої енергії; 3) виконану газом роботу
А.
2.23 Водень займає об'єм V1=10 м3 при тиску p1=100 кПа. Газ нагріли при постійному об'ємі до тиску p2=300 кПа. Визначити: 1) зміну U внутрішньої енергії газу; 2) роботу А, виконану газом; 3) кількість теплоти Q, одержану газом.
2.24При ізохорному нагріванні кисню об'ємом V=50 л тиск газу змінився на p=0,5 МПа. Знайти кількість теплоти Q, одержану газом.
2.25Балон ємністю V=20 л містить водень при температурі
T=300 К під тиском p=0,4 МПа. Якими будуть температура T1 і тиск p1, якщо газу передати кількість теплоти Q=6 кДж?
2.26Кисень нагрівається при постійному тиску р=80 кПа. Його об'єм збільшується від V1=1 м3 до V2=3 м3. Визначити:
1)зміну U внутрішньої енергії кисню; 2) роботу А, що виконана ним при розширенні; 3) кількість теплоти Q, одержану газом.
2.27Азот нагрівається при постійному тиску. При цьому йому було надано кількість теплоти Q=21 кДж. Визначити
50
