
- •1. Коллоидная химия. Свойства коллоидных систем. Признаки объектов коллоидной химии.
- •2. Классификация коллоидных систем.
- •5.Очистка коллоидных систем: диализ, ультрафильтрация.
- •7. Поверхностное натяжение. Зависимость поверхностного натяжение от различных факторов. Методы измерения поверхностного натяжения.
- •12. Изотермы адсорбции и поверхностного натяжения растворов пав. Уравнение Шишковского.
- •14. Представления о полимолеку-
- •15. Получение, классификация твердых пористых адсорбентов.
- •16. Понятия о капиллярных явлениях. Теория капиллярной конденсации.
- •20. Избирательное смачивание. Способы определения краевого угла смачивания. Инверсия смачиваемости поверхности.
- •22. Седиментация суспензий и седиментационный анализ дисперсных систем.
- •26. Реологические свойства структурированных жидкообразных и твердообразных систем. Вязкость агрегативно устойчивых дисперсных систем.
- •27 Агрегативная устойчивость дисп сист.Факторы агрег устойчив:
- •30Электрокинетич потенциал.Влияние разл факторов на вел электрокин потенциала.
- •31. Коагуляция дисперсных систем. Факторы, влияющие на электролитную коагуляцию дисперсных систем. Быстрая и медленная коагуляция.
- •39. Пены. Методы получения. Устойчивость и разрушение пен. Практическое значение пен.
- •19Адгезия.Когезия.Смачивание,Краевые углы смачивания и работа адгезии.
19Адгезия.Когезия.Смачивание,Краевые углы смачивания и работа адгезии.
А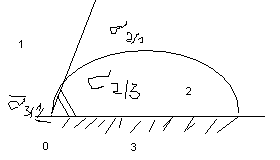 дгезия-это
межфазное взаимодействие конденсир
тел разной природы. Идет с уменьшением
поверх энергии за счет взаимодейств
межфазных границ.Wа-раб
адгезии. Раб адгезии численно равна раб
обратимого изотермич разрыва соед
единич площади. Wa=2/1+3/1-2/3
–ур-ие
Дюпре. Когезия- внутрифазное взаимод,
обусл силами межмолекулярн притяж
различн природы. Характериз раб когезии
Wк.
Это обратимая изотерм раб разрыва тела
по сечению единичной площади. Wк=22/1.
Параметры:
энергия преобраз, тем-ра кипения, поверх
натяжение и тд. Смачивание-это поверх
явл,которое возник при взаимод ж с тв
или с др жидк телом при одновременном
контакте 3-х
несмешивающихся
фаз, одна из которых обычно явл газом.
Нанесем на тв поверхраздела фаз каплю
жидк и рассм усл равновесия поверх
сил(случай контакта 3 фаз). 3/1=2/3+2/1cos-
зак Юнга. -
это краевой угол смач. Он образ касательными
к межфазным поверх ограничивающ смачив
жидкости и имеющ вершину на линии раздела
фаз.Если угол менише 90-смочивается, если
больше 90-не смачив. Wa=2/1+2/1cos=
2/1(1+
cos)-ур-ие
Дюпре-Юнга. При рассм смач пов-тей делаем
выводы:1лиофобн пов-ти(легко смач)
а)
дгезия-это
межфазное взаимодействие конденсир
тел разной природы. Идет с уменьшением
поверх энергии за счет взаимодейств
межфазных границ.Wа-раб
адгезии. Раб адгезии численно равна раб
обратимого изотермич разрыва соед
единич площади. Wa=2/1+3/1-2/3
–ур-ие
Дюпре. Когезия- внутрифазное взаимод,
обусл силами межмолекулярн притяж
различн природы. Характериз раб когезии
Wк.
Это обратимая изотерм раб разрыва тела
по сечению единичной площади. Wк=22/1.
Параметры:
энергия преобраз, тем-ра кипения, поверх
натяжение и тд. Смачивание-это поверх
явл,которое возник при взаимод ж с тв
или с др жидк телом при одновременном
контакте 3-х
несмешивающихся
фаз, одна из которых обычно явл газом.
Нанесем на тв поверхраздела фаз каплю
жидк и рассм усл равновесия поверх
сил(случай контакта 3 фаз). 3/1=2/3+2/1cos-
зак Юнга. -
это краевой угол смач. Он образ касательными
к межфазным поверх ограничивающ смачив
жидкости и имеющ вершину на линии раздела
фаз.Если угол менише 90-смочивается, если
больше 90-не смачив. Wa=2/1+2/1cos=
2/1(1+
cos)-ур-ие
Дюпре-Юнга. При рассм смач пов-тей делаем
выводы:1лиофобн пов-ти(легко смач)
а)![]() полное
смачивание=0,cos=1,Wa=21=Wк.Взаимод
между фазами = взаим внутри фазы.б)неполное
смачивание
полное
смачивание=0,cos=1,Wa=21=Wк.Взаимод
между фазами = взаим внутри фазы.б)неполное
смачивание
![]() 0<<90,0<cos<1?
0<<90,0<cos<1?![]() <Wa<Wk
2Лиофобные поверхности:а)
<Wa<Wk
2Лиофобные поверхности:а)![]() полное
несмачивание=180,
cos=-1,W=0.
б)несмачивание
полное
несмачивание=180,
cos=-1,W=0.
б)несмачивание![]() 90<0<180,-1<cos<0,0<Wa<
90<0<180,-1<cos<0,0<Wa<![]() .Лучше
смачивает данную поверх та жидк, которая
ближе к ней по полярности. Чем выше
полярность жидк,тем слабее ее смачив
поверх .Чем выше полярность, тем ниже
избир момент.
.Лучше
смачивает данную поверх та жидк, которая
ближе к ней по полярности. Чем выше
полярность жидк,тем слабее ее смачив
поверх .Чем выше полярность, тем ниже
избир момент.
