
- •1. Коллоидная химия. Свойства коллоидных систем. Признаки объектов коллоидной химии.
- •2. Классификация коллоидных систем.
- •5.Очистка коллоидных систем: диализ, ультрафильтрация.
- •7. Поверхностное натяжение. Зависимость поверхностного натяжение от различных факторов. Методы измерения поверхностного натяжения.
- •12. Изотермы адсорбции и поверхностного натяжения растворов пав. Уравнение Шишковского.
- •14. Представления о полимолеку-
- •15. Получение, классификация твердых пористых адсорбентов.
- •16. Понятия о капиллярных явлениях. Теория капиллярной конденсации.
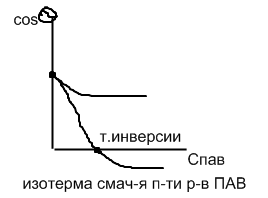
- •20. Избирательное смачивание. Способы определения краевого угла смачивания. Инверсия смачиваемости поверхности.
- •22. Седиментация суспензий и седиментационный анализ дисперсных систем.
- •26. Реологические свойства структурированных жидкообразных и твердообразных систем. Вязкость агрегативно устойчивых дисперсных систем.
- •27 Агрегативная устойчивость дисп сист.Факторы агрег устойчив:
- •30Электрокинетич потенциал.Влияние разл факторов на вел электрокин потенциала.
- •31. Коагуляция дисперсных систем. Факторы, влияющие на электролитную коагуляцию дисперсных систем. Быстрая и медленная коагуляция.
- •39. Пены. Методы получения. Устойчивость и разрушение пен. Практическое значение пен.
- •19Адгезия.Когезия.Смачивание,Краевые углы смачивания и работа адгезии.
16. Понятия о капиллярных явлениях. Теория капиллярной конденсации.
Капиллярные явления наблюдаются в содержащих жидкость капиллярных сосудах, у которых расстояние между стенками капилляра соизмеримо с радиусом кривизны поверхности жидкости. Кривизна возникает в результате взаимодействия жидкости со стенками сосудов (адгезия, смачивание). Специфика поведения жидкости зависит от того, смачивает или нет она стенки сосудов. Рассмотрим положение уровня жидкости в двух капиллярах, один из которых имеет лиофильную поверхность(смачивается жидкостью)
,а другой нет. ΔР стремится растянуть жидкость и поднимает ее в капилляре до тех пор, пока капил.давление не уравновесится с гидростатическим давлением столба жидкости.
Теория капиллярной конденсации. Явления капиллярной конденсации состоит в том, что конденсация пара адсорбции в тонких капиллярах происходит при меньших давлениях, чем давление насыщенного пара над ровной поверхностью, при данной температуре в условиях смачиваемости поверхности пор жидким адсорбатом.
Условия действия капиллярных сил:
смачивание поверхности адсорбента жидкостью, кот. появляется в результате конденсации пара адсорбатом.
наличие пор с удельной поверхностью от 10 до 500 м2/г, что соответствует переходно-пористым адсорбентам(радиус капилляра = радиусу кривизны поверхности)
микропористая структура обеспечвает резкое увеличение адсорбционного потенциала из-за перекрытия поверхностных сил. С увеличением давления газа начинают действовать капиллярные силы. Капиллярная конденсация начинается при определенном заполнении пор адсорбента или при определенном значении пара адсорбата. К этому моменту поверх. энергия практически скомпенсирована в результате полимолекулярной адсорбции, а микропоры заполнены жидким адсорбатом. С увеличением давления газа конденсация происходит и в более крупных порах, радиус мениска жидкости r в которых находится в соответствии с уравнением капил.конденсации Кельвина.
lnP0/P=2σVм/rRT P0/P<<1
при смачивании поверхности конденсация в порах наступает при давлении меньшим, чем Ро.
1.пора конусообразная: конденса-
ция начинается со дна поры, где кривизна наибольшая, по мере заполнения поры радиус увеличи-
вается и давление повышается. Процесс десорбции описывется той же кривой.
2. пора цилиндрическая с открытм концом: конденсация адсорбата идет со дна поры, где кривизна сферическая, т.е.наибольшая. Т.к. пора цилиндрическая она заполняя-
ется при 1-ом значении радиуса мениска, соответствующего опред. давлению Р
3. цилиндрическая пора с 2-мя открытыми концами: конденсация начинается на стенках цилиндра, имеющего кривизну в 2 раза меньшую, чем у сферы того же радиуса. Адсорбция приводит к уменьшению радиуса поры и мгновенному заполнению ее при Рцил., на концах поры образуются мениски, поэтому десорбция начинается при давлении соответствующем большей кривизне сферической, давление открытия поры меньше, чем давление закрытия поры.
17. Основные закономерности адсорбции из растворов неэлектролитов на твердых адсорбентах.Молекулярная адсорбция – адсорбция из растворов неэлектролитов или слабых электролитов. Растворенные вещества адсорбируются на поверхности твердого тела в виде молекул. Особенность: наряду с растворенным веществом адсорбируются молекулы растворителя.
![]() моль/г
моль/г
Адсорбция зависит от:
концентрации адсорбента.
Ур-я Ленгмюра, Фрейндлиха и БЭТ.
природа растворителя.
а) чем хуже адсорбция растворителя, тем лучше адсорбция растворенного вещества.
б) чем лучше в-во (адсорбат) растворяется, тем хуже адсорбируется из данного растворителя.
влияние природы адсорбента.
Подобные адсорбируются на подобном (по полярности).
Влияние природы адсорбата.
а) правило Ребиндера: Процесс адсорбции идет в сторону уравнения полярностей фаз и тем сильнее, чем больше первоначальная разность полярностей адсорбента и растворителя. Если адсорбат – ПАВ, то на поверхности образуется слой, ориентированный определенным образом. Неполярный радикал в сторону неполярной фазы, а полярная группа в сторону полярной.
б) правило Дюкло-Траубе: Адсорбция гомологов возрастает при повышении углеводородного радикала.
18. Основные закономерности адсорбции из растворов электролитов на твердых адсорбентах.Твердые адсорбенты-природные или искусственные материалы с большой наружной или внутренней энергией на которой происходит адсорбция газов или р-ров. Их классификация:
1.По структуре
а) Корпускулярные-это структуры из сросшихся между собой мельчайших, связанных физ. Или хим. Силами (корпускулы)
Синтетические:синтез гидрозоля→коагуляция(гель)→сушка,дробление
Природные: уголь, древесина, картон, кожа, зерна, почва, грунты.
б) Кристаллические цеолиты, амосиликаты - обладающие строго регулярной кристалл. Структурой
в)Губчатые – массивные тела пронизанные порами( активированные угли, никель Рэнея)
2. По полярности
-полярные: бумага, силикагель, алюмогель
-неполярные: угли,сажа
3. Пористость(по размеру пор)
П= Vпор/Vадс
Макропоры(r=100/200 нм) Sуд= 0.2/2 м2/г
Переходно-пористые( r=2/100нм) Sуд=10/500 м2/г
Микропористые r=0.5/2 нм) Sуд=500/1000 м2/г
Основные закономерности заключаются в следующем:
-Поверхность твердого тела, в отличие от поверхности жидкости, имеет сложный неоднородный характер. Даже полированное зеркало имеет на пов-ти выступы размерами до 3*10-7см
- Адсорбция
происходит не на всей пов-ти а, лишь на
активных центрах
Адсорбция
происходит не на всей пов-ти а, лишь на
активных центрах
-Адсорбция кинетически обратима - наряду с адсорбцией газа происходит его десорбция. Адсорбционное равновесие устанавливается очень быстро.
