
- •1. Коллоидная химия. Свойства коллоидных систем. Признаки объектов коллоидной химии.
- •2. Классификация коллоидных систем.
- •5.Очистка коллоидных систем: диализ, ультрафильтрация.
- •7. Поверхностное натяжение. Зависимость поверхностного натяжение от различных факторов. Методы измерения поверхностного натяжения.
- •12. Изотермы адсорбции и поверхностного натяжения растворов пав. Уравнение Шишковского.
- •14. Представления о полимолеку-
- •15. Получение, классификация твердых пористых адсорбентов.
- •16. Понятия о капиллярных явлениях. Теория капиллярной конденсации.
- •20. Избирательное смачивание. Способы определения краевого угла смачивания. Инверсия смачиваемости поверхности.
- •22. Седиментация суспензий и седиментационный анализ дисперсных систем.
- •26. Реологические свойства структурированных жидкообразных и твердообразных систем. Вязкость агрегативно устойчивых дисперсных систем.
- •27 Агрегативная устойчивость дисп сист.Факторы агрег устойчив:
- •30Электрокинетич потенциал.Влияние разл факторов на вел электрокин потенциала.
- •31. Коагуляция дисперсных систем. Факторы, влияющие на электролитную коагуляцию дисперсных систем. Быстрая и медленная коагуляция.
- •39. Пены. Методы получения. Устойчивость и разрушение пен. Практическое значение пен.
- •19Адгезия.Когезия.Смачивание,Краевые углы смачивания и работа адгезии.
5.Очистка коллоидных систем: диализ, ультрафильтрация.
Д ля
очистки коллоидных растворов от
примесей используют такие методы,
как фильтрация, диализ, электродиализ,
ультрафильтрация.Фильтрация
(основана
на способности коллоидных частиц
проходить через поры обычных фильтров.При
этом более крупные частицы
задерживаются.Элементарный процесс
фильтрования может происходить только
при условии, что имеет место разность
давлений жидкости над перегородкой
и под ней. Диализ
-
удаление с помощью мембран низкомолекулярных
соединений из коллоидных растворов
и растворов ВМС. При этом используют
свойство мембран пропускать молекулы
и ионы малого размера и задерживать
коллоидные частицы и макромолекулы.
Жидкость, подвергаемую диализу,
отделяют от чистого растворителя
соответствующей мембраной. Малые
молекулы и ионы диффундируют через
мембрану в растворитель и при его
достаточно частой замене почти
нацело удаляются из диализуемой
жидкости. Проницаемость мембраны для
низкомолекулярных веществ
обусловливается тем, что малые
молекулы и ионы или свободно проходятчерез
капилляры, пронизывающие мембраны,
или растворяются в веществе мембраны.
Электродиализпозволяет
в несколько десятков раз увеличить
скорость диализа низкомолекулярных
электролитов. С этой целью в
диализаторе создают постоянное
электрическое поле с падением
потенциала 20—250 В/см и выше.
Ультрафильтрация
применяется
для очистки систем, содержащих
частицы коллоидных размеров (золи,
растворы ВМС, взвеси бактерий и
вирусов). Суть метода - в продавливании
разделяемой смеси через фильтры с
порами, пропускающими только молекулы
и ионы низкомолекулярных веществ.
ля
очистки коллоидных растворов от
примесей используют такие методы,
как фильтрация, диализ, электродиализ,
ультрафильтрация.Фильтрация
(основана
на способности коллоидных частиц
проходить через поры обычных фильтров.При
этом более крупные частицы
задерживаются.Элементарный процесс
фильтрования может происходить только
при условии, что имеет место разность
давлений жидкости над перегородкой
и под ней. Диализ
-
удаление с помощью мембран низкомолекулярных
соединений из коллоидных растворов
и растворов ВМС. При этом используют
свойство мембран пропускать молекулы
и ионы малого размера и задерживать
коллоидные частицы и макромолекулы.
Жидкость, подвергаемую диализу,
отделяют от чистого растворителя
соответствующей мембраной. Малые
молекулы и ионы диффундируют через
мембрану в растворитель и при его
достаточно частой замене почти
нацело удаляются из диализуемой
жидкости. Проницаемость мембраны для
низкомолекулярных веществ
обусловливается тем, что малые
молекулы и ионы или свободно проходятчерез
капилляры, пронизывающие мембраны,
или растворяются в веществе мембраны.
Электродиализпозволяет
в несколько десятков раз увеличить
скорость диализа низкомолекулярных
электролитов. С этой целью в
диализаторе создают постоянное
электрическое поле с падением
потенциала 20—250 В/см и выше.
Ультрафильтрация
применяется
для очистки систем, содержащих
частицы коллоидных размеров (золи,
растворы ВМС, взвеси бактерий и
вирусов). Суть метода - в продавливании
разделяемой смеси через фильтры с
порами, пропускающими только молекулы
и ионы низкомолекулярных веществ.
6. Межмолекулярное взаимодействие. Молекулярные силы (силы Ван-дер-Ваальса).Межмолекулярное взаимодействие может иметь разный характер:
1)Химические связи. Образуются путем перекрывания электронных орбиталей и потому сугубо специфичны.
2)Водородные связи возникают между молекулами, содержащими функциональную группу OH (кислоты, щелочи, вода, спирты).
3) Силы Ван-дер-Ваальса. Молекулярные связи, которые действуют между любыми молекулами. К этим силам относят:
а) ориентационные – возникают между полярными молекулами в результате взаимодействия дипольных моментов. Из-за диполь-дипольного взаимодействия молекулы приобретают определенную ориентацию относительно друг друга.
б) индукционные – у полярных и неполярных молекул. Диполь-неполярные молекулы возникают в электрическом поле ил под действием поля полярной молекулы.
в) дисперсионные силы действуют между всеми молекулами и возникают из-за непрерывного движения электронов в атомах, приводящего к образованию мгновенных диполей. Электрическое поле мгновенного диполя 1-ого атома индуцирует дипольный момент другого атома, что приводит к возникновению сил притяжения.
7. Поверхностное натяжение. Зависимость поверхностного натяжение от различных факторов. Методы измерения поверхностного натяжения.
Пов.нат. – работа обратимого изотермич. обр-я ед пов-ти.
Ф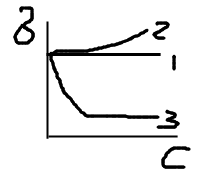 акторы:
1) температура: с ув-емT
пов.нат. уменьшается: усиливается
тепловое дв-е мол-л, кот.ведет к ослаблению
межмол. вз-я => ум-ся внутр.давл =>
ум-ся пов.нат.
акторы:
1) температура: с ув-емT
пов.нат. уменьшается: усиливается
тепловое дв-е мол-л, кот.ведет к ослаблению
межмол. вз-я => ум-ся внутр.давл =>
ум-ся пов.нат.
2) природа фазы: чем больше межмол. вз-е внутри фазы, тем больше пов.нат на границе раздела фаз. 3) природа граничащих фаз: чем больше межмол. вз-е между контактирующими фазам, тем меньше пов.нат на границе раздела этих фаз. Если жид. Раств-ся друг в друге, то пов.нат на границу ж1/ж2 приблизит-но равны разности пов.нат взаимно насыщ.жид-й на границе с возд. 4) влияние добавок: 1.ПНАВ; 2.ПИВ (р-ры электролитов, кот. в воде дисс-ют с обр-ем ионов, ионы гидротируются, т.к. Епол/н2о>Eн2о/н2о, поэтому ионы интенсивно втяг-ся вглубь р-ра и әσ/әТ>0. 3.ПАВ(мол-лы с несимметрич.дефильным строением из непол. УВ-рад и пол группы)
Методы определения:
1) статч: осн. на изуч. утстойч. равновес. сост, к кот.самопроизв.приз.сист. 1.метод капиллярного поднятия (рис+формула) 2. м.висячей или лежачей капли: осн.на изуч-и формы капель в поле силы тяж. Ведется учет отклон-я их формы от сферич. (рис) 3. м.уравновеш-я пластинки: толщ.d закр.на коромысле весов погруж.в исслед.жид.,кот.хорошо.смач.её пов-ть. σ=F/2d.
2 )полустатич: осн.на изуч.усл,при кот сист.теряет равновесие. 1. метод наиб.давл.в пузырьке газа σ =1/2ΔPmax*r0(рис)
2. метод отрыва кольца σ=F/4πr*K (рис)
3. сталагмометрич: осн.на опред.веса капель,отрыв.под дейст.силы тяж. в момент отрыва капли её вес уравновеш.силами пов.нат, умнож.на её капилляры. Р=2πr0σ/K (рис)
3) днамческие: метод колеблющихся струй: изуч.св-ва поверх.жид.через малые пром-ки врем после их образ-я. С пом-ю эллиптич.отв-я образ.струю в фотрме эллиптич.цил. под д-ем сил пов.нат.,кот стрем.придать ф-му цил и инерц-х сил устан поперечное колебструи.
8. Внутренняя поверхностная энергия. Поверхностная энергия – это избыток энергии в тонком слое вещества у поверхности соприкосновения фаз по сравнению с энергией вещества внутри фазы. Полная поверхностная энергия складыва-
ется из работы образования поверхности, т.е. работы, необхо-димой для преодаления сил межмолекулярного взаимодейст-вия при перемещении молекул из объема фазы в поверхностный слой, и теплового эффекта, связанного с этим процессом. В соответствии с термодинамическими зависимостями удельная полная п.э. равна:
dU=- T (∂σ/∂T)+σ/ при V=const
уравнение Гиббса-Гельмгольца.
σ уменьшается линейно с ростом Т. И в линейной области ∂σ/∂T = const, ∂2σ/∂T2=0, дифференциальное уравнение по Т дает: ∂U/∂T=∂σ/∂T-∂σ/∂T-Т(∂2σ/∂T2), ∂U/∂T=0.
Таким образом, величина U является температурным инвариантом. Благодаря этому свойству удельная поверхностная энергия – одна из важнейших характеристик межмолекулярных сил в чистых жидкостях.
9. Физическая адсорбция и хемосорбция. Количественные характеристики адсорбции.Адсорбция – процесс самопроизвольного изменения концентрации компонентов системы между поверхностным слоем и объемной фазой. В зависимости от характера сил, действующих между частицами адсорбата и адсорбента, различают физическую и химическую (хемосорбцию). Физическая адсорбция происходит под влиянием сил Ван-дер-Ваальса и по своей природе аналогична процессам конденсации паров адсорбата. Хемосорбция обусловлена перекрыванием электронных орбиталей частиц адсорбата и адсорбента, т.е. вызывается их химическим взаимодействием. Теплота хемосорбции соизмерима с теплотами химических реакций. Хемосорбция необратима, физическая обратима. Физическая малоспецифична, химическая специфична (адсорбция происходит, только если возможна хим. реакция). Физ. адсорбция сопровождается образованием полислоев, химическая монослойна.
Количественные характеристики:
а - Абсолютная адсорбция.
Число моль или грамм адсорбата, приходящиеся на единицу поверхности или массы адсорбента.
г – Избыточная (Гиббсова) адсорбция.
Избыток адсорбата в поверхностном слое по сравнению с его количеством в таком же объеме фазы, приходящейся на единицу поверхности, или массы адсорбента.
10.Адсорбция паров и газов на однородной поверхности. Изотерма адсорбции Ленгмюра.Основные положения теории Ленгмюра, которая описывает данный вид адсорбции:
1.Адсорбция мономолекулярна
2.Адсорбция локализована
3.Энергетическая однородность пов-ти(все центры адсорбции обладают равной энергией и адсорбированные молекулы не взаимодействуют друг с другом)
Ур-е Ленгмюра Г=Г∞bc/1+bc, изотерму рисуем сами.
11ПАВ и ПИВ.Поверхн активность.Прав Дюкло-Траубе.Ур-ие Гиббса.ПИВ-это растворы электролитов,котор в воде диссоц с образованием ионов, ионы в свою очередь гидротир, поэтому ионы интенсивно втягив вглубь р-ра,что получ >0.ПАВ-орган молек с несимметр дефильным строением сост из неполярного углевод радикала и полярной группы.Правило Д-Т:С увелич длины углеводородного радикалана одну группу СН2 поверх активность растет в гомологич ряду в 3-3,5 раза.
![]() =3-3,5.Г
бесконечность одинак потому, что
опред величина одной группы.
=3-3,5.Г
бесконечность одинак потому, что
опред величина одной группы.
Ур-ие
Гиббса
![]() .
.
