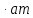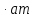- •2.Анализ свариваемости металлов на основе диаграмм состояния сплавов
- •3.Диффузионные процессы при сварке плавлением и сварке давлением
- •4. Особенности образования неразъемных соединений пластмасс
- •5. Формирование неразъемных соединений в процессах пайки
- •6. Образование неразъемных соединений посредством склеивания
- •6.1. Механизм адгезии
- •6.2. Выбор клея
- •6.3. Подготовка поверхности склеиваемых материалов
- •6.4. Образование соединения
- •6.5. Факторы, влияющие на прочность соединения
- •6.7. Склеивание пластических масс
3.Диффузионные процессы при сварке плавлением и сварке давлением
Диффузия в металлах и сплавах — это элементарные процессы перемещения атомов кристаллического вещества на расстояние больше параметра кристаллической решетки.
Наиболее вероятный механизм диффузии связан с перемещением атомов по незанятым узловым положениям — вакансиям (рис. 3.1, а) или междуузлиям (рис. 3.1, б). В сумме такие элементарные процессы перемещения определяют массоперенос. Если массоперенос направленный и приводит к местным изменениям концентрации перемещающихся атомов элемента, растворенного в растворителе, процесс называют гетеродиффузией, если имеет место перемещение атомов металла основного компонента без изменения концентрации, процесс называют самодиффузией.
Как самодиффузия, так и гетеродиффузия имеют большое значение для большинства процессов изменения состояния металлов, влияющих на свойства. Фазовые и структурные превращения при нагреве и охлаждении, получение того или иного структурного состояния металла и, соответственно, его свойства связаны с протеканием диффузионных процессов. Даже образование мартенсита при закалке, считающееся бездиффузионным превращением, зависит от однородности твердого раствора перед закалкой, которая определяется диффузией растворенных элементов.

Рис.3.1. Схемы механизма перемещения атомов при диффузии
Очень большое значение процессы диффузии имеют при сварке. Например, при сварке давлением диффузия является основным процессом, определяющим рекристаллизацию и улучшение свойств сварного соединения после установления связи между свариваемыми активированными поверхностями.
При сварке плавлением процессы диффузии влияют на степень химической и механической неоднородности металла шва и сварного соединения. Особенно большое значение процессы гетеродиффузии имеют для формирования сварных соединений разнородных сталей и разнородных металлов, так как обычные закономерности диффузионного процесса осложняются специфическими условиями диффузии — реакционной диффузией и диффузией, вызванной влиянием состава на изменение термодинамической активности растворенного и диффундирующего вещества.
3.1. Основные закономерности диффузии
Основной параметр диффузии — скорость переноса массы перемещающегося элемента, металла через единицу площади сечения за единицу времени. Основной причиной перемещения растворенного вещества служат разность его концентраций в соседних объемах и стремление к равномерному распределению. В этом случае масса М перемещающегося вещества пропорциональна разности концентраций dс и обратно пропорциональна интервалу расстояния dх, на котором имеет место градиент концентрации dс/dx:
М = —Ddс/dх. (3.1)
Коэффициент пропорциональности: D — коэффициент диффузии характеризует количество вещества в граммах или молях, перемещающегося через единицу площади за единицу времени при градиенте концентрации, равном единице. Знак минус показывает, что диффузия идет в направлении уменьшения градиента концентрации dс/dх.
Выражение (3.1) характеризует первый закон диффузии (первый закон Фика), связывающий массоперенос с перепадом концентрации диффундирующего элемента. Коэффициент диффузии — очень важный показатель данного процесса. При определенной температуре он зависит в основном от природы растворителя и диффундирующего вещества. Зная, например, коэффициенты диффузии различных элементов в α и γ-Fе, можно судить о способности соответствующих растворов к гомогенизации или, наоборот, к гетерогенизации во время пребывания при той или иной температуре, что имеет значение для регулирования параметров термообработки, и, следовательно, свойств, химической и механической неоднородности сварных соединений.
Особенно сильно коэффициент диффузии зависит от температуры:
D = D0 е—Q/(RT) (3.2)
или
LnD = LnD0 — Q/(RT) ), (3.3)
где D0 — предэкспоненциальный множитель; Q — энергия активации диффузии; R — газовая постоянная; Т — температура.
Предэкспоненциальный множитель зависит от типа кристаллической решетки
D0 = Qa2/(Nh), (3.4)
где а — межатомное расстояние; N — число Авогадро; h — постоянная Планка.
Энергия активации диффузии зависит от энергии связи диффундирующего атома в решетке растворителя. Чем выше Q, тем сильнее удерживается атом в первоначальной позиции, тем ниже D и меньше скорость диффузии.
По мере протекания процесса диффузии разность концентраций растворенного, диффундирующего вещества уменьшается и меняется градиент концентрации dс/dx. Это изменение градиента концентрации со временем τучитывается вторым законом диффузии (второй закон Фика), который для одноосного потока имеет вид
 (x,t)=
C0
(x,t)=
C0 (3.5)
(3.5)

где C0 — исходная концентрация; Ф—функция Крампа, значение которой находят по таблицам в зависимости от величины аргумента x/(2Dτ).
Выражение (3.5) служит для определения коэффициента диффузии при разных температурах на основе экспериментально установленных значений с0, с и x за время τ . При этом все рассмотренные закономерности справедливы для протекания процессов диффузии при концентрациях, не достигающих предела насыщения растворенного элемента.
Зная
коэффициент диффузии D
и продолжительность процесса τ,
по выражению
 =
=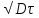 . можно приближенно оценить размер
диффузионной зоны для данного элемента
и растворителя. Это выражение показывает,
что графически зависимостьx
= f (τ) является параболической, что
позволяет судить о характере
рассматриваемых процессов и оценивать
роль диффузии в их протекании.
. можно приближенно оценить размер
диффузионной зоны для данного элемента
и растворителя. Это выражение показывает,
что графически зависимостьx
= f (τ) является параболической, что
позволяет судить о характере
рассматриваемых процессов и оценивать
роль диффузии в их протекании.
Для состояния и свойств сварных соединений, прежде всего сталей, имеет значение диффузионное перемещение углерода, водорода, серы, фосфора, железа, марганца, хрома, молибдена, ванадия, алюминия и некоторых других элементов, Диффузия этих элементов определяет степень химической и механической неоднородности сварных соединений, протекание процессов рекристаллизации, изменение свойств при термообработке и т. п.
В процессе диффузии перемещение атомов внедрения и атомов замещения происходит по-разному, характеризуется различными энергетическими параметрами и протекает с различной скоростью.
Небольшие по размеру атомы внедрения значительно отличаются от параметров решетки и размеров атомов растворителя, они удерживаются в своих положениях менее устойчиво, чем находящиеся в узлах атомы замещения. Кроме того, чем меньше размер внедренного атома, чем больше он отличается от атома растворителя, тем слабее он удерживается в кристаллической решетке и тем меньше его энергия активации диффузии и больше скорость диффузии (табл. 4.1).
Таблица 4.1
|
Элемент |
Н |
N |
C |
B |
Fe- |
|
Атомный диаметр d , 10-8 м. |
0,56 |
1,02 |
1,14 |
1,78 |
1,26 |
|
Отклонение, d - dFe , 10-8 м. |
-0,7 |
-0,24 |
-0,12 |
+0,52 |
0 |
|
Q, кал./г.ат |
3 750 |
18 200 |
20 100 |
21 160 |
|
Значения энергии активации диффузии некоторых элементов в γ-Fе, дающих растворы замещения, приведены ниже:
|
Элемент |
S |
А1 |
Мо |
Сu |
Мn |
N |
Fe |
С |
W |
Сг |
|
Q,
кал/г х 103 (в
|
28,8
|
44
|
77
|
61
|
66, 4
|
67,5
|
68
|
87
|
90
|
97
|
Наибольшей подвижностью обладают атомы серы, что создает предпосылки для устранения при нагреве ликвации по сере. Наиболее трудно устраняется химическая неоднородность по хрому и вольфраму. Диффузия углерода и легирующих элементов в α- и γ-Fе идет с различной скоростью. В α-Fе энергия активации диффузии углерода меньше, а скорость диффузии больше:
|
Элемент |
С |
Fе |
Мо |
W |
Сг |
|
Q
(в α - Fе),
кал/г |
18 100 |
59 000 |
65000 |
70 000 |
82 000 |
|
Q(в
γ - Fе),
кал/г
|
36 000
|
68 000
|
77 000
|
78 000
|
97 000
|
Повышенная скорость диффузии в α -Fе создает предпосылки для активного протекания процессов при температуре нагрева несколько ниже Ас1. что может иметь место при эксплуатации сварных соединений теплоэнергетического оборудования, химической и нефтеперерабатывающей промышленности, работающего частов интервале температур 500 —650 °С, а также при термообработке сварных соединений в режиме высокого отпуска.

Рис. 3.2. Зависимость коэффициента диффузии углерода в α -Fе от температуры

Рис. 3.3. Влияние легирования α -Fе на коэффициент диффузии углерода при температуре 700 °С
Для сварных соединений важно, что по границам зерен диффузионные процессы идут активнее, чем по телу зерна, что связано с большей плотностью несовершенств кристаллического строения по границам зерен. В результате этого сосредоточение по границам зерен различного рода примесей и, прежде всего, углерода, водорода и серы определяет возможность значительного изменения свойств металла этих зон, их поведения при деформации и разрушении. Состояние границ зерен для сварных соединений имеет большее значение, чем для свариваемого металла в связи с наличием крупных литых кристаллов в металле шва и выросшего зерна в околошовной зоне.
Поскольку процесс диффузии связан с энергетическими характеристиками взаимодействия диффундирующего атома с решеткой растворителя, большое влияние на процесс оказывают температура и состояние решетки растворителя — наличие в ней инородных атомов — атомов легирующих элементов. Таким образом, скорость диффузии какого-либо элемента в легированной стали зависит от характера и степени ее легирования. Несомненно, имеет значение и концентрация атомов диффундирующего элемента.
Зависимость скорости диффузии от температуры — степенная (рис. 4.2), Влияние легирования α -Fе на коэффициент диффузии углерода при температуре 700 °С показано на рис. 4.3.
3.2. Диффузионные процессы при сварке
Рассмотренные закономерности диффузии относились к случаю перемещения растворенных атомов в однородном твердом растворе при наличии градиента их концентрации, т. е. в твердом состоянии металлы А и Б неограниченно растворимы друг в друге(рис. 3.4, а). При контактировании — сварке таких металлов в твердом состоянии при температуре ^ распределение концентраций после нагрева в течение какого-то времени будет описываться графиком на рис. 3.4, а, II. Изменение концентрации А в Б и Б в А будет зависеть от температуры и продолжительности нагрева и характеризоваться параболическим законом.
Диффузию, сопровождающуюся фазовыми изменениями, называют реактивной. Для этой диффузии характерно образование зон неизменной концентрации — зон химических соединений. В сварном соединении эти зоны не обязательно должны располагаться в плоскости контактирования свариваемых металлов. Они могут быть сосредоточены в участке с соответствующей концентрацией компонентов в зависимости от относительной скорости диффузии при данной температуре. Последующий нагрев (термообработка), приводящий к дальнейшему развитию диффузионного процесса, сместит положение этих зон.
Для сварных соединений характерен еще один вид диффузии, когда процесс перемещения в растворе какого-либо элемента происходит не в связи с разностью его концентраций в растворе, а в связи с разницей его термодинамической активности: например, диффузия углерода на границе сварки легированной и нелегированной сталей или разнолегированных сталей. При исследовании такой диффузии и вызываемой ею неоднородности состава и строения сварных соединений было замечено, что если сварное соединение состоит из сталей с различным содержанием легирующих элементов, то независимо от содержания в этих сталях углерода направление его перемещения определяется разницей в легировании контактирующих сталей. Перемещение углерода при этом может происходить даже из стали с меньшей его концентрацией (рис. 4.5). Было также замечено, что кремний является элементом, «выталкивающим» углерод, а хром, молибден и ванадий «притягивающими» его,
Предложенная трактовка механизма такого действия легирующих элементов сводится к следующему. Если у атомов легирующего элемента силы связи с атомами углерода меньше, чем у атомов железа, то атомы углерода отталкиваются от атомов такого элемента и стремятся попасть в окружение только атомов железа. Следовательно, данный легирующий элемент увеличивает термодинамическую активность атомов углерода к перемещению в участки, не содержащие атомов этого легирующего элемента.

Рис. 3.5. Образование обезуглероженной и науглероженной зон в сварном соединении в связи с диффузией углерода, вызванной различием его термодинамической активности в свариваемых сталях
К элементам, увеличивающим термодинамическую активность углерода в железе, относятся кремний и никель.
С
другой стороны, в растворе
 -
или
-
или -Fе,
где имеются атомы легирующего элемента
со сродством к углероду большим, чем у
железа, углерод стремится закрепиться
у этих атомов и его активность к
перемещению понизится. Понижают
термодинамическую активность углерода
в железе атомы карбидообразующих
элементов (марганец, хром, молибден,
вольфрам, ванадий и др.).
-Fе,
где имеются атомы легирующего элемента
со сродством к углероду большим, чем у
железа, углерод стремится закрепиться
у этих атомов и его активность к
перемещению понизится. Понижают
термодинамическую активность углерода
в железе атомы карбидообразующих
элементов (марганец, хром, молибден,
вольфрам, ванадий и др.).
Количество вещества, перемещающегося в связи с разностью его термодинамической активности в растворе, определяется выражением
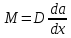 (3.6)
(3.6)
где
 — градиент термодинамической
активности.
— градиент термодинамической
активности.
Таким
образом, по показателю термодинамической
активности углерода в
 -
или
-
или -Fе
можно судить о склонности сварного
соединения к образованию структурной
неоднородности на границе раздела в
связи с диффузией углерода из стали с
большей активностью углерода в сталь
с его меньшей активностью.
-Fе
можно судить о склонности сварного
соединения к образованию структурной
неоднородности на границе раздела в
связи с диффузией углерода из стали с
большей активностью углерода в сталь
с его меньшей активностью.
Несколько подробнее следует остановиться на значении диффузии водорода в сплавы, и особенно в сварные соединения. Водородимеет наименьший атомный размер и способен быстрее всех других элементов проникать в кристаллические решетки металлов и перемещаться в их решетках. Это наглядно видно на примере диффузии водорода в железе по тому, что водрод имеет самую низкую энергию активации диффузии. Столь большая подвижность водорода и малый атомный размер приводит к тому, что в металл быстро проникает и растворяется большое количество водорода.
На многие свойства технических металлов, таких например . как сталь и сплавы титана, водород оказывает вредное влияние. Водород способен сильно увеличивать хрупкость и хладноломкость, склонность к замедленному разрушению, а тем самым, к образованию холодных трещин в сварных соединениях. При повышении температурах водород вызывает обезуглероживание стали, разлагая карбид железа (Fe3C+ 4H = 3Fe+CH4). В реакцию при этом вступает диффундирующий или растворенный атомарный водород. При обезуглероживании понижается прочность стали, а образующийся метан создает в микро- и макропустотах высокое давление, способствуя появлению очагов разрушения.
Хотя механизм вредного влияния водорода на свойства сталей и других металлов изучали многие исследователи, существо явления до сих пор нельзя признать полностью ясным. Водород в стали образует раствор внедрения. Атомы внедрения, скапливаясь около несовершенств кристаллического строения — дислокаций, уменьшают их подвижность, способствуют их скоплению и тем самым с одной стороны, уменьшают способность металла к общей и локальной пластической деформации, а с другой — способствуют образованию зародышевых трещин в местах скопления дислокаций. Активность проявления такого охрупчивающего действия водорода увеличивается при наличии других факторов, благоприятствующих хрупкому разрушению — низкой температуры, скорости иагружения, сложно-напряженного состояния, наличия концентраторов напряжений.
Отмечается и другое вредное влияние водорода в металлах. Атомы водорода, быстро проникая в металл и попадая в микро- и макропустоты — поры, несплошности в виде плен и закатов, зоны строчечных неметаллических включений — ассоциируют там в молекулы. Молекула не способна к дальнейшему перемещению. Таким образом, скапливаясь в пустотах, молекулы водорода создают местные, очень высокие давления, приводящие к вздутию металла, сильному расслоению и образованию трещин.
Водород может оказывать большое влияние на свойства сварных соединений. При дуговых методах сварки плавлением имеются разные источники попадания водорода в металл шва; влага из электродных покрытий и флюсов, органические составляющие электродных покрытий, окалина на кромках свариваемого металла и электродной проволоке и т. п. Поэтому металл шва часто содержит значительные количества водорода, превышающие количество водорода в свариваемом металле. Содержание водорода в металле шва сталей доходит до 30 см3/100 г, в то время, как в деформированной стали оно обычно не превышает 8—10 см3/100 г. Повышенному количеству водорода в металле сварного шва способствует его меньшая плотность — наличие большего количества пор. В то же время, при надлежащих мерах предосторожности — просушке электродов и флюсов, очистке проволоки и кромок, использовании низководородных электродных покрытий и т. п. металл шва практически не наводороживается.
Высокая скорость диффузии водорода способствует обогащению водородом околошовной зоны в процессе сварки стали. С одной стороны, это может вызываться перемещением водорода из свариваемой стали в околошовную зону, где в связи с повышением температуры значительно увеличивается растворимость водорода. С другой стороны, водород поступает в околошовную зону из металла шва, если его там содержится больше, чем в свариваемой стали. Обогащение околошовной зоны водородом повышает ее хрупкость и снижает способность к локальной пластической деформации. Поэтому водород способствует повышению склонности к образованию холодных трещин.



 -Fe)
-Fe)