
- •Министерство образования и науки рф
- •Предмет коллоидной химии
- •Глава I.Дисперсные системы:
- •1.1 Основные свойства дисперсных систем
- •1.2 Классификация дисперсных систем
- •Классификация по степени дисперсности
- •Классификация по агрегатному состоянию
- •Классификация по структурно-механическим свойствам
- •Раздел II. Поверхностные явления. Адсорбция
- •2.1 Классификация поверхностных явлений
- •Классификация поверхностных явлений
- •2.2 Поверхностное явление – адсорбция
- •2.2.1 Основные понятия и определения
- •2.2.2 Адсорбция на границе жидкость-газ
- •2.2.3. Адсорбция на твердом адсорбенте
- •2.3 Адгезия и смачивание
- •Раздел III. Электрические свойства дисперсных
- •3.1 Возникновение электрического заряда
- •3.2 Современные представления о строении
- •3.3Строение мицеллы гидрофобного золя
- •3.4. Факторы, влияющие на электрокинетический потенциал
- •3.4.1 Влияние температуры
- •3.4.2 Влияние электролитов
- •3.4.3 Влияние рН среды
- •3.4.4 Влияние природы дисперсионной среды
- •3.5 Электрокинетические явления
- •3.5.1 Электрофорез
- •3.5.2 Потенциал седиментации
- •3.5.3 Электроосмос
- •3.5.4 Потенциал течения
- •Раздел IV. Устойчивость и нарушение устойчивости лиофобных золей
- •4.1. Седиментационная устойчивость
- •4.2 Агрегативная устойчивость и коагуляция
- •4.2.1 Теория устойчивости гидрофобных золей длфо
- •4.2.2 Факторы, определяющие агрегативную устойчивость
- •4.3. Коагуляция гидрофобных дисперсных систем
- •4.3.1 Коагуляция золей электролитами
- •Явление неправильных рядов
- •4.3.2 Кинетика коагуляции
- •Теория быстрой коагуляции Смолуховского
- •Константа скорости медленной коагуляции
- •Раздел V. Оптические свойства дисперсных систем
- •5.1. Рассеяние света
- •Теория светорассеяния Рэлея
- •5.2. Поглощение света и окраска золей
- •5.3. Оптические методы исследования коллоидных растворов
- •Раздел VI. Молекулярно-кинетические свойства
- •6.1. Броуновское движение
- •6.2. Диффузия
- •6.3. Осмос
- •Раздел VII. Виды дисперсных систем
- •7.1. Растворы высокомолекулярных соединений (вмс)
- •7.1.1. Классификация вмс
- •7.1.2. Особенности строения полимеров
- •7.1.3. Набухание вмс
- •Термодинамика набухания
- •Кинетика набухания
- •Факторы, влияющие на набухание
- •7.1.4. Свойства растворов вмс
- •7.2. Коллоидные пав. Мицеллообразование в растворах пав
- •Применение коллоидных пав
- •7.3. Эмульсии
- •7.3.1. Классификация эмульсий
- •7.3.2. Методы получения эмульсий
- •7.3.3. Устойчивость эмульсий
- •Типы эмульгаторов
- •7.3.4. Применение эмульсий
- •7.4. Пены
- •7.4.1. Основные характеристики и классификация пен
- •7.4.2. Устойчивость пен
- •7.4.3. Методы разрушения пен
- •7.4.4. Практическое применение пен
- •7.5. Золи и суспензии
- •7.6. Порошки
- •7.6.1. Основные свойства и устойчивость порошков
- •7.6.2. Практическое применение порошков
- •Раздел VIII. Структурообразование в дисперсных системах
- •8.1. Типы структур в дисперсных системах
- •8.2. Особенности структурообразования в растворах вмс. Студни и студнеобразование
2.2.3. Адсорбция на твердом адсорбенте
Особенности адсорбции на твердом адсорбенте
Адсорбция происходит на межфазной поверхности газ-твердое тело, жидкость-твердое тело.
В отличие от жидкой твердая поверхность
энергетически и геометрически неоднородна.
Кроме того, твердые адсорбенты могут
иметь поры.Наличие
пор приводит к тому, что адсорбция
сопровождается капиллярной
конденсацией.
отличие от жидкой твердая поверхность
энергетически и геометрически неоднородна.
Кроме того, твердые адсорбенты могут
иметь поры.Наличие
пор приводит к тому, что адсорбция
сопровождается капиллярной
конденсацией.
Рассмотрим сечение зерна адсорбента (рис. 14).
А
Рис. 14.
Сечение зерна
адсорбента
Внутри фазы все силы уравновешены. На поверхности раздела фаз пространственная симметрия сил межмолекулярного взаимодействия отсутствует. Поэтому в пиках нескомпенсированная энергия максимальна.
Адсорбция на твердом адсорбенте протекает в две стадии:
диффузионная – диффузия вещества к поверхности адсорбента;
собственно адсорбция.
Лимитирующей стадией, определяющей скорость всего процесса, является диффузионная. Поэтому важный фактор – перемешивание.
Вследствие геометрической неровности поверхности адсорбента величину адсорбции определяют как количество адсорбата, отнесенное к единице массы адсорбента
![]() ,
моль/кг.
,
моль/кг.
Характеристика твердых адсорбентов.
Требования, предъявляемые к адсорбентам
В качестве адсорбентов наиболее часто применяют углеродные сорбенты (древесный или костный уголь, графитированная термическая сажа ГТС), бентонитовые глины, силикагель, цеолиты и др.
Углеродные сорбентыполучают из всевозможного сырья, которое при определенных условиях может давать твердый углеродный остаток – ископаемых углей, торфа, древесины, ореховой скорлупы, фруктовых косточек и животных костей. Лучшими считаются угли, полученные из скорлупы кокосовых орехов и абрикосовых косточек.
Для повышения адсорбционной способности углеродных сорбентов их дополнительно активируют, выдерживая при повышенной температуре в присутствии паров воды и углекислого газа. В процессе активации выгорает смола, заполняющая поры углей, удельная поверхность адсорбента, а следовательно, и его адсорбционная способность, возрастают.
Удельная поверхность активированного угля, включая поверхность всех его пор, может достигать 1000 м2/г.
Углеродные сорбенты применяют для очистки воды, пищевых масс; очистки и разделения газов; в медицине.
Силикагельполучают высушиванием студня поликремниевой кислоты; по химическому составу – этоSiO2. Выпускается в виде пористых крупинок, удельная поверхность составляет ~ 500 м2/г.
Бентониты– предварительно активированные кислотой глины, применяют для очистки сиропов, соков, растительных масел.
Пористые стеклаполучают при удалении из стекол щелочных и щелочноземельных металлов.
Цеолиты(в переводе с греческого «кипящий камень» из-за способности вспучиваться при нагревании) – природные и синтетические алюмосиликатные материалы. Кристаллическая структура их образована тетраэдрами [SiO4]4–и [AlO4]5–, объединенными общими вершинами в трехмерный каркас, пронизанный полостями и каналами, в которых находятся молекулы воды и катионы металловI,IIгрупп.
Цеолиты проявляют адсорбционные свойства после удаления воды из их полостей (при нагревании). Цеолиты различных разновидностей имеют строго определенный размер входов в полости и каналы. Поэтому их называют еще «молекулярными ситами» за способность сорбировать лишь определенные компоненты.
Используются для выделения и очистки углеводородов нефти; очистки, осушки и разделения газов (в т.ч. воздуха); осушки фреонов; извлечения радиоактивных элементов.
Твердые адсорбенты бывают пористыеинепористые.
Пористость адсорбентаопределяется отношением суммарного объема порVпк общему объему адсорбентаVадс
П = Vп/ Vадс.
В зависимости от размера пор различают макропористые, мезопористые и микропористые адсорбенты.
Т а б л и ц а 3
|
Тип адсорбента |
Диаметр пор, нм |
Удельная поверхность, м2/кг |
Примеры |
|
Непористые |
– |
1-500 |
Цемент, бетон |
|
Пористые |
|
|
|
|
– макропористые |
>4,0 |
500-2000 |
Асбест, мука, древесина, |
|
– мезопористые |
1,2-4,0 |
|
Бентониты, силикагель |
|
– микропористые |
<1,2 |
>4,0·105 |
Активированный уголь, цеолиты, пористые стекла |
Пористость адсорбента имеет большое значение для адсорбции: чем она выше, тем больше удельная поверхность и выше адсорбционная способность. Однако это справедливо только в том случае, если молекулы адсорбата невелики и легко могут проникать в поры, т.е. соизмеримы с размером пор.
Различают полярные (гидрофильные) и неполярные (гидрофобные) адсорбенты.
Полярные(хорошо смачиваются водой) – силикагель, цеолит, глины, пористое стекло; неполярные(водой не смачиваются) – активированный уголь, графит, тальк, парафин.
Требования, предъявляемые к адсорбентам:
большая удельная поверхность (достигается за счет измельчения, активирования поверхности, нанесения тонкого слоя адсорбента на пористую поверхность (керамику, кирпич));
механическая прочность, термическая и химическая устойчивость;
низкая себестоимость;
возможность регенерации.
Правила подбора адсорбентов
При выборе адсорбента необходимо определить тип адсорбируемого вещества (полярное, неполярное, ПАВ). Полярные адсорбенты не следует применять при адсорбции из водных растворов, т.к. они могут адсорбировать растворитель – воду. Их целесообразно использовать при адсорбции из неводных растворов.
Неполярные адсорбенты хорошо адсорбируют из водных сред.
Дифильные молекулы могут адсорбироваться на любом адсорбенте. При этом они ориентируются своими полярными группами в полярную среду, неполярными – в неполярную (рис. 15).

Образовавшийся адсорбционный слой может изменить характер поверхности. Например, адсорбция дифильных молекул из водного раствора приводит к гидрофилизацииповерхности угля, вследствие чего уголь приобретает способность смачиваться водой.
Эффект Ребиндера: при адсорбции ПАВ разность полярностей между адсорбентом и растворителем уменьшается.
Степень разделения растворенного вещества и растворителя тем выше, чем больше разница в полярности.
При выборе адсорбента необходимо учитывать размеры молекул адсорбтива: диаметр пор должен превышать диаметр молекул.
Основные теории адсорбции на твердых адсорбентах
Все теории разработаны для адсорбции газов и паров твердыми телами, поскольку система твердое тело-газ состоит всего из двух компонентов и поэтому удобна для теоретического рассмотрения явления адсорбции.
В 1915 году Ленгмюром и Поляни одновременно и независимо были созданы две совершенно различные теории адсорбции газов на твердом теле.
Основные положения теории мономолекулярной адсорбции Ленгмюра.
При разработке теории мономолекулярной адсорбции газа на твердом адсорбенте Ленгмюр исходил из следующих допущений.
1. Адсорбция происходит не на всей свободной поверхности адсорбента, а на активных центрах, характеризующихся максимальной свободной энергией (при адсорбции на границе жидкость-газ все активные центры в энергетическом отношении одинаковы) (рис. 16).
2 .
Адсорбция локализована на отдельных
адсорбционных центрах (молекулы не
перемещаются по поверхности).
.
Адсорбция локализована на отдельных
адсорбционных центрах (молекулы не
перемещаются по поверхности).
3. Вследствие малого радиуса действия адсорбционных сил каждый активный центр, адсорбируя молекулу адсорбата, ста-
новится уже неспособным к дальнейшей адсорбции (молекулы, ударяющиеся об адсорбированные молекулы, отражаются без задержки).
4. Взаимодействием между молекулами адсорбата можно пренебречь.
5. В системе устанавливается динамическое равновесие, т.е. скорость адсорбции равна скорости десорбции.
Уравнение Ленгмюра для описания адсорбции газа твердой поверхностью
![]() .
.
Уравнение Ленгмюра можно использовать только при отсутствии адсорбции сверх мономолекулярного слоя.
П
Рис. 17.
s-образная
изотерма адсорбции
В связи с необходимостью объяснения характера таких изотерм возникла потребность в других теориях.
Основные положения теории полимолекулярной адсорбции Поляни.
1. Адсорбция обусловлена только физическими силами.
2. На поверхности адсорбента нет активных центров, а адсорбционные силы исходят от всей поверхности адсорбента и образуют около нее непрерывное силовое поле.
3
Рис.
18.
Схема полимолекулярной
адсорбции
по теории
Поляни .
Адсорбционные силы действуют на
достаточно больших расстояниях,
превышающих размеры отдельных молекул
адсорбтива, и поэтому можно говорить о
существовании у поверхности адсорбента
адсорбционного объема, который заполняется
молекулами адсорбтива (рис. 18).
.
Адсорбционные силы действуют на
достаточно больших расстояниях,
превышающих размеры отдельных молекул
адсорбтива, и поэтому можно говорить о
существовании у поверхности адсорбента
адсорбционного объема, который заполняется
молекулами адсорбтива (рис. 18).
4. Действие адсорбционных сил по мере удаления от поверхности уменьшается и на некотором расстоянии становится равным нулю.
5. Под воздействием адсорбционного поля возникает возможность образования нескольких слоев молекул адсорбата. Наибольшее притяжение и сжатие испытывает первый адсорбционный слой; газообразные продукты в нем конденсируются в жидкость.
6. Притяжение данной молекулы поверхностью адсорбента не зависит от наличия в адсорбционном пространстве других молекул.
7. Адсорбционные силы не зависят от температуры и, следовательно, с изменением температуры адсорбционный объем не изменяется.
Теория полимолекулярной адсорбции Поляни позволяет описать адсорбцию на пористых адсорбентах и качественно объяснить характер s-образной изотермы. Главный недостаток теории Поляни – отсутствие аналитического выражения изотермы адсорбции.
Основные положения теории полимолекулярной адсорбции БЭТ.
Брунауэр, Эммет и Теллер разработали теорию применительно к адсорбции паров. Эта теория получила название теории БЭТ по первым буквам фамилий авторов.
1. Адсорбция осуществляется под действием сил Ван-дер-Ваальса.
2. Нескомпенсированная поверхностная энергия неравномерно распределена по поверхности адсорбента. На поверхности имеются активные центры с большой концентрацией энергии.
3. Все активные центры поверхности занимают частицы адсорбата, образуя первый слой. Каждая молекула первого слоя представляет собой активный центр для дальнейшей адсорбции, что приводит к образованию второго, третьего и т. д. слоев. При этом построение последующих слоев возможно при незаполненном первом (рис. 19).
4 .
Взаимодействием соседних адсорбированных
молекул в рамках одного слоя пренебрегают;
.
Взаимодействием соседних адсорбированных
молекул в рамках одного слоя пренебрегают;
5. Существует динамическое равновесие адсорбция десорбция.
Теория БЭТ объясняет s-образную изотерму адсорбции.
Кроме того, было получено уравнение, описывающее изотерму адсорбции, названное уравнением полимолекулярной адсорбции БЭТ:
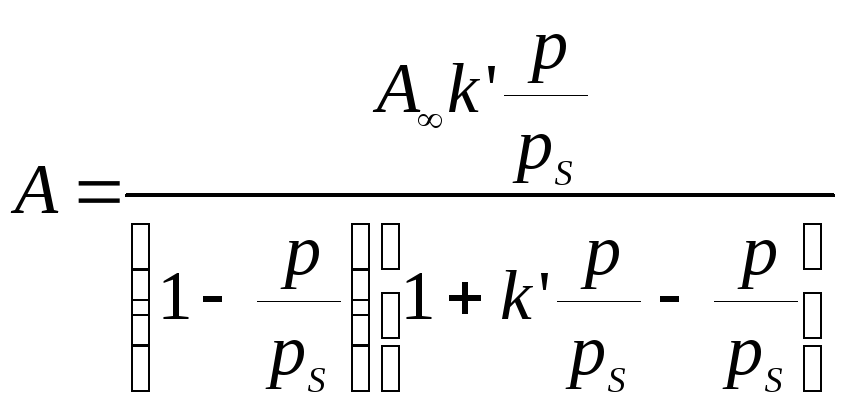 ,
,
где рs– давление насыщенного пара при данной температуре; р/рs– относительное давление пара;
![]() ,
,
kр – константа адсорбционного равновесия для первого слоя; kL – константа конденсации пара.
При малых относительных давлениях (р/рs << 1 и p << ps) уравнение БЭТ превращается в уравнение мономолекулярной адсорбции Ленгмюра.
Уравнение Фрейндлиха
На практике часто для аналитического описания зависимости адсорбции на твердом адсорбенте от концентрации адсорбтива применяется эмпирическое уравнение Фрейндлиха:
![]() – для адсорбции газа;
– для адсорбции газа;
![]() – для адсорбции из раствора,
– для адсорбции из раствора,
где β, n– эмпирические коэффициенты, зависящие от природы адсорбтива и температуры.
Уравнение Фрейндлиха представляет собой уравнение параболы, поэтому оно описывает не всю изотерму адсорбции, а только ее криволинейный участок.
П остоянные
уравнения Фрейндлиха определяются на
основе опытных данных. Для этого уравнение
Фрейндлиха приводят к линейному виду
(логарифмируют):
остоянные
уравнения Фрейндлиха определяются на
основе опытных данных. Для этого уравнение
Фрейндлиха приводят к линейному виду
(логарифмируют):
![]()
и строят график в координатах lnA = f(lnр), который представляет собой прямую (рис. 20). Тангенс угла наклона равенn, а отрезок, отсекаемый прямой на оси ординат, –lnp.
Уравнение Фрейндлиха – эмпирическое уравнение. Поэтому его можно применять для расчета величины адсорбции в том диапазоне равновесных концентраций, для которого найдены значения констант и n.
Преимущество – простота в использовании, поэтому часто применяется в инженерных расчетах.
Капиллярная конденсация
П ри
давлении, равном давлению насыщенного
парарs,
начинается капиллярная
конденсация.
ри
давлении, равном давлению насыщенного
парарs,
начинается капиллярная
конденсация.
Процесс сорбции паров твердыми пористыми адсорбентами включает 2 стадии.
П
Рис. 21. Капиллярная
конденсация
смачивает поверхность твердого тела, поверхность жидкости на границе с паром образует вогнутый мениск (рис. 21).
Известно, что давление насыщенного пара над вогнутой поверхностью (с радиусом кривизны r) жидкости меньше давления пара над плоской поверхностью (радиус кривизны равен ).
В результате пар, который над плоской поверхностью является насыщенным, оказывается пересыщенным при контакте с вогнутой поверхностью жидкости и конденсируется.
На второй стадии идет заполнение капилляров жидкостью – капиллярная конденсация. Внешне это проявляется как резкое увеличение адсорбции при давлении рs (рис. 22).
С вязь
между радиусом сферического мениска и
давлением насыщенного пара при температуреТнад мениском выражается уравнением
Томсона (Кельвина):
вязь
между радиусом сферического мениска и
давлением насыщенного пара при температуреТнад мениском выражается уравнением
Томсона (Кельвина):
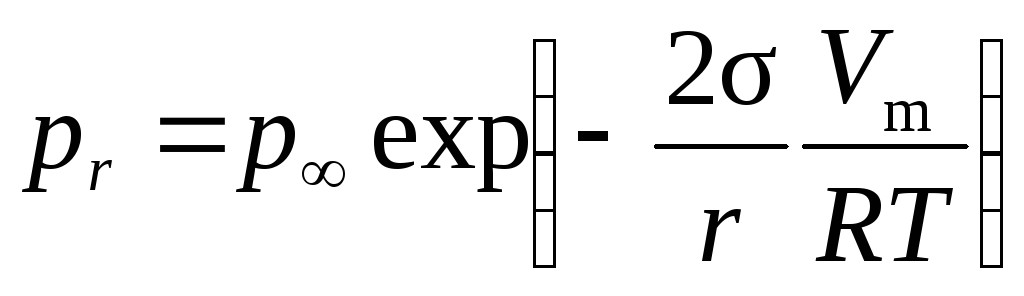
где рr– давление насыщенного пара над вогнутым мениском с радиусом кривизныr;р – давление насыщенного пара над плоской поверхностью (радиус кривизны плоской поверхности равен бесконечности); σ – поверх-
ностное натяжение жидкости; r– радиус кривизны вогнутого мениска;Vm– мольный объем жидкости;R– универсальная газовая постоянная.
Уравнение Томсона-Кельвина является основным при расчетах, связанных с явлением капиллярной конденсации. Зная давления рrир, можно вычислить максимальный радиус капилляров, в которых будет происходить конденсация. Эти данные необходимы для правильного подбора адсорбента.
Капиллярная конденсация – вторичное явление. Она происходит не под действием адсорбционных сил, а под действием сил притяжения пара к вогнутому мениску жидкости.
Капиллярная конденсация происходит обычно довольно быстро, завершаясь в несколько минут.
На практике явление адсорбции, сопровождающееся капиллярной конденсацией, применяют в процессе рекуперации, т.е. улавливания и возвращения в производство летучих растворителей. Например, при получении пектина (который широко применяется в пищевой промышленности) из свекловичного жома используется этиловый спирт. В ходе производственных операций испаряется ~ 2 л этанола в расчете на 1 кг пектина. Для избежания потерь спирта воздух, насыщенный парами этанола, пропускают через слой пористого адсорбента – активированного угля, в капиллярах которого сначала идет адсорбция, а затем капиллярная конденсация спирта. После насыщения адсорбента через него пропускают горячий водяной пар, в результате чего происходит испарение и десорбция спирта, и водно-спиртовую паровую смесь конденсируют в холодильнике.
Ионная адсорбция из растворов
Ионная адсорбция — адсорбция из растворов сильных электролитов. В этом случае растворенное вещество адсорбируется в виде ионов.
Ионная адсорбция является более сложным процессом по сравнению с молекулярной адсорбцией, так как в растворе присутствуют уже частицы как минимум 3 видов: катионы, анионы растворенного вещества и молекулы растворителя.
Ионная адсорбция имеет ряд особенностей.
1 Адсорбируются заряженные частицы (ионы), а не молекулы;
Адсорбция происходит только на полярных адсорбентах, часто ее так и называют – полярная адсорбция;
Адсорбция сопровождается образованием двойного электрического слоя (ДЭС);
Адсорбция является избирательной, т. е. на данном адсорбенте катионы и анионы адсорбируются неодинаково.
В основе ионной адсорбции лежат химические силы, и она чаще всего кинетически необратима;
Для ионной адсорбции характерно явление обменной адсорбции.
На ионную адсорбцию влияет рядфактров.
1 Химическая природа адсорбента
Чем более полярным является адсорбент, тем лучше он адсорбирует ионы из водных растворов. На активных центрах, несущих положительный заряд, адсорбируются анионы, на отрицательных – катионы.
2. Химическая природа ионов
а) На адсорбцию ионов большое влияние оказывает величина радиуса иона. Чем больше кристаллический радиус иона при одинаковом заряде, тем лучше он адсорбируется, так как с увеличением кристаллического радиуса иона возрастает его поляризуемость, а следовательно, способность притягиваться к полярной поверхности — адсорбироваться на ней. Одновременно увеличение кристаллического радиуса приводит к уменьшению гидратации иона, а это облегчает адсорбцию, В соответствии с этим ионы можно расположить в ряды по возрастающей способности к адсорбции, называемые лиотропными рядами:
Li+ < Na+ < К+ < Rb+ < Cs+
Mg2+ < Ca2+ < Sr2+ < Ba2+
Сl– < Br– < NQ3– < I– < NCS–.
а дсорбционная
способность возрастает
дсорбционная
способность возрастает
б) Чем больше заряд иона, тем сильнее ион притягивается противоположно заряженной поверхностью твердого тела, тем сильнее адсорбция:
К+ << Са2+ << А13+ << Th4+.
у силение
адсорбции
силение
адсорбции
Особый интерес для коллоидной химии представляет адсорбция ионов поверхностью кристалла, в состав которого входят такие же или родственные ионы. В этом случае адсорбцию можно рассматривать как кристаизацию, т.е. достройку кристаллической решетки способными адсорбироваться на ней ионами. Это позволило Панету и Фаянсу сформулировать следующее правило:
На кристаллической поверхности адсорбируются ионы, которые способны достраивать кристаллическую решетку и дают труднорастворимое соединение с ионами, входящими в кристалл.
Так, если мы имеем кристалл хлорида серебра nAgCl, а в растворе ионы К+ и Сl–, то адсорбироваться на кристалле будут ионы Сl–.
Ионообменная адсорбция
Ионообменная адсорбция — это процесс, при котором твердый адсорбент обменивает свои ионы на ионы того же знака из жидкого раствора.
Твердый адсорбент, практически нерастворимый в воде поглощает из раствора ионы одного заряда (катионы или анионы) и вместо них отдает в раствор эквивалентное число других ионов того же заряда. Такой обменный ионный процесс аналогичен обменным химическим реакциям, но только протекает на поверхности твердой фазы.
Ионообменная адсорбция имеет следующие особенности:
специфична, т. е. к обмену способны только определенные ионы;
не всегда обратима;
протекает более медленно, чем молекулярная адсорбция;
может приводить к изменению рН среды.
Вещества, проявляющие способность к ионному обмену, называются ионитами. В зависимости от того, какой вид ионов участвует в обмене, иониты подразделяются на катиониты и аниониты. Катиониты способны обменивать катионы, в т. ч. ион Н+, аниониты – анионы, в т. ч. ион ОН–. Существуют также амфолиты, которые в зависимости от условий способны проявлять как катионообменные, так и анионообменные свойства.
Иониты имеют структуру в виде каркаса, «сшитого», обычно, ковалентными связями. Каркас имеет положительный или отрицательный заряд, скомпенсированный противоположным зарядом подвижных ионов (противоионов), которые могут легко заменяться на другие ионы с зарядом того же знака. Каркас выступает в роли полииона и обусловливает нерастворимость ионита в растворителях.
Различают природные и синтетические иониты. Природные: алюмосиликатные материалы – гидрослюда, цеолиты и т.д. Синтетические: ионообменные смолы, сульфитированные угли, ионообменные целлюлозы.
Ионный обмен широко применяется в различных отраслях промышленности. Иониты применяют для очистки сточных вод, умягчения и обессоливания воды, при производстве сахара, молока (для изменения его солевого состава), вина (для предотвращения помутнения и понижения кислотности).
