
- •Министерство образования и науки рф
- •Предмет коллоидной химии
- •Глава I.Дисперсные системы:
- •1.1 Основные свойства дисперсных систем
- •1.2 Классификация дисперсных систем
- •Классификация по степени дисперсности
- •Классификация по агрегатному состоянию
- •Классификация по структурно-механическим свойствам
- •Раздел II. Поверхностные явления. Адсорбция
- •2.1 Классификация поверхностных явлений
- •Классификация поверхностных явлений
- •2.2 Поверхностное явление – адсорбция
- •2.2.1 Основные понятия и определения
- •2.2.2 Адсорбция на границе жидкость-газ
- •2.2.3. Адсорбция на твердом адсорбенте
- •2.3 Адгезия и смачивание
- •Раздел III. Электрические свойства дисперсных
- •3.1 Возникновение электрического заряда
- •3.2 Современные представления о строении
- •3.3Строение мицеллы гидрофобного золя
- •3.4. Факторы, влияющие на электрокинетический потенциал
- •3.4.1 Влияние температуры
- •3.4.2 Влияние электролитов
- •3.4.3 Влияние рН среды
- •3.4.4 Влияние природы дисперсионной среды
- •3.5 Электрокинетические явления
- •3.5.1 Электрофорез
- •3.5.2 Потенциал седиментации
- •3.5.3 Электроосмос
- •3.5.4 Потенциал течения
- •Раздел IV. Устойчивость и нарушение устойчивости лиофобных золей
- •4.1. Седиментационная устойчивость
- •4.2 Агрегативная устойчивость и коагуляция
- •4.2.1 Теория устойчивости гидрофобных золей длфо
- •4.2.2 Факторы, определяющие агрегативную устойчивость
- •4.3. Коагуляция гидрофобных дисперсных систем
- •4.3.1 Коагуляция золей электролитами
- •Явление неправильных рядов
- •4.3.2 Кинетика коагуляции
- •Теория быстрой коагуляции Смолуховского
- •Константа скорости медленной коагуляции
- •Раздел V. Оптические свойства дисперсных систем
- •5.1. Рассеяние света
- •Теория светорассеяния Рэлея
- •5.2. Поглощение света и окраска золей
- •5.3. Оптические методы исследования коллоидных растворов
- •Раздел VI. Молекулярно-кинетические свойства
- •6.1. Броуновское движение
- •6.2. Диффузия
- •6.3. Осмос
- •Раздел VII. Виды дисперсных систем
- •7.1. Растворы высокомолекулярных соединений (вмс)
- •7.1.1. Классификация вмс
- •7.1.2. Особенности строения полимеров
- •7.1.3. Набухание вмс
- •Термодинамика набухания
- •Кинетика набухания
- •Факторы, влияющие на набухание
- •7.1.4. Свойства растворов вмс
- •7.2. Коллоидные пав. Мицеллообразование в растворах пав
- •Применение коллоидных пав
- •7.3. Эмульсии
- •7.3.1. Классификация эмульсий
- •7.3.2. Методы получения эмульсий
- •7.3.3. Устойчивость эмульсий
- •Типы эмульгаторов
- •7.3.4. Применение эмульсий
- •7.4. Пены
- •7.4.1. Основные характеристики и классификация пен
- •7.4.2. Устойчивость пен
- •7.4.3. Методы разрушения пен
- •7.4.4. Практическое применение пен
- •7.5. Золи и суспензии
- •7.6. Порошки
- •7.6.1. Основные свойства и устойчивость порошков
- •7.6.2. Практическое применение порошков
- •Раздел VIII. Структурообразование в дисперсных системах
- •8.1. Типы структур в дисперсных системах
- •8.2. Особенности структурообразования в растворах вмс. Студни и студнеобразование
3.4.3 Влияние рН среды
Введение в золь ионов Н+и ОН-может сильно сказываться на величине-потенциала, так как эти ионы обладают высокой сорбционной способностью: первые – благодаря малому радиусу, что позволяет им близко подходить к поверхности твердой фазы, вторые – из-за большого дипольного момента (большой поляризуемости).
3.4.4 Влияние природы дисперсионной среды
Дисперсионная среда обычно характеризуется двумя величинами: диэлектрической проницаемостью и вязкостью.
-потенциал частиц золя тем больше, чем больше (полярность растворителя).
Чем больше вязкость, тем толще слой дисперсионной среды, который прилипает к частице при разрыве мицеллы и, следовательно, тем меньше численное значение -потенциала.
3.5 Электрокинетические явления
Электрокинетические явления – это явления, которые возникают при воздействии электрического поля на дисперсную систему (электрофорез, электроосмос), а также в результате перемещения частиц дисперсной фазы или дисперсионной среды (потенциал протекания, потенциал оседания).
Несмотря на различие электрокинетических явлений, все они связаны с наличием ДЭС на частицах дисперсной фазы. Интенсивность всех электрокинетических явлений определяется значением -потенциала.
3.5.1 Электрофорез
Электрофорез– направленное движение частиц дисперсной фазы относительно дисперсионной среды под действием внешнего электрического поля.
При наложении внешнего электрического поля происходит разрыв мицеллы: частицы дисперсной фазы вместе с адсорбированными на них потенциалопределяющими ионами и противоионами адсорбционного слоя перемещаются к электроду, знак которого противоположен знаку заряда коллоидной частицы (-потенциалу), а противоионы диффузионного слоя – к другому электроду. Например, если дисперсная фаза заряжена отрицательно, коллоидные частицы движутся к аноду (положительному электроду), а положительно заряженные противоионы диффузного слоя – к катоду (рис. 32).
Е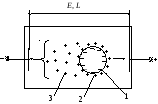 сли
дисперсная фаза заряжена положительно,
направление движения частиц меняется
на противоположное.
сли
дисперсная фаза заряжена положительно,
направление движения частиц меняется
на противоположное.
С
Рис 32.
Схема движения коллоидной частицы и
противоионов при электрофорезе: 1 –
потенциалопределяющие ионы, 2 –
противоионы адсорбционного слоя, 3 –
противоионы диффузионного слоя
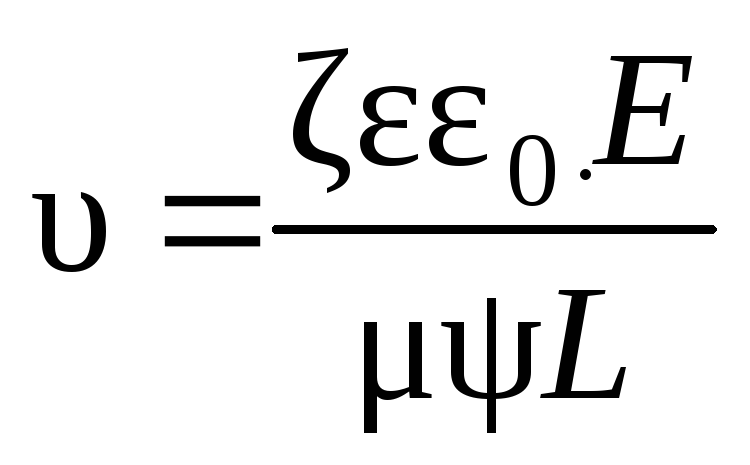 ,
,
где – электрофоретическая скорость;– электрокинетический потенциал;– диэлектрическая проницаемость среды;0– электрическая постоянная,0 = 8,8510-12Кл/(Вм);Е– разность потенциалов внешнего электрического поля;L– расстояние между электродами;E/L=H –напряженность, или градиент, внешнего электрического поля;– динамическая вязкость сплошной среды;– фактор формы.
Коэффициент учитывает форму частиц и их ориентацию в электрическом поле. Для шарообразных частиц коэффициент равен 0,66, а для цилиндрических, ориентированных вдоль силовых линий электрического поля – 1.
Скорость движения в расчете на единицу напряженности электрического поля Нназываетсяэлектрофоретической подвижностью
![]() .
.
Электрофоретическая подвижность зависит только от свойств дисперсной фазы и дисперсионной среды.
На подвижность коллоидной частицы оказывают влияние электрофоретический и релаксационный эффекты.
Электрофоретический эффект(эффект торможения): под действием внешнего электрического поля противоионы передвигаются в направлении, противоположном движению частицы. За счет гидратации противоионы увлекают за собой и окружающую их жидкость (дисперсионную среду). Это приводит к тому, что частица перемещаются в направлении, противоположном движению жидкости, скорость ее уменьшается.
Релаксационный эффектвызывается нарушением симметрии ДЭС вокруг частицы при ее движении. ДЭС деформируется и отстает от частицы. В результате возникает добавочное электрическое поле, которое действует на частицу, стремясь двигать ее в обратном направлении, и тем самым влияет на скорость электрофореза.
Для учета влияния этих факторов в уравнение для расчета электрофоретической скорости и вводится коэффициент .
Применение электрофореза.
1. Метод электрофореза широко используется для определения -потенциала. Для этого измеряют электрофоретическую скорость при известной напряженности электрического поля.
Н аиболее
простой метод – метод подвижной границы,
в котором скорость движения частиц при
электрофорезе оценивают по перемещению
границы между прозрачной контактной
жидкостью и окрашенным золем (рис. 33).
При этом полагают, что все частицы
движутся с одинаковой скоростью.
Контактная жидкость представляет собой
дисперсионную среду данного золя.
аиболее
простой метод – метод подвижной границы,
в котором скорость движения частиц при
электрофорезе оценивают по перемещению
границы между прозрачной контактной
жидкостью и окрашенным золем (рис. 33).
При этом полагают, что все частицы
движутся с одинаковой скоростью.
Контактная жидкость представляет собой
дисперсионную среду данного золя.
Э
Рис. 33. Определение
-потенциала
методом
электрофореза: 1 – золь,
2
– контактная жидкость
![]() .
.
Зная скорость перемещения частиц и свойства дисперсионной среды (и), рассчитывают-потенциал.
2. Разделение белков и других высокомолекулярных соединений, биологически активных веществ на фракции.
3. Нанесение ровных, тонких, прочных покрытий на металлические поверхности любой формы.
4. В медицине – для разделения и анализа белков, введения лекарственных препаратов. На кожу пациента накладывают тампон, смоченный раствором лекарственного препарата, а сверху помещают электроды, к которым приложен низкий потенциал. В ходе этой процедуры частички лекарственного препарата под действием электрического поля переходят в ткани организма человека.
