
Химия учеб посрбие
.pdf
Химическая связь, осуществляемая за счет образования общей или поделенной пары или нескольких пар электронов, называется ковалентной. В 1916 г. Льюис предложил механизм возникновения химической связи между взаимодействующими атомами. В образовании одной общей пары электронов каждый атом вносит по одному электрону, то есть участвует в равной доле.
.. .. .. ..
:Cl. + .Cl:
.. ..
. .
:N. + .N: →
. .
SiCl4;
:Cl : Ñl : → неподеленная пара электронов
.. ..
общая поделенная пара электронов
:N: : :N:
N≡ N
тройная связь |
|
|
|
|
.. |
|
|
|
:Cl: |
|
Cl |
.. |
: |
.. |
| |
: Cl : Si : Cl: → |
Cl — Si — Cl |
||
.. |
: .. |
| |
|
|
:Cl: |
|
Ñl |
|
.. |
|
|
d = 0 — дипольный момент; эти соединения неполярные
— гомеополярные.
Ковалентность определяется числом непарных электронов в атоме или числом общих пар, окружающих данный атом в молекуле соединения. Ковалентность для хлора — 1, для азота
— 3, для кремния — 4.
Ковалентная связь проявляется при образовании молекул элементарных веществ (H2, Cl2, O2, F2, N2) и тех сложных веществ, которые расположены близко друг к другу в периодической системе (ClF, BrCl, SiC).
Недостаток теории Льюиса в том, что она не все могла объяснить и носит односторонний характер. Проблема химической связи получила дальнейшее развитие в работах Гейтлера, Лондона, Полинга, Гунда и др.
Химическая связь и волновые свойства электрона
— 31 —
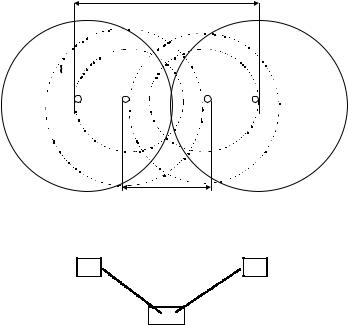
Важнейшими количественными характеристиками химической связи являются энергия связи и длина связи — расстояние между центрами двух ядер в молекуле.
Легче изучить Н2. При возникновении химической связи в молекуле Н2 происходит перекрывание электронных облаков с образованием молекулярного электронного облака, сопровождающееся выигрышем энергии.
Молекулярное электронное облако располагается между центрами обоих ядер и обладает повышенной электронной плотностью по сравнению с плотностью атомного электронного облака.
Для молекулы водорода энергия связи составляет около 103 ккал/моль = 430,9 кДж/моль, а длина связи 0,74 А°:
1,06А°
Н |
Н |
0,74А°
Эта величина совпадает с экспериментальными данными:
H |
H2 |
H |
↑ |
|
↓ |
атомная |
|
атомная |
орбиталь |
|
орбиталь |
↑↓ |
молекулярная
орбиталь
Å1 > Å2 < Å1 — образование молекулы с энергией связи Å2 сопровождается выделением энергии.
— 32 —

Анализ квантомеханической задачи взаимодействия двух атомов водорода показывает, что осуществление ковалентной связи возможно лишь в случае антипараллельных спинов непарных электронов, принадлежащих различным атомам. При параллельных спинах электронов атомы не притягиваются, а отталкиваются; ковалентная связь не осуществляется. Соединиться в молекулу водорода могут только два атома с антипараллельными спинами непарных электронов, так как валентность водорода равна единице.
Валентность углерода по отношению к водороду равна 4, и атом углерода может присоединить максимально 4 атома водорода, насыщая полностью свои валентности.
Возбуждение электрона возможно, если в данном уровне имеются незанятые энергетические состояния. Возбуждение требует затраты энергии и не всегда осуществимо.
Возбуждение электрона достигается переводом его с одного подуровня на другой в пределах одного и того же уровня за счет затраты энергии извне.
Электронные конфигурации:
|
Нормальное |
|
|
|
|
Возбужденное |
|
|||||||
|
состояние |
|
|
n = 2 |
|
|
состояние |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S |
|
P |
|
|
|
|
S |
|
|
P |
|
|
|
|
|
|
|
|
|
|
Ne |
|
|
|
|
|
|
|
Ne |
↑↓ |
↑↓ |
↑↓ |
↑↓ |
|
|
↑↓ |
|
↓↑ |
↑↓ |
|
↓↑ |
Вал. = 0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
F |
↑↓ |
↑↓ |
↑↓ |
↑ |
|
|
F |
↑↓ |
|
↑↓ |
↑↓ |
|
↑ |
Вал.= 1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
↑↓ |
↑↓ |
↑ |
↑ |
|
|
O |
↑↓ |
|
↑↓ |
↑ |
|
↑ |
Вал. = 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вал. = 5,3 |
N |
↑↓ |
↑ |
↑ |
↑ |
|
|
N |
↑↓ |
|
↑ |
↑ |
|
↑ |
|
C |
↑↓ |
↑ |
↑ |
|
s2p2→ |
sp3 |
C |
↑ |
|
↑ |
↑ |
|
↑ |
Вал. = 2,4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
B |
↑↓ |
↑ |
|
|
s2p → |
sp2 |
B |
↑ |
|
↑ |
↑ |
|
|
Вал. = 1,3 |
|
|
|
|
|
s2 → |
|
|
|
|
|
|
|
|
Вал. = 1,2 |
Be |
↑↓ |
|
|
|
sp |
Be |
↑ |
|
↑ |
|
|
|
||
Li |
↑ |
|
|
|
|
|
Li |
↑ |
|
|
|
|
|
Вал. = 1 |
Электронные и химические аналоги F и Сl:
Атом фтора |
Атом хлора |
— 33 —

|
|
n =2 |
|
|
|
|
|
|
n = 3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
s |
|
|
p |
|
|
s |
|
p |
|
|
|
d |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вал. = 1 |
↑↓ |
↑↓ |
|
↑↓ |
↑ |
|
↑↓ |
↑↓ |
↑↓ |
↑ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Возбуждение |
|
|
↑↓ |
↑↓ |
↑ |
↑ |
↑ |
|
|
|
|
Вал. = 3 |
|||
невозможно |
|
|
|
|
|
|
|
|
|
|
|
Вал. = 5 |
|||
|
|
↑↓ |
↑ |
↑ |
↑ |
↑ |
↑ |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вал. = 7 |
|
|
|
|
|
|
↑ |
↑ |
↑ |
↑ |
↑ |
↑ |
↑ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HOCl — хлорноватистая кислота;
HClO2 — хлористая кислота;
HClO3 — хлорноватая кислота;
HClO4 — хлорная кислота.
Энергия химической связи
При образовании молекулы вещества из свободных атомов выделяемая энергия называется атомарной энергией образования молекул (êêàë/ìîëü, êÄæ/ìîëü).
Для двухатомных молекул:
Í + Í = Í : Í + 103,2 êêàë/ìîëü (+431,72 êÄæ/ìîëü).
103,2 ккал/моль есть энергия химической связи Н : Н. SiCl4, CH4 — средняя энергия химической связи.
Ñ + 4Í → CH4 + 3924 ,8 êêàë/ìîëü = 98,2 êêàë/ìîëü =
= + 1643,47 êÄæ/ìîëü = 410,9 êÄæ/ìîëü.
4
Повышение энергии с повышением кратности не пропорционально увеличению числа связей.
Í |
Í |
Í |
|
Í |
|
| |
85 êêàë | |
| |
145 êêàë |
| |
|
Í — Ñ |
— Ñ — Í |
Ñ |
= |
Ñ |
|
| |
| |
| |
|
| |
+198 êêàë |
Í |
Í |
Í |
|
Í Í — Ñ ≡ Ñ — Í |
|
|
Направленность химической |
связи |
|
||
— 34 —
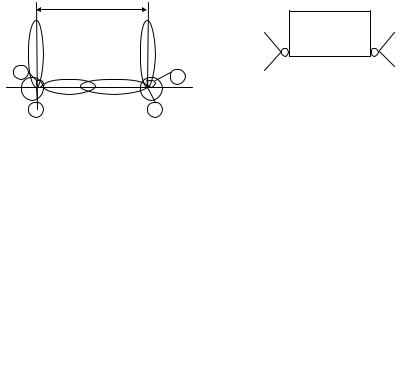
Ковалентная химическая связь возникает в направлении максимального перекрывания электронных облаков взаимодействующих атомов. Направленность — это одно из важнейших свойств ковалентной связи, зависящее от типа взаимодействующих электронов и числа атомов.
Если в химической связи данного атома участвуют несколько электронов разного типа, то возникает гибридная связь.
|
Типы молекул на примере некоторых соединений. |
|
||||
|
У этилена есть σ - è π -связь; π -связь менее прочная, чем |
|||||
σ -связь |
π |
|
|
π |
|
|
|
|
|
|
|
||
|
|
p |
|
p |
Н |
H |
|
|
|
|
|
δ |
|
Н |
|
σ |
Н |
Н |
H |
H |
|
|
р |
р |
|
|
|
|
H |
|
|
H |
|
|
Перекрывание облаков происходит в двух взаимно перпендикулярных направлениях. Связь, действующая в направлении, перпендикулярном к осям ð-электронных облаков, называется
π -связью:
Молекулы, в которых «центры тяжести» положительных зарядов ядер и отрицательных зарядов электронов совпадают в одной точке, называются неполярными, дипольный момент d = 0. У этих атомов одинаковая электроотрицательность (ЭО). Если соединяющиеся атомы обладают различной ЭО, то электронное
— 35 —

облако, находящееся между ними, смещается из симметрического положения ближе к атому с наибольшей электроотрицательностью. Смещение электронного облака называется поляризацией. Центры тяжести положительных и отрицательных зарядов в молекуле не совпадают в одной точке, между ними возникает некоторое расстояние (L — длина диполя), такие молекулы называются полярными èëè дипольными, а связь между ними называется полярной — это разновидность ковалентной связи, претерпевшей незначительную одностороннюю поляризацию.
Для оценки полярности молекул пользуются постоянным дипольным моментом:
|
|
|
µ = å . L(Ä), |
ãäå Ä |
— |
дебаи, меняются от 0 до 10; |
|
å |
— |
заряд; |
|
L — |
расстояние; |
||
L = 0, µ |
= 0 — у неполярных молекул; |
||
L > 0, µ |
> 0 — у полярных молекул. |
||
У атомов с большой разницей ЭО явная односторонняя поляризация, электронное облако смещено в сторону с наибольшей ЭО, это равносильно переходу электрона с атома на атом, а атомы переходят в противоположно заряженные ионы, и возникает ионная молекула. Ковалентная связь становится ионной, дипольный момент возрастает до 10 дебаев. Электроассиметрия возрастает, L увеличивается.
|
e→ |
|
|
|
+ − |
|
+ F → |
Na + + F − → |
|||
|
|||||
Na |
Na F |
||||
кулоновские силы
Химическая связь, возникающая за счет перехода электронов от атома к атому, называется ионной èëè электровалентной связью.
Электровалентность определяется числом электронов, теряемых или приобретаемых каждым атомом. Электроположительная валентность свойственна атомам металлов (восстановителей), отдающим электроны. Электроотрицательная валентность свойственна атомам (окислителям), принимающим электроны.
— 36 —
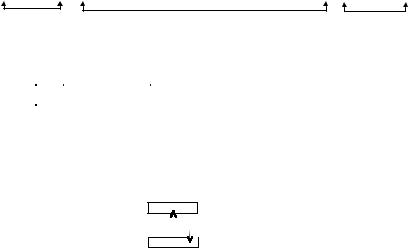
Молекулы химических соединений, возникающие за счет электровалентной связи, называются ионными èëè гетерополярными (гетерос — различный).
Из изложенного выше следует, что природа химической связи едина; принципиального различия в механизме возникновения ковалентной, полярной и ионной связей нет!
Эти виды связи отличаются лишь степенью поляризации электронного облака молекулы. Возникающие молекулы отлича- ются длинами диполей и величинами постоянных дипольных моментов.
Неполярные молекулы: Н2, ÑÍ4; полярные молекулы: CO, HJ, H2S, NH3, H2O, AsF3; ионные молекулы: KCl, NaJ.
Возрастание односторонней поляризации
µ = 0 |
0,11; |
0,38; |
0,93; |
1,43; |
1,84; |
2,6 |
3,5 10Д |
H2, CH4 |
CO |
HJ |
H2S |
NH3 |
H2O |
AsF3 |
KCl NaJ |
Чем выше дипольный момент, тем выше реакционная способность молекул.
Î2 — молекула кислорода, трехэлектронная связь. s p
↑↓ |
↑↓ |
↑ |
↑ |
Раньше считали, что О2 имеет две связи; из ð-электронов
—îäíà σ - и другая π -связь.
Âнастоящее время
.. . ...
:Î. .Î: = :ΗÎ:
. .. ...
одна ковалентная
è äâå
 трехэлектронные связи
трехэлектронные связи
Непарные электроны обуславливают парамагнетизм кисло-
ðîäà.
Трехэлектронные связи в молекулах окиси азота и окиси хлора:
... |
... |
:N = O: |
:Cl = O: |
|
.. |
Энергетически эти связи более выгодны, чем π -связь.
— 37 —

Донорно-акцепторная связь проявляется при взаимодействии, когда есть неподеленная пара электронов и свободная орбиталь.
Компонент А, предоставляющий неподеленную пару электронов, называется донором, а компонент В, предоставляющий свободную орбиталь, — акцептором.
Схема образования донорно-акцепторной связи (1893 г., швейцарский химик Вернер) такова:
À: + Â = À : Â
Вследствие вовлечения в координационную связь неподеленных пар электронов и свободных орбиталей число химических связей превышает число возможной максимальной валентности.
Комплексообразователями могут быть положительно заряженные ионы металлов (Ag+, Cu+2, Co+3, Ni+2, Fe+2, Pt+2), нейтральные атомы (Cr, Fe, Mn, Re, Mo и др.), атомы неметаллов в различной положительной степенью окисления (B+3, Si+4, P+5, S+6, J+7) и, реже, отрицательные ионы (J-1, S-2).
Лигандами являются отрицательно заряженные ионы OH–, Cl– F–, NO −2 , CN–, CO −32 и другие полярные молекулы H2O, NH3, CO, NO, PH3 и другие неполярные, но легко поляризующиеся этилендиамин (CH2)2(NH2)2 è äð.
|
.. |
.. |
BF3 è KF; |
:F: + e → |
:F: → F− 1 |
|
.. |
.. |
Бор (В) имеет три непарных электрона, в возбужденном состоянии присоединяет три атома фтора за счет ковалентной связи:
.. ..
:F: B :F:
.. .. ..
:F:
..
У фторида-иона есть неподеленная пара электронов, он может быть донором, у бора — орбиталь свободная.
 s-p-состоянии 4 атомных орбиталей, из которых заполнены три, а одна может быть акцептором.
— 38 —

Образование комплексного соединения происходит по схе-
ìå:
|
.. |
|
.. |
|
– |
|
|
|
|||
.. |
:F: |
|
:F: |
|
|
.. .. |
|
.. .. .. |
|
|
|
K+ :F− : + Â :F: = K+ |
|
:F : B :F : |
|
|
|
.. |
.. .. |
|
.. .. .. |
|
|
|
:F: |
|
:F: |
|
|
|
.. |
|
.. |
|
|
|
|
|
|
||
Атом В с координационным числом 4, F — лиганды, К+
— составляют внешнюю сферу (все 4 связи в молекуле равноценны).
Число, показывающее, сколько лигандов координируется вокруг центрального атома, называется координационным числом.
Водородная связь
Это одна из разновидностей донорно-акцепторной связи, осуществляется между молекулами различных веществ, содержащих в своем составе водород.
Энергия водородной связи невысока и равна 20,9—41 кДж/ моль.
Î... HO
//\
CH3—C |
C—CH3 уксусная кислота |
\ |
// |
O—H ... O
Спирты, кислоты, вода, фенолы, аммиак ассоциированы в димеры, тримеры, полимеры.
В сложных молекулах проявляются различные типы связей: Н2SO4
..
.O.
.- .. .-
H+ : O : S: O: Í+
. .. .
.O.
..
— 39 —
Движение молекул и межмолекулярное взаимодействие
Следует различать движение молекулы в целом — поступательное и вращательное — и движение внутри молекулы отдельных ее составных частей — ядер, электронов, атомов и радикалов.
Полная энергия молекулы равна сумме энергии электронного U(ý), колебательного U(k) и вращательного Uâ движений, то есть:
Uì = Uý + Uê + Uâ,
Uý > Uê > Uâ.
Изучение молекулярных спектров позволяет определить энергию электронов в молекуле, распределение электронной плотности, энергию химической связи и природу ее, наличие определенных групп в молекуле, пространственную структуру молекул, размеры связей и молекул и углы между связями.
Известны следующие агрегатные состояния веществ: газообразное, жидкое и твердое.
Любое вещество при определенных условиях может быть получено во всех трех агрегатных состояниях. Каждое из этих состояний определяется соотношением между силами отталкивания и притяжения молекул. Силы притяжения называются âàí- дер-ваальсовыми (Ван-дер-Ваальс — голландский ученый).
Âгазах энергия молекулярного взаимодействия невелика
—â 10—100 раз меньше энергии взаимодействия между молекулами.
Âжидком состоянии расстояние меньше между молекулами, а поэтому ван-дер-ваальсовы силы проявляются в большей степени.
Молекулы жидкости «скользят» одна около другой и только те из них, которые окажутся у поверхности, могут преодолеть силы межмолекулярного взаимодействия и перейти в парообразную форму.
Âтвердых телах поступательное движение молекул отсутствует, частицы могут совершать лишь колебательное движение. Силы межмолекулярного взаимодействия в данном агрегатном состоянии имеют наибольшее значение. Ван-дер-ваальсовы силы обуславливаются электрическими полями молекул или атомов.
—40 —
