
- •3.Основные положения атомно-молекулярного учения
- •8. Принцип Паули. Принципы заполнения орбиталей.
- •28. Закон Рауля
- •29. Закон Вант-Гоффа. Осмос
- •30. Закон Генри. Растворимость.
- •31 Температура кипения и замерзания раствора.
- •32. Растворы электролитов. Сильные и слабые электролиты.
- •33. Водородный показатель
- •34. Гидролиз солей
- •36. Строение мицеллы
- •37. Кристаллическое и аморфное состояние веществ. Типы кристаллической решетки.
- •39. Методы получения металлов
- •40. Электролиз. Законы электролиза
- •41. Гальванические элементы
- •42. Коррозия металлов
- •43. Методы защиты металлов от коррозии
- •44. Сплавы. Основные типы двухкомпонентных диаграмм состояния.
- •46. Минеральные вяжущие вещества, и их химический состав.
- •49. Классификация органических соединений.
41. Гальванические элементы
Это устройства ддля преобразования хим.энергии в электрическую
Принцип действия основан на пространственном разделении окислительного и восстановит. Процесса. Электроны от восстановителя окислителю переходят по внешнему проводнику.
Любой гальванический элемент сост. Из 2х электродов: анода и катода
Каждый электрод представляет собой систему, содержащую один и тот же элемент в 2х разных степенях окисления(окисленной и восстановленной формах)
Гальванический элемент Даниэля-Якоби
42. Коррозия металлов
Самопроизвольное разрушение Ме под действием окр. среды, это ОВР, протекающие на пов-ти раздела фаз
По механизму протекания м.б.:-химическая,-электрохимическая
Хим. обусловлена вз-ием Ме с сухими газами или жидкостями, не проводящими эл.ток. Протекает без возникновения тока. (разновидность-газовая коррозия). У некоторых Ме соприкосновение с возд.(газами) замедляет коррозию, т.к. на пов-ти Ме обр-ся защитная оксидная пленка, которая препятствует проникновение к Ме газов и жидкостей. Такой Ме становится пассивным, неактивным(Al, Cr, Zn, пассивным Ме делает конц. HNO3). Примером корр. в неэлектролитах может служить разруш. цилиндров в ДВС за счет серы, содерж. в бензине. S+O2->SO2 – обр-ся агрессивные оксиды
Наиб. вред наносит электрохим. коррозия-процесс разрушения Ме, находящегося в контакте с др. Ме среди электролита(возникнов. гальв. тока)
*место для рисунка*
 ;
pH<7
;
pH<7
Анодный
процесс:

Катодный процесс: водородная диполяризация

Атмосферная коррозия.
H20, ph=7; среда нейтральная
*место для рисунка*
Анодный
процесс:

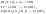 Катодный
процесс:
Катодный
процесс:
43. Методы защиты металлов от коррозии
Лаки, краски, покрытия
Электрохимические способы:
А)
анодная защита - менее активный Ме
покрывает более активный

Б) катодная защита – обратна анодной защите

В) протекторная – вариант анодной. Используется для защиты мостов, тоннелей, ж/д путей, линий электропередач
3. создание инертной атмосферы
4. Вакуумирование
5. Использование различных сплавов
44. Сплавы. Основные типы двухкомпонентных диаграмм состояния.
Сплавы делятся на:
- Металлические (только из металлов Cu+Zn – латунь, Fe+C – чугун)
- Неметаллические (Естественные силикаты – гнейс, базальт, гранит; искусственные силикаты – стёкла, шлаки металлического производства, славы солей)
Свойства сплавов зависят от их состава.
Типы: 1. Сплавы не образующие интерметаллические соединения и твёрдых растворов.
2. Сплавы образующие интерметаллические соединения. 3. Сплавы образующие твердые растворы.
Температура сплавов ниже, а прочность а твёрдость выше чем у компонентов их образующих.
Можно получить сплавы с заранее заданными свойствами.
Бронза(медь + олово) Латунь(медь + цинк(35-30%)) Баббиты(олово + свинец) Нихром(никель + хром) Победит(углерод + вольфрам + кобальт(при бурении горных парод)) Сталь(Fe+C(1,7%)) Чугун(Fe+C(>2%))
