
- •3.Основные положения атомно-молекулярного учения
- •8. Принцип Паули. Принципы заполнения орбиталей.
- •28. Закон Рауля
- •29. Закон Вант-Гоффа. Осмос
- •30. Закон Генри. Растворимость.
- •31 Температура кипения и замерзания раствора.
- •32. Растворы электролитов. Сильные и слабые электролиты.
- •33. Водородный показатель
- •34. Гидролиз солей
- •36. Строение мицеллы
- •37. Кристаллическое и аморфное состояние веществ. Типы кристаллической решетки.
- •39. Методы получения металлов
- •40. Электролиз. Законы электролиза
- •41. Гальванические элементы
- •42. Коррозия металлов
- •43. Методы защиты металлов от коррозии
- •44. Сплавы. Основные типы двухкомпонентных диаграмм состояния.
- •46. Минеральные вяжущие вещества, и их химический состав.
- •49. Классификация органических соединений.
1.Химия как предмет естествознания Химия изучает ту форму движения материи, в которой происходит взаимодействие атомов с образованием новых определенных веществ.Химия-наука о оставе,строении и свойствах веществ, их превращении или явлениях, кот.эти превращения сопровождают.Современная химия включает:общую, органическую,коллоидную,аналитическую,физическую,геологическую,биохимию,химию строительных материалов.Предмет химии — химические элементы и их соединения, а также закономерности, которым подчиняются различные химические реакции. соединяет физико-математические и биолого-социальные науки.
2.Класс неорганических соединений. Основные химические свойства кислот, оснований, солей. По свойствам неорганических соединений разделяеют на след. Классы: оксиды, основания, кислоты, соли.Оксиды-соединение элементов с кислородом, в которых последний является более электроотрицательным элементом, а именно проявляет степень окисления -2. и имеет место связь только элемент О2.Общ.формула СхОу. Бывают:кислотные-способны к солеобразованию с основными оксидами и основаниями (SO3+Na2O=Na2SO4; So3+2NaOH=Na2SO4=H2O),основные-способны к солеобразовнию с кислотными оксидами и кислотами(СаО+СО2=СаСО3; СаО+2НСl=CaCl2+H2O ),амфотерные(к-ты и основ.)и с тем и с тем(ZnO,BeO,Cr2O3,SnO,PbO,MnO2).и несолеобразующие(CO,NO,N2O)Основания - вещества, при электролтической диссоциации которых анион м.б. только гидроксильная группа ОН. Кислотность основания-число ионов ОН образующихся при диссоциации гидроксида. Гидроксиды-вещества, содержащие группу ОН, получаются соединением оксидов с водой.Бывают 3видов: основные( основания) ,кислотные (кислородсодержащие кислоты) и амфотерные(амфолиты-проявляют основные и кислотные свойства Cr(OH)3,Zn(OH)2,Be(OH)2,Al(OH)3) Кислоты-вещества, при электролитической диссоциации кот. Катионом м.б. только + заряженный ион Н. Бывают: бескислородные,кислородсодержащие.Число Н-основность кислоты. мета и орто формы-молекулы воды. Соли—вещества, при электоролитической диссоциации которых катионом может быть ион аммония(NH4) или ион металла, а анионом любой кислотный остаток Бывают:средние(полное замещение.состоят из кисотного остатка и иона метала), кислые(неполное замещение.наличие в составе незамещенных Н), основные (неполное замещение.наличие незамещенных ОН) По составу неорганические вещества делятся на бинарные – состоящие только из двух элементов, и многоэлементные – состоящие из нескольких элементов.
3.Основные положения атомно-молекулярного учения
1.Все вещества состоят из молекул(корпускулы), при физических явлениях, молекулы сохраняются, при химических разрушаются.
2.Молекулы состоят из атомов(элементы), при химических реакциях атомы сохраняются.
3.Атомы каждого вида (элемента) одинаковы между собой, но отличаются от атомов любого другого вида.
4. При взаимодействии атомов образуются молекулы: гомоядерные (при взаимодействии атомов одного элемента) или гетероядерные (при взаимодействии атомов разных элементов).
5.Химичские реакции заключаются в образовании новых веществ, из тех же самых атомов, из которых состоят первоначальные вещества.+6.молек. и атомы находятся в непрерывном движении, а теплота состоит во внутреннем движении этих частиц
. Атом - наименьшая частица элемента, сохраняющая его химические свойства. Атомы различаются зарядами ядер, массой и размерами
Химический элемент - вид атомов с одинаково полож. Зарядом ядра. Физических свойств, характерных для простого вещества, химическому элементу приписать нельзя. Простые вещества - это вещества, состоящие из атомов одного и того же химического элемента. 4.Основные законы химии(закон сохранения, постоянства состава,кратных отношений, закон Авагадро) Закон сохранения: Масса веществ, вступающих в реакцию, равна массе веществ, образующихся в результате реакции. Закон постоянства состава: (любое хим. Соединение имеет один и тот же количественный состав независимо от способа его получения)Соотношения между массами элементов, входящих в сотав данного соединения,постоянны и не зависят от способа получения этого соединения.
Закон кратных отношений: Если два элемента образут друг с другом несколько химических соединений, то массы одного из элементов, приходящиеся в этих соединениях на одну и ту же массу другого, относятся между собой как небольшие целые числа.
Закон Авогадро. В равных объемах любых газов, взятых при одной и той же температуре при одинаковом давлении, содержится одно и то же число молекул.
5.
Закон Эквивалентов.
Эквивалент
вещества-
это такое количество вещества,какое
взаимодействует с 1 молем атома водорода
или вытесняет такое же количество
атомов Н в хим. Реакций.
Vэ(Л/Моль)-
эквивалентный объем вещества, тоесть
то объем одного эквивалента вещества
в газообразном состояние.ЗАКОН.Все
вещества реагируют в химических реакциях
и образуются в эквивалентных количествах.
Отношение
эквивалентных масс, объемов, реагирующих
или образующих вещества,прямо
пропорционально отнощению их
масс(объемов)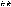 или
или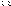 или
или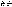 Э(простые)=А(атомная
масса)/В(валентность элемента)
Э(кислоты)=М(молярная
масса)/осн(основание кислоты)
Э(Гидроксида)=М/Кисл)Кислотность
гидроксида)
Э(аксиды
соли)=M/а(количество
атомов элемента образ. Оксид(соли)*в
(валентность этого элемента или металла)
Э(простые)=А(атомная
масса)/В(валентность элемента)
Э(кислоты)=М(молярная
масса)/осн(основание кислоты)
Э(Гидроксида)=М/Кисл)Кислотность
гидроксида)
Э(аксиды
соли)=M/а(количество
атомов элемента образ. Оксид(соли)*в
(валентность этого элемента или металла)
6. Строение атомов. Ядро. Ядерные реакции. Виды излучения. Модель по резерфорду:1.практически вся масса сосредоточена в ядре 2.+ компенисруются – 3.заряд равен номеру группы. Простейшим –Н водород Современное понятие хим. Элемента-вид атомов с одинаково полож. Зарядом ядря атом состоит из положительно заряженного ядра и электронной оболочки. Электронная оболочка образована электронами. Число электронов равно числу протонов, поэтому заряд атома в целом равен 0 Число протонов, заряд ядра и число электронов численно равны порядковому номеру химического элемента. практически вся масса атома сосредоточена в ядре. Электроны двигаются вокруг ядра атома, не беспорядочно, а в зависимости от энергии, которой они обладают, образуя так называемый электронный слой. На каждом электронном слое может располагаться определенное число электронов: на первом — не больше 2, на втором — не больше 8, на третьем — не больше 18. Число электронных слоев определяется по номеру периода Число электронов на последнем (внешнем) слое определяется по номеру группы в периоде происходит постепенное ослабление металлических свойств и возрастание свойств неметаллов Я́дерная реа́кция — процесс образования новых ядер или частиц при столкновениях ядер или частиц. Радиоактивностью называют самопроизвольное превращение неустойчивого изотопа одного химического элемента в изотоп другого элемента, сопроваждающееся испусканием элементарных частиц или ядер.Виды излучений :альфа ,бета(отриц и полож) и гамма. Алфа частица – ядро атома гелия 4/2He. При испускании альфа-частиц ядро теряет два протона и два нейтрона,следовательно заряд уменьшается на 2, а массовое число на 4.отрицательная бэта частица – электрон . при испускании электрона заряд ядра увеличивается на единицу, а массовое число не изменяется. нестабильный изотоп оказывается настолько возбужденным, что испускание частицы не приводит к полному снятию возбуждения, тогда он выбрасывает порцию чистой энергии, называемой гамма-излучением. Атомы обладающие одинаковы зарядом ядра, но разными массовыми числами, называются изотопами(например 35/17 Cl и 37/17Cl) Атомы имеющие одинаковые массовые числа,но разное число протонов в ядре,называются изобарами(например 40/19K и 40/20Ca) Периодом полураспада (Т ½ )называется время,за которое распадается половина исходного количества радиоактивного изотопа.
