
- •Министерство сельского хозяйства Российской Федерации
- •Введение.
- •Лекция 1
- •Ж) мгновенное ускорение
- •Выражение пути и перемещения через мгновенную скорость.
- •Равнопеременное движение.
- •1.2. Криволинейное движение. Центростремительное ускорение. Кинематика вращательного движения. Движение материальной точки по окружности.
- •Ускорение при криволинейном движении.
- •Вопросы для самоконтроля
- •Лекция 2 основы динамики материальной точки
- •2.1. Законы Ньютона. Виды взаимодействий. Сила и масса. Виды сил в механике.
- •Законы Ньютона.
- •2.2. Импульс тела и импульс силы. Закон сохранения импульса для системы тел. Системы замкнутые и открытые. Центр массы системы тел.
- •2.3. Работа и мощность. Кинетическая и потенциальная энергия. Закон сохранения энергии.
- •Вопросы для самоконтроля
- •Лекция 3
- •Вращение твердого тела.
- •Теорема Штейнера.
- •Основное уравнение динамики вращательного движения.
- •Кинетическая энергия вращающегося твердого тела.
- •Вопросы для самоконтроля
- •Лекция 4 колебания и волны
- •4.1. Колебательное движение. Дифференциальное уравнение гармонических колебаний математического, физического и пружинного маятников. Амплитуда, фаза, частота и период колебаний.
- •Колебания математического маятника.
- •Вынужденные колебания. Резонанс. Затухающие колебания. Декремент затухания. Добротность.
- •Затухающие колебания.
- •Волновое движение. Продольные и поперечные волны. Уравнение волны. Фазовая и групповая скорость. Длина волны и частота. Энергия волны. Сложение волн. Стоячие волны.
- •Вопросы для самоконтроля
- •Лекция 5. Основы молекулярной физики и термодинамики.
- •5.1. Статистический и термодинамический методы в молекулярной физике. Масса и размеры молекул. Число Авогадро. Идеальный газ. Термодинамические параметры. Уравнение состояния. Изопроцессы.
- •5.2. I начало термодинамики. Теплота, работа и внутренняя энергия.
- •I начало термодинамики.
- •I начало термодинамики для различных процессов.
- •Уравнение Пуассона для адиабатического процесса.
- •Политропический процесс.
- •Вопросы для самоконтроля
- •Лекция 6.
- •6.1. Основное уравнение молекулярно-кинетической теории газов для давления. Распределение Максвелла-Больцмана молекул газа по скоростям.
- •Распределение Максвелла. Распределение молекул по скоростям.
- •Барометрическая формула.
- •Распределение Больцмана.
- •6.2. Число степеней свободы. Распределение энергии по степеням свободы. Явление переноса. Принцип распределения энергии по степеням свободы.
- •Явления переноса.
- •Цикл Карно. Теорема Карно.
- •Теорема Карно.
- •Понятие энтропии.
- •Неравенство Клазиуса.
- •Статистический смысл энтропии.
- •Вопросы для самоконтроля
- •Содержание
Вопросы для самоконтроля
Какое движение называется колебательным?
Что называют амплитудой, периодом, фазой колебания?
Как период колебания маятника зависит от амплитуды при малых амплитудах?
Что называется математическим маятником?
Как называется явление резкого возрастания амплитуды колебаний? При каком условии оно наступает?
Как определяется декремент затухания?
Что называется добротностью колебательной системы.
Какие процессы называются волновыми?
Какие типы волн вы знаете?
Что представляет собой волновое уравнение.
СПИСОК ЛИТЕРАТУРЫ
Основная
Детлаф, А.А. Курс физики учеб. пособие / А.А. Детлаф, Б.М. Яворский.-7-е изд. Стер.-М. : ИЦ «Академия».-2008.-720 с.
Савельев, И.В. Курс физики: в 3т.: Т.1: Механика .Молекулярная физика : учеб.пособие / И.В. Савельев.-4-е изд. стер. – СПб.; М. Краснодар: Лань.-2008.-352 с.
Трофимова, Т.И. курс физики: учеб. пособие/ Т.И. Трофимова.- 15-е изд., стер.- М.: ИЦ «Академия», 2007.-560 с.
Дополнительная
Фейнман, Р. Фейнмановские лекции по физике / Р. Фейнман, Р. Лейтон, М. Сэндс. – М.: Мир.
Т.1. Современная наука о природе. Законы механики. – 1965. –232 с.
Т. 2. Пространство, время, движение. – 1965. – 168 с.
Т. 3. Излучение. Волны. Кванты. – 1965. – 240 с.
Берклеевский курс физики. Т.1,2,3. – М.: Наука, 1984
Т. 1. Китель, Ч. Механика / Ч. Китель, У. Найт, М. Рудерман. – 480 с.
Т. 2. Парселл, Э. Электричество и магнетизм / Э. Парселл. – 448 с.
Т. 3. Крауфорд, Ф. Волны / Ф. Крауфорд – 512 с.
Фриш, С.Э. Курс общей физики: в 3 т.: учеб. / С.Э. Фриш, А.В. Тиморева.- СПб.: М.; Краснодар: Лань.-2009.
Т. 1. Физические основы механики. Молекулярная физика. Колебания и волны: учебник - 480 с.
Т.2: Электрические и электромагнитные явления: учебник. – 518 с.
Т. 3. Оптика. Атомная физика : учебник– 656 с.
Лекция 5. Основы молекулярной физики и термодинамики.
5.1. Статистический и термодинамический методы в молекулярной физике. Масса и размеры молекул. Число Авогадро. Идеальный газ. Термодинамические параметры. Уравнение состояния. Изопроцессы.
1. Масса и размер молекул.
Один моль – количество вещества, масса которого, выраженная в граммах численно равна атомному (молекулярному) весу вещества.
С А = 12 а.е.м
1 моль – 12 г
H2O 1 моль – 18 г молекулярный вес – 18 а.е.м.
Число Авогадро – количество атомов или молекул вещества, содержащееся в 1 моле вещества.
Na = 6,02·1023 моль-1
Масса одной молекулы углерода
mC
=
![]() =
=
![]()
Размер.
1г
– 1 см3 VH2O
=
![]() - объем одной молекулы.
- объем одной молекулы.
так как в жидкости молекулы находятся рядом друг с другом (нет пустоты).
![]()
Мы оценили размер и массу маленького атома и молекулы, те атомы, которые находятся в конце таблицы Менделеева, они в 10 – 15 раз тяжелее С. В органической химии получены молекулы, размеры которых составляют доли мм (полимеры).
Эти
молекулы – длинные, но поперечный размер
~
![]()
Существует 2 способа описания газов.
1. Газ можно описывать как целое с помощью макропараметров, к которым относятся: давление, объем, температура. Макропараметры еще называют основными термодинамическими параметрами вещества. Наука, которая описывает вещество с помощью макропараметров, называется термодинамика.
2. Вещество можно описывать с помощью микропараметров (параметров, характеризующих одну отдельно взятую молекулу вещества) – импульс одной молекулы, скорость молекулы, кинетическая энергия молекулы, момент импульса молекул и т.д.
Раздел физики, который описывает вещество с помощью микропараметров, называется молекулярно – кинетической теорией.
В термодинамике важнейшее место занимает уравнение состояния вещества.
Наиболее постой вид имеет уравнение состояния идеального газа, называемое уравнением Менделеева – Клайперона.
![]()
Изопроцессами называются такие термодинамические процессы, при которых один из основных термодинамических параметров вещества остается неизменным.
1. Изотермический процесс. (T = const)
![]() (закон
Бойля - Мариотта)
(закон
Бойля - Мариотта)
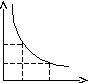 Р
Р
P1
P2
V1 V2 V
2. Изобарный процесс (P = const).
![]() (закон
Гей - Люссака)
(закон
Гей - Люссака)
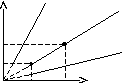
P V
 V2
V2
V1
V T1 T2 T
3. Изохорный процесс (V = const)
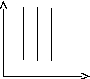 P
P![]() (закон Шарля)
(закон Шарля)
V
 P
P
T
