
- •1.Электромагниттік сәуленің табиғаты және оның негізгі сипаттамалары, эмс спектрі
- •3. Атомдық спектр. Спектрлік сызықтардың толқын ұзындықтарын анықтау әдістері.
- •4. Атомдық спектрларді заттың химиялық құрамын анықтау үшін қолдану.
- •5. Жылулық шығарылған сәуле және оның сипаттамалары. Қара дене.
- •7.Жарық кванттары жайындағы Эйнштейн гипотезасы
- •12.Фотондар. Фотонның энергиясы, импульсы,массасы.
- •14. Микробөлшектердің толқындық қасиеттерінің тәжірибелік расталуы ( Дэвиссон мен Джермер, Томсон, Тартаковский тәжірибелері).
- •1.Кванттық механикада бөлшек траекториясы ұғымы мағынасын жояды.
- •2. Микробқлшектің толық тыныштық күйде болуы мүмкін еместігі.
- •3.Анықталмағандықтар қатынастарынан шығатын тағы бір қорытынды:бөлшектің толқындық қасиеттерін ескергенде бөлшектің толық энергиясын кинетикалық және потенциалдық энергияға бөлудің мағынасы жойылады.
- •16. Резерфорд тәжірибелері. Атомның құрылысы.
- •17.Атомның ядролық моделі, оның классикалық физика заңдарымен үйлеспеуі.
- •20 Ғ бас кезінде ешқандай күмәнсыз бар екендігі мойындалды.
- •18. Атомдық спектрлер.Сериялық заңдылықтар. Спектрлік терм. Комбинация принципі.
- •25.Бор теориясының кемшілігі
- •26.Спектрлік сызықтардың изотоптық ығысуы. Сутегі атомы мен сутегі тәрізді иондардың жиіліктері үшін формулалар мына түрге келеді
- •31. Бір электрондық атомдық жүйелер үшін Шредингер теңдеуі және атомның квантталуы.
- •32.Бір электронды атомның кванттық сандары және бұлардың физикалық мағынасы.
- •1.Атомдық жүйелердің ең қарапайымы бір электрондық атомдар: н,,,…; мезоатомдар, позитроний.
- •33. Бір электронды атомның толқындық функциялары. Энергия деңгейлерінің азғындау дәрежесі.
- •34.Күйлердің белгіленуі. Сұрыптау ережелері і.
- •35. Сутегі атомының энергетикалық спектрі. Шығару және жұтылу спектрі.
- •45.Ядро спині.Атомның энергия деңгейлерінің және спектрлік сызықтарының аса нәзік түзілісі.
- •I және j берілген жағдайда векторының абсолют шамасы
- •49.Рентген түтікшесінің антикатодын электрондармен атқылағанда пайда болатын рентгендік спектрлердің екі түрі болады:тұтас және сызықтық.
- •53.Қарапайым Зееман эффекті.
- •57. Екі атомды молекуланың айналысы, айналыс спектрі.
- •58.Екі атомды молекуланың тербелісі
3. Атомдық спектр. Спектрлік сызықтардың толқын ұзындықтарын анықтау әдістері.
Атом—химиялық элементтің оның химиялық қасиеттеріне ие ең кіші бөлшек. Атомның спектірі— сызықтық спектр.
Спектрлiк сызықтардың толқын ұзындықтарын анықтау ең дәл физикалық өлшеулерге жатады. Спектрлiк сызықтардың толқын ұзындықтарын 10-4 нм-ге дейiнгi дәлдiкпен есептеуге мүмкіндік беретiн көптеген әр түрлi тәсiлдер бар.
Спектрлiк прибордың дисперсиялық қисығы бойынша немесе прибордың толқын ұзындықтар шкаласын тiкелей пайдаланып толқын ұзындықты шамалап анықтауға болады.
Салыстыру спектрi. Спектроскопия практикасында толқын ұзындықты өлшеу үшін көбiнесе спектр фотографиялық тiркелiнедi. Өлшеулер үшін салыстыру тәсiлi қолданылады. Сонда толқын ұзындықтары жоғары дәлдiкпен өлшенген (нормальдар деп аталатын) сызықтары бар салыстыру спектрi сызықтарының аралығындағы өлшенетiн сызықтардың толқын ұзындықтарына интерполяция жасалады. Салыстыру спектрi ретiнде көбiнесе бiрнеше жақсы атластары шығарылған темiрдiң доғалық спектрi алынады. Кейбiр жағдайларда сынап, мыс, аргон, неон және басқа элементтер спектрi пайдаланылады.
21
Дәл өлшеулер үшін екi спектр-өлшенетiн және салыстырылатын спектрде-бұлар жартылай немесе толық қабаттасатындай етiлiп суретке түсірiлуi тиiс.
Сызықтық интерполяция. Прибордың сызықтық дисперсиясы тұрақты болған жағдайда сызықтың толқын ұзындығын анықтау үшін белгiлi екi сызықтың ара қашықтығын және бұлардың бiреуiнен өлшенетiн сызыққа дейiнгi қашықтықты өлшеу жеткiлiктi.
Осы жағдайда өлшеу приборының толқын ұзындықтары 1 және 2 белгiлi сызықтарға келтiрiлгендегi көрсетуi (санауы) n1 және n2, ал өлшенетiн х сызыққа келтiрiлгендегi прибордың көрсетуi (санауы) nх болсын дейiк.
Сонда дисперсияның тұрақтылығы шартынан мына өрнек алынады:
 (1.1)
(1.1)
осыдан
 (1.2)
(1.2)
Гартман формуласы. Призмалық аспаптар үшін аспаптың сызықтық дисперсиясын бейнелейтiн Гартман формуласы
 (1.3)
(1.3)
жақсы нәтиже бередi. Бұл формулада n0, с және 0 үш тұрақты бар; бұлар 1, 2 және 3 толқын ұзындықтары белгiлi үш сызық арқылы анықталады. Осы 1, 2, 3 мәндерiн және бұларға сәйкес аспаптың n1, n2, және n3 көрсетулерiн (1.3) формулаға қойғанда теңдеулер жүйесi алынады. Осы жүйенiң шешiмi :
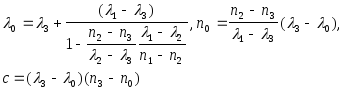
Толқын ұзындығын спектрлік сызықтардың атласы көмегімен анықтау.
Спектропроектор экранына проекцияланған спектрограммадағы темір спектрін планшеттегі темір спектрімен беттестіреді. Зерттелетін зат үлгісі спектріндегі сызықтың толқын ұзындығы атлас бойынша тікелей анықталады.
4. Атомдық спектрларді заттың химиялық құрамын анықтау үшін қолдану.
Әрбір химиялық элемент атомының және әрбір молекуласының тек өзіне тән спектрі б.ды.демек спектр б/ша заттың химиялық (элементтік) құрамын анықтауға б.ды.
Сапалық спектрлiк талдау негiзiне әрбiр химиялық элемент атомдары қоздырылған кезде осы элементке тән сызықтық спектр шығару қабілетi алынған. Сондықтан зат үлгісiнiң шығару спектрiнде элементтiң көрiнген кезкелген спектрлiк сызығы осы элементтiң зат үлгісiнде бар екендiгiнiң дәлелi ретiнде қабылдауға болады.
Басқа талдау әдiстерiмен салыстырғанда спектрлiк талдау ең қарапайым, тез әрi сезгiштiгi жоғары әдiс болып табылады. Спектрлiк талдау, әдетте, талданатын материалды жiктеудi қажет етпейдi. Фотографиялық тiркеу әдiсiн қолданғанда бiрнеше мг болатын зат үлгісiндегi көптеген элементтi бiрден анықтауға болады.
Сапалық талдауды жүргізу бiрнеше iс-әрекеттен тұрады:
Талданатын зат үлгісi буға айналдырылып және спектрiн қоздыру; 2. Спектрдi көзбен қарау немесе суретке түсіру; 3. Спектрден тиiстi элементтердiң бұларға тән сызықтарын табу.
Зерттелетiн зат үлгісiнде берiлген элементтiң бар екендiгiн анықтау үшін спектрден бiр-екi тиiстi сызықтың (талдау сызығы-аналитическая линия) сенiмдi табылуы жеткiлiктi болады.
Әрбiр элемент үшін «соңғы» сызықтар деп аталатын бiрнеше ең сезгiш сызықтар тағайындалған; бұлар берiлген элемент концентрациясын төмендеткенде спектрдегi сызықтар саны бiрте-бiрте азайып спектрден ең соңында жойылатын (көрiнбей кететiн) сызықтар. Әр түрлі элемент үшін «соңғы» сызықтар жойылатын концентрация да әр түрлі болады. Элементтердiң көпшiлiгiн бұлардың концентрациясы 0,01-0,001% болғанда, кейде <0,001% болғанда анықтауға болады. «Соңғы» сызықтардың, әдетте, қоздыру потенциалы жоғары болмайды. Көбiнесе бұл сызықтар атомның төменгi, негiзгi деңгейге ауысуларына сәйкес келедi де резонанстық сызықтар болып табылады. Талдау сенiмдiлiгiн арттыру үшін әрбiр элементтi анықтау жалғыз сызық бойынша емес, көбiне оның бiрнеше «соңғы» сызығы бойынша жүргізiледi. Барлық элементтер үшін бұлардың «соңғы» сызықтары жақсы белгiлi. Бұлардың тiзбеci спектрлiк сызықтар кестелерiнде, спектрлiк сызықтар атластарында келтiрiлген.
Ескеретiн нәрсе, үлгідегi элемент концентрациясын төмендеткенде спектрлiк сызықтардың жойылу ретi қатаң тұрақты емес, көптеген себептерге: қоздыру көзiне, фотопластинка сезгiштiгiне, үлгі құрамына тәуелдi болады. Мысалы, Zn I 213,9 нм сызығы спектрдiң қысқа толқынды бөлiгiне арнайы сезгiштiгi күшейтiлген пластинканы қолданғанда ғана «соңғы» сызық бола алады. Ал бұлай болмаған жағдайда бұл сызық спектрден басқаларынан бұрын жойылады (көрiнбей кетедi).
Әр түрлі элементтердiң көптеген сызықтары толқын ұзындықтары бойынша бiрiне-бiрi өте жақын болады; бұлар спектрограммада бiрiмен-бiрi қабаттасып жататындықтан бұларды ажырату қиын болады.
Егер барлық элементтер үшін құрастырылған спектрлiк сызықтар кестелерiн 13,14 қарайтын болсақ, онда әрбiр 0,1-0,15 нм-ге әр түрлі элементтердiң ондаған сызығы келетiнiн көруге болады. Бiрақ талдау сызығына сызықтары қабаттасуы мүмкін элементтердiң саны әдетте онша көп болмайды. Талдау сызығына көршi сызықтардың көпшiлiгiн берiлген жарық көзiнде қоздырылу мүмкіндiгiне немесе үлгі құрамына байланысты алдын-ала ескермеуге болады.
Спектрлiк талдау тәсiлi зат құрамына 0,01-0,001% және бұдан да төмен мөлшерде енетiн 80-нен астам химиялық элементтi анықтауға мүмкіндiк бередi. Алайда элементтердiң ең сезiмтал сызықтары инфрақызыл аймақтан бастап вакуумдық ультракүлгін аймаққа дейiн созылып жатқан өте кең спектрлiк алқапты аралықта орналасқан. Сондықтан бұлардың бәрiн тiркеу үшін әр түрлі сәуле қабылдағыштар мен спектрлiк аспаптарды қолдану қажет болады. Бұған қоса осы элементтердiң «соңғы» сызықтарының қоздыру энергияларында үлкен айырмашылық болатындықтан барлық элементтердiң спектрлерiн бiр жарық көзiнде қоздыру да мүмкін болмайды. Осыған байланысты химиялық элементтер екi топқа бөлiнедi: оңай қоздырылатын және қоздырылуы қиын элементтер. Оңай қоздырылатын элементтерге, әдетте, металдар, ал екiншi топқа металлоидтар, инерттi газдар, оттегi, азот, күкiрт жатады. Екiншi топ элементтерiнiң сезiмтал сызықтары алыс ультракүлгін аймақта (200 нм) жатады да тiркеу қиындық туғызады.
