
- •Глава 1
- •§ 1. Модели в механике. Система отсчета. Траектория, длина пути, вектор перемещения
- •§ 2. Скорость
- •§ 3. Ускорение и его составляющие
- •§ 4. Угловая скорость и угловое ускорение
- •Глава 2
- •§ 5. Первый закон Ньютона. Масса. Сила
- •§6. Второй закон Ньютона
- •§ 7. Третий закон Ньютона
- •§ 8. Силы трения
- •§ 9. Закон сохранения импульса. Центр масс
- •§ 10. Уравнение движения тела переменной массы
- •Глава 3 Работа и энергия
- •§11. Энергия, работа, мощность
- •§ 12. Кинетическая и потенциальная энергии
- •§ 13. Закон сохранения энергии
- •§ 14. Графическое представление энергии
- •§ 15. Удар абсолютно упругих и неупругих тел
- •Глава 4
- •§ 16. Момент инерции
- •§ 17. Кинетическая энергия вращения
- •§ 18. Момент силы. Уравнение динамики вращательного движения твердого тела
- •§ 19. Момент импульса и закон его сохранения
- •§ 20. Свободные оси. Гироскоп
- •§21. Деформации твердого тела
- •Глава 5
- •§ 22. Законы Кеплера.
- •§ 23. Сила тяжести и вес. Невесомость
- •§ 24. Поле тяготения и его напряженность
- •§ 25. Работа в поле тяготения. Потенциал поля тяготения
- •§ 26. Космические скорости
- •§ 27. Неинерциальные системы отсчета. Силы инерции
- •Глава 6
- •§ 28. Давление в жидкости и газе
- •§ 29. Уравнение неразрывности
- •§ 30. Уравнение Бернулли и следствия из него
- •§ 31. Вязкость (внутреннее трение). Ламинарный и турбулентный режимы течения жидкостей
- •§ 32. Методы определения вязкости
- •§ 33. Движение тел в жидкостях и газах
- •Глава 7
- •§ 34. Преобразования Галилея. Механический принцип относительности
- •§ 35. Постулаты специальной (частной) теории относительности
- •§ 36. Преобразования Лоренца
- •§ 37. Следствия из преобразований Лоренца
- •§ 38. Интервал между событиями
- •§ 39. Основной закон релятивистской динамики материальной точки
- •§ 40. Закон взаимосвязи массы и энергии
- •Глава 9
- •§ 50. Число степеней свободы молекулы. Закон равномерного распределения энергии по степеням свободы молекул
- •§51. Первое начало термодинамики
- •§ 52. Работа газа при изменении его объема
- •§ 53. Теплоемкость
- •§ 54. Применение первого начала термодинамики к изопроцессам
- •§ 55. Адиабатический процесс. Политропный процесс
- •§56. Круговой процесс (цикл). Обратимые и необратимые процессы
- •§ 57. Энтропия, ее статистическое толкование и связь с термодинамической вероятностью
- •§ 58. Второе начало термодинамики
- •§ 59. Тепловые двигатели и холодильные машины. Цикл Карно и его к. П. Д. Для идеального газа
- •Глава 10
- •§ 60. Силы и потенциальная энергия межмолекулярного взаимодействия
- •§61. Уравнение Ван-дер-Ваальса
- •§ 62. Изотермы Ван-дер-Ваальса и их анализ
- •§ 63. Внутренняя энергия реального газа
- •§ 64. Эффект Джоуля — Томсона
- •§ 65. Сжижение газов
- •§ 66. Свойства жидкостей. Поверхностное натяжение
- •§ 67. Смачивание
- •§ 68. Давление под искривленной поверхностью жидкости
- •§ 69. Капиллярные явления
- •§ 70. Твердые тела. Моно- и поликристаллы
- •§71. Типы кристаллических твердых тел
- •2. Физический признак кристаллов.
- •§ 72. Дефекты в кристаллах
- •§ 73. Теплоемкость твердых тел
- •§ 74. Испарение, сублимация, плавление и кристаллизация. Аморфные тела
- •§75. Фазовые переходы I и II рода
- •§ 76. Диаграмма состояния. Тройная точка
- •Глава 11
- •§ 77. Закон сохранения электрического заряда
- •§ 78. Закон Кулона
- •§ 79. Электростатическое поле. Напряженность электростатического поля
- •§ 80. Принцип суперпозиции электростатических полей, Поле диполя
- •§81. Теорема Гаусса для электростатического поля в вакууме
- •§ 82. Применение теоремы Гаусса к расчету некоторых электростатических полей в вакууме
- •4. Поле объемно заряженного шара. Шар
- •§ 83. Циркуляция вектора напряженности электростатического поля
- •§ 84. Потенциал электростатического поля
- •§ 85. Напряженность как градиент потенциала. Эквипотенциальные поверхности
- •§ 86. Вычисление разности потенциалов по напряженности поля
- •§ 87. Типы диэлектриков. Поляризация диэлектриков
- •§ 88. Поляризованность. Напряженность поля в диэлектрике
- •§ 89. Электрическое смещение. Теорема Гаусса для электростатического поля в диэлектрике
- •§ 90. Условия на границе раздела двух диэлектрических сред
- •§91. Сегнетоэлектрики
- •§ 92. Проводники в электростатическом поле
- •§ 93. Электрическая емкость уединенного проводника
- •§ 94. Конденсаторы
- •§ 95. Энергия системы зарядов, уединенного проводника и конденсатора. Энергия электростатического поля
- •4. Энергия электростатического поля.
- •Глава 12 Постоянный электрический ток
- •§ 96. Электрический ток, сила и плотность тока
- •§ 97. Сторонние силы. Электродвижущая сила и напряжение
- •§ 98. Закон Ома. Сопротивление проводников
- •§ 99. Работа и мощность тока. Закон Джоуля — Ленца
- •§ 100. Закон Ома для неоднородного участка цепи
- •§ 101. Правила Кирхгофа для разветвленных цепей
- •Глава 13
- •§ 102. Элементарная классическая теория электропроводности металлов
- •§ 103. Вывод основных законов электрического тока в классической теории электропроводности металлов
- •§ 104. Работа выхода электронов из металла
- •§ 105. Эмиссионные явления и их применение
- •§ 106. Ионизация газов. Несамостоятельный газовый разряд
- •§ 107. Самостоятельный газовый разряд и его типы
- •§ 108. Плазма и ее свойства
- •Глава 21
- •§ 165. Основные законы оптики. Полное отражение
- •§ 166. Тонкие линзы. Изображение предметов с помощью линз
- •§ 167. Аберрации (погрешности) оптических систем
- •§ 168. Основные фотометрические величины и их единицы
- •§ 169. Элементы электронной оптики
- •Глава 22
- •§ 170. Развитие представлений о природе света
- •§ 171. Когерентность и монохроматичность световых волн
- •§ 172. Интерференция света
- •§ 173. Методы наблюдения интерференции света
- •§ 174. Интерференция света в тонких пленках
- •2. Полосы равной толщины (интерференция от пластинки переменной толщины).
- •§ 175. Применение интерференции света
- •Глава 23
- •§176. Принцип Гюйгенса — Френеля
- •§ 177. Метод зон Френеля. Прямолинейное распространение света
- •§ 178. Дифракция Френеля на круглом отверстии и диске
- •§ 179. Дифракция Фраунгофера на одной щели
- •§ 180. Дифракция Фраунгофера на дифракционной решетке
- •§ 181. Пространственная решетка. Рассеяние света
- •§ 182. Дифракция на пространственной решетке. Формула Вульфа — Брэггов
- •§ 183. Разрешающая способность оптических приборов
- •§ 184. Понятие о голографии
- •Глава 26 Квантовая природа излучения
- •§197. Тепловое излучение и его характеристики
- •§ 198. Закон Кирхгофа
- •§ 199. Законы Стефана — Больцмана и смещения Вина
- •§ 200. Формулы Рэлея — Джинса и Планка
- •§201. Оптическая пирометрия.
- •1. Радиационная температура — это
- •§202. Виды фотоэлектрического эффекта. Законы внешнего фотоэффекта
- •§ 203. Уравнение Эйнштейна для внешнего фотоэффекта. Экспериментальное подтверждение квантовых свойств света
- •§ 204. Применение фотоэффекта
- •§ 205. Масса и импульс фотона. Давление света
- •§ 206. Эффект Комптона и его элементарная теория
- •§ 207. Диалектическое единство корпускулярных и волновых свойств электромагнитного излучения
- •7 Элементы физики
- •Глава 32
- •§251. Размер, состав и заряд атомного ядра. Массовое и зарядовое числа
- •§ 252. Дефект массы и энергия связи ядра
- •§ 253. Спин ядра и его магнитный момент
- •§ 254. Ядерные силы. Модели ядра
- •§ 255. Радиоактивное излучение и его виды
- •§ 256. Закон радиоактивного распада. Правила смещения
- •§ 257. Закономерности -распада
- •§258. -Распад. Нейтрино
- •§ 259. Гамма-излучение и его свойства
- •§ 260. Резонансное поглощение -излучения (эффект Мёссбауэра)
- •§ 261. Методы наблюдения и регистрации радиоактивных излучений и частиц
- •§ 262. Ядерные реакции и их основные типы
- •§ 264. Открытие нейтрона. Ядерные реакции под действием нейтронов
- •§ 265. Реакция деления ядра
- •§266. Цепная реакция деления
- •§267. Понятие о ядерной энергетике
- •§ 268. Реакция синтеза атомных ядер. Проблема управляемых термоядерных реакций
- •1.1. Электрический заряд. Закон Кулона
§ 52. Работа газа при изменении его объема
Для рассмотрения конкретных процессов найдем в общем виде внешнюю работу, совершаемую газом при изменении его объема. Рассмотрим, например, газ, находящийся под поршнем в цилиндрическом сосуде (рис. 78). Если газ, расширяясь, передвигает поршень на бесконечно малое расстояние dl, то производит над ним работу
A=Fdl=pSdl=pdV,
где S — площадь поршня, Sdl=dV— изменение объема системы. Таким образом,
A=pdV. (52.1)
Полную работу A, совершаемую газом при изменении его объема от V1 до V2, найдем

91

интегрированием формулы (52.1):

Результат интегрирования определяется характером зависимости между давлением и объемом газа. Найденное для работы выражение (52.2) справедливо при любых изменениях объема твердых, жидких и газообразных тел.
Произведенную при том или ином процессе работу можно изобразить графически с помощью кривой в координатах р, V. Например, изменение давления газа при его расширении изобразится кривой на рис. 79. При увеличении объема на dV совершаемая газом работа равна pdV, т. е. определяется площадью полоски с основанием dV на рисунке. Поэтому полная работа, совершаемая газом при расширении от объема V1 до объема V2, определяется площадью, ограниченной осью абсцисс, кривой p = f(V) и прямыми V1 и V2.
Графически можно изображать только равновесные процессы — процессы, состоящие из последовательности равновесных состояний. Они протекают так, что изменение термодинамических параметров за конечный промежуток времени бесконечно мало. Все реальные процессы неравновесны (они протекают с конечной скоростью), но в ряде случаев неравновесностью реальных процессов можно пренебречь (чем медленнее процесс протекает, тем он ближе к равновесному). В дальнейшем рассматриваемые процессы будем считать равновесными.
§ 53. Теплоемкость
Удельная теплоемкость вещества величина, равная количеству теплоты, необходимому для нагревания 1 кг вещества на 1 К:

Единица удельной теплоемкости — джоуль на килограмм-кельвин (Дж/(кг•К)).
Молярная теплоемкость— величина, равная количеству теплоты, необходимому для нагревания 1 моля вещества на 1 К:

где v = m/M — количество вещества, выражающее число молей.
Единица молярной теплоемкости — джоуль на моль-кельвин (Дж/(моль•К)).
Удельная теплоемкость с связана с молярной Сm соотношением
Ст = сМ, (53.2)
где М — молярная масса вещества.
Различают теплоемкости при постоянном объеме и постоянном давлении, если в процессе нагревания вещества его объем или давление поддерживается постоянным.
Запишем выражение первого начала термодинамики (51.2) для 1 моля газа с учетом формул (52.1) и (53.1):
CmdT = dUm + pdVm. (53.3)
Если газ нагревается при постоянном объеме, то работа внешних сил равна нулю (см. (52.1)) и сообщаемая газу извне теплота идет только на увеличение его внутренней энергии:

т. е. молярная теплоемкость газа при постоянном объеме Сv равна изменению внутренней энергии 1 моля газа при повышении его температуры на 1 К. Согласно формуле (50.1),

92
тогда
Cv = iR/2. (53.5)
Если газ нагревается при постоянном давлении, то выражение (53.3) можно записать в виде
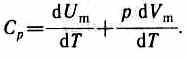
Учитывая, что dUm/dT не зависит от вида процесса (внутренняя энергия идеального газа не зависит ни от р, ни от V, а определяется лишь температурой Т) и всегда равна Сv (см. (53.4)); продифференцировав уравнение Клапейрона — Менделеева pVm=RT (42.4) по T(p=const), получим
Cp = Cv + R. (53.6)
Выражение (53.6) называется уравнением Майера; оно показывает, что Ср всегда больше Сv на величину молярной газовой постоянной. Это объясняется тем, что при нагревании газа при постоянном давлении требуется еще дополнительное количество теплоты на совершение работы расширения газа, так как постоянство давления обеспечивается увеличением объема газа.
Использовав (53.5), выражение (53.6) можно записать в виде

При рассмотрении термодинамических процессов важно знать характерное для каждого газа отношение Ср к Cv:
=Cp/Cv=(i+2)/i. (53.8)
Из формул (53.5) и (53.7) следует, что молярные теплоемкости определяются лишь числом степеней свободы и не зависят от температуры. Это утверждение молекулярно-кинетической теории справедливо в довольно широком интервале температур лишь для одноатомных газов. Уже у двухатомных газов число степеней свободы, проявляющееся в теплоемкости, зависит от температуры. Молекула двухатомного газа обладает тремя поступательными, двумя вращательными и одной колебательной степенями свободы.

По закону равномерного распределения энергии по степеням свободы (см. § 50), для комнатных температур Cv = 7/2R. Из качественной экспериментальной зависимости молярной теплоемкости Сv водорода (рис. 80) следует, что Cv зависит от температуры: при низкой температуре (50 К) Cv=3/2R, при комнатной — Cv=5/2R (вместо расчетных 7/2R!) и очень высокой — Сv=7/2/R. Это можно объяснить, предположив, что при низких температурах наблюдается только поступательное движение молекул, при комнатных — добавляется их вращение, а при высоких — к этим двум видам движения добавляются еще колебания молекул.
Расхождение теории и эксперимента нетрудно объяснить. Дело в том, что при вычислении теплоемкости надо учитывать квантование энергии вращения и колебаний молекул (возможны не любые вращательные и колебательные энергии, а лишь определенный дискретный ряд значений энергий). Если энергия теплового движения недостаточна, например, для возбуждения колебаний, то эти колебания не вносят своего вклада в теплоемкость (соответствующая степень свободы «замораживается» — к ней неприменим закон равнораспределения энергии). Этим объясняется, что теплоемкость моля двухатомного газа — водорода — при комнатной температуре равна 5/2 R вместо 7/2 R. Аналогично можно объяснить уменьшение теплоемкости при низкой температуре («замораживаются» вращательные степени сво-
93
боды) и увеличение при высокой («возбуждаются» колебательные степени свободы).
