
- •7. Элементарные частицы.
- •9. Функция распределения Ферми — Дирака.
- •10.Решение уравнения Шрёдингера для кристаллов. Волновая функция электронов в кристалле. Зона Бриллюэна.
- •13. Эффективная масса электрона в кристалле. Электроны и дырки.
- •14. Энергия Ферми. Поверхность Ферми. Заполнение энергетических зон: металлы, диэлектрики, полупроводники.
1.
Нестационарная теория возмущений. Пусть
H0 –
не зависящий от времени гамильтониан
квантовой системы в отсутствие внешних
полей, причем для этого гамильтониана
уравнение Шредингера допускает точное
решение. Тогда гамильтониан H этой
системы в присутствии нестационарного
внешнего поля имеет вид - H =
H0 +
V(r,t),
где V(r,t)
– оператор, описывающий взаимодействие
внешнего поля с системой (оператор
возмущения). Теория возмущений
используется тогда, когда выполняется
условие V(r,t) << H0.
Пусть квантовая система находится в
поле, характеристики которого периодически
меняются со временем с частотой ![]() (примером
такого поля является поле монохроматической
электромагнитной волны). Тогда оператор
возмущения V(r,t)
также будет периодически меняться со
временем с той же частотой и, следовательно,
может быть записан в виде
(примером
такого поля является поле монохроматической
электромагнитной волны). Тогда оператор
возмущения V(r,t)
также будет периодически меняться со
временем с той же частотой и, следовательно,
может быть записан в виде![]()
![]() Введем
обозначение , тогда
Введем
обозначение , тогда![]() .В
первом порядке зависящей от времени
теории возмущений вероятность перехода
w квантовой
системы в единицу времени из состояния,
описываемого волновой функцией
.В
первом порядке зависящей от времени
теории возмущений вероятность перехода
w квантовой
системы в единицу времени из состояния,
описываемого волновой функцией ![]() i, в
состояние, описываемое волновой
функцией
i, в
состояние, описываемое волновой
функцией ![]() f (
f (![]() i и
i и ![]() f –
собственные функции оператора H0)
под действием возмущения
f –
собственные функции оператора H0)
под действием возмущения ![]() ,
дается выражением
,
дается выражением![]() причем
переходы происходят в состояния,
обладающие энергией Ef =
Ei +
причем
переходы происходят в состояния,
обладающие энергией Ef =
Ei + ![]()
![]() и
плотностью
и
плотностью![]() f(Ef)(Ei и
Ef –
собственные значения оператора H0,
отвечающие собственным
функциям
f(Ef)(Ei и
Ef –
собственные значения оператора H0,
отвечающие собственным
функциям ![]() i и
i и ![]() f).Возмущение
V+(r,t)
приводит к тому, что квантовая система
теряет энергию
f).Возмущение
V+(r,t)
приводит к тому, что квантовая система
теряет энергию ![]()
![]() путем
вынужденного испускания, Ef =
Ei -
путем
вынужденного испускания, Ef =
Ei - ![]()
![]() . Под
действием возмущения V–(r,t) система
приобретает энергию
. Под
действием возмущения V–(r,t) система
приобретает энергию ![]()
![]() и Ef =
Ei +
и Ef =
Ei + ![]()
![]() . B
дальнейшем мы будем рассматривать лишь
последний случай, соответствующий
поглощению энергии поля, оставляя в
операторе возмущения V(r,t) лишь
второе слагаемое V–(r,t),
которое зависит от времени как
. B
дальнейшем мы будем рассматривать лишь
последний случай, соответствующий
поглощению энергии поля, оставляя в
операторе возмущения V(r,t) лишь
второе слагаемое V–(r,t),
которое зависит от времени как ![]() .Для
того чтобы вычислить с помощью выражения
(1.1) вероятность поглощения электромагнитного
излучения квантовой системой, требуется
знание конкретного вида оператора
взаимодействия системы с электромагнитным
полем. Для этого оператора можно получить
точное выражение (см. прил. 1). Подчеркнем,
что в том
случае, когда между квантовой системой
и налетающей частицей осуществляется
сильное взаимодействие, выражение для
гамильтониана этого взаимодействия
можно получить лишь в определенных
модельных приближениях.
.Для
того чтобы вычислить с помощью выражения
(1.1) вероятность поглощения электромагнитного
излучения квантовой системой, требуется
знание конкретного вида оператора
взаимодействия системы с электромагнитным
полем. Для этого оператора можно получить
точное выражение (см. прил. 1). Подчеркнем,
что в том
случае, когда между квантовой системой
и налетающей частицей осуществляется
сильное взаимодействие, выражение для
гамильтониана этого взаимодействия
можно получить лишь в определенных
модельных приближениях.
2.
Стационарная теория возмущений в
квантовой механике может
применяться для систем, для которых
существует диагонализуемый оператор
Гамильтона и
вклада возмущения: H = H0 +
λH1 при
этом параметр λ должен быть
настолько маленьким, чтобы нарушение
не слишком искажало спектр H0,
однако для этого не имеется никаких
точных правил. В теории возмущений
решение представляется в виде![]()
![]() Конечно,
должно быть выполненоуравнение
Шрёдингера:
Конечно,
должно быть выполненоуравнение
Шрёдингера:![]() Подставляя
разложение в это уравнение, получим
Подставляя
разложение в это уравнение, получим![]()
![]() Собирая
слагаемые одинакового порядка по λ,
получим последовательности уравнений
Собирая
слагаемые одинакового порядка по λ,
получим последовательности уравнений![]()
![]()
![]() и
т.д. Эти уравнения должны решаться
последовательно для получения
и
т.д. Эти уравнения должны решаться
последовательно для получения![]() иnk.
Слагаемое с индексом k =
0 - это решение для невозмущённого
уравнения Шрёдингера, поэтому говорят
также о "приближении нулевого
порядка". Аналогично говорят о
"приближении k-го порядка", если
рассчитывают решение до слагаемых
иnk.
Слагаемое с индексом k =
0 - это решение для невозмущённого
уравнения Шрёдингера, поэтому говорят
также о "приближении нулевого
порядка". Аналогично говорят о
"приближении k-го порядка", если
рассчитывают решение до слагаемых ![]() иnk.
второго уравнения получаем, что можно
определяться однозначно решения
для n1 только
с дополнительными условиями, так как
каждая линейная
комбинация n1 и n0 является
решением. Возникает вопрос о нормализиции.
Так как мы можем предположить, что
иnk.
второго уравнения получаем, что можно
определяться однозначно решения
для n1 только
с дополнительными условиями, так как
каждая линейная
комбинация n1 и n0 является
решением. Возникает вопрос о нормализиции.
Так как мы можем предположить, что ![]() ,
но в то же время теория из посылок теории
возмущений следует
,
но в то же время теория из посылок теории
возмущений следует![]() .
Тогда в первом порядке (по параметру
λ) для условия нормировки нужно
положить
.
Тогда в первом порядке (по параметру
λ) для условия нормировки нужно
положить![]() .
Поскольку выбор фазы в квантовой
механике произволен можно без потери
общности сказать, что число
.
Поскольку выбор фазы в квантовой
механике произволен можно без потери
общности сказать, что число![]() реально.
Поэтому
реально.
Поэтому![]() ,
и как следствие налагаемое дополнительное
условие примет вид:
,
и как следствие налагаемое дополнительное
условие примет вид:![]() Так как невозмущённое состояниеn0 должно
быть нормируемо,
сразу следует
Так как невозмущённое состояниеn0 должно
быть нормируемо,
сразу следует![]() и из этого
и из этого![]() Получаем поправку в первом порядке
Получаем поправку в первом порядке![]()
![]() и
для поправки энергии во втором порядке
и
для поправки энергии во втором порядке![]()
3. Молекулы. Энергия молекулы. Молекулярные спектры.Моле́кула (новолат. molecula, уменьшительное от лат. moles — масса) — наименьшая частица химического вещества, обладающая всеми его химическими свойствами[1]. Молекула состоит из двух или более атомов, характеризуется количеством входящих в неё атомных ядер и электронов, а также определённой структурой. Обычно подразумевается, что молекулы нейтральны (не несут электрических зарядов) и не несут неспаренных электронов (все валентности насыщены); заряженные молекулы называют ионами, молекулы с мультиплетностью, отличной от единицы (то есть с неспаренными электронами и ненасыщенными валентностями) — радикалами. Молекулы, образованные сотнями или тысячами атомов, называются макромолекулами. Особенности строения молекул определяют физические свойства вещества, состоящего из этих молекул. К веществам, сохраняющим молекулярную структуру в твердом состоянии, относятся, например, вода, оксид углерода (IV), многие органические вещества. Они характеризуются низкими температурами плавления и кипения. Большинство же твердых (кристаллических) неорганических веществ состоят не из молекул, а из других частиц (ионов, атомов) и существуют в виде макротел (кристалл хлорида натрия, кусок меди и т. д.)[1]. Состав молекул сложных веществ выражается при помощи химических формул[1] [Энергия молекулы – нет, точнее есть, но очень много]
Молекулярные спектры, оптические спектры испускания и поглощения, а также комбинационного рассеяния света, принадлежащие свободным или слабо связанным между собой молекулам. Молекулярные спектры имеют сложную структуру. Типичные Молекулярные спектры - полосатые, они наблюдаются в испускании и поглощении и в комбинационном рассеянии в виде совокупности более или менее узких полос в ультрафиолетовой, видимой и близкой инфракрасной областях, распадающихся при достаточной разрешающей силе применяемых спектральных приборов на совокупность тесно расположенных линий. Конкретная структура Молекулярные спектры различна для различных молекул и, вообще говоря, усложняется с увеличением числа атомов в молекуле. Для весьма сложных молекул видимые и ультрафиолетовые спектры состоят из немногих широких сплошных полос; спектры таких молекул сходны между собой. Молекулярные спектры возникают при квантовых переходах между уровнями энергии E‘ и E‘’ молекул согласно соотношению hn = E‘ - E‘’, (1) где hn - энергия испускаемого поглощаемого фотона частоты n (h - Планка постоянная). При комбинационном рассеянии hn равно разности энергий падающего и рассеянного фотонов. Молекулярные спектры гораздо сложнее линейчатых атомных спектров, что определяется большей сложностью внутренних движений в молекуле, чем в атомах. Наряду с движением электронов относительно двух или более ядер в молекулах происходят колебательное движение ядер (вместе с окружающими их внутренними электронами) около положений равновесия и вращательное движение молекулы как целого. Этим трём видам движений - электронному, колебательному и вращательному - соответствуют три типа уровней энергии и три типа спектров.
4. Строение атомных ядер. Ядерные силы. Энергия связи ядра. Проблему строения атомного ядра удалось решить лишь после того, как в 1932 г. Д. Чэдвиком (1891-1974) была открыта новая частица - нейтрон. В этом же году советский физик Д. Иваненко и немецкий ученый В. Гей-зенберг (1901-1976) предложили протонно-нейтронную модель ядра. Протон обладает положительным зарядом qp= 1,6-10-19 Кл и массой mр= 1836,2 mе= 1,67 • КГ-27кг = 1,00728 а.е.м. Нейтрон - электрически нейтральная частица (qn= 0), его масса покоя mn = 1838,7 mе= 1,68 • 10-27 кг = 1,00867 а.е.м. В свободном состоянии он неустойчив: распадается на протон, электрон и антинейтрино. Его время жизни ~ 103 с. Число протонов в ядре равно атомному номеру химического элемента в периодической таблице Д. Менделеева - z. Число нейтронов в ядре определяется как разность между общим числом А всех частиц в ядре и количеством протонов в нем: N =А - z, где А - массовое число, число нуклонов в ядре. Нуклонами называются нейтроны и протоны, входящие в состав атомного ядра. Ядро, или атом, обозначается как Azх, где х - химический символ элемента, например 168 О.
ЯДЕРНЫЕ
СИЛЫ, силы, удерживающие нуклоны
(протоны и нейтроны) в ядре. Ядерные
силы действуют только на расстояниях
не более 10-13 см, в 100-1000 раз превышают
силу взаимодействия электрических
зарядов и не зависят от заряда нуклонов.
Ядерные силы обусловлены сильным
взаимодействием (смотри Взаимодействия
фундаментальные).
Энергия
связи ядра –
минимальная энергия, необходимая для
того, чтобы разделить ядро на составляющие
его нуклоны (протоны и нейтроны). Ядро
– система связанных нуклонов, состоящая
из Z протонов (масса протона в свободном
состоянии mp)
и N нейтронов (масса нейтрона в свободном
состоянии mn).
Для того, чтобы разделить ядро на
составные нуклоны, нужно затратить
определенную минимальную энергию W,
называемую энергией связи. При этом
покоящееся ядро с массой М переходит
в совокупность свободных покоящихся
протонов и нейтронов с суммарной массой
Zmp + Nmn.
Энергия покоящегося ядра Мс2.
Энергия освобождённых покоящихся
нуклонов (Zmp
+ Nmn)с2.
В соответствии с законом сохранения
энергии Мс2 + W = (Zmp + Nmn)с2.
Или W = (Zmp + Nmn)с2
- Мс2.
Поскольку W > 0, то М <
(Zmp + Nmn),
т.е. масса, начального ядра, в котором
нуклоны связаны, меньше суммы масс
свободных нуклонов, входящих в его
состав.
W растёт с увеличением
числа А нуклонов в ядре (А = Z + N). Удобно
иметь дело с удельной энергией связи
![]() =
W/A, т.е. средней энергией связи, приходящейся
на один нуклон. Для большинства ядер
=
W/A, т.е. средней энергией связи, приходящейся
на один нуклон. Для большинства ядер![]()
![]() 8
МэВ (1 МэВ = 1.6.10-13
Дж). Для разрыва химической связи нужна
энергия в 106
раз меньше.
8
МэВ (1 МэВ = 1.6.10-13
Дж). Для разрыва химической связи нужна
энергия в 106
раз меньше.
5.Радиоакти́вность (от лат. radius «луч» и āctīvus «действенный») — свойство атомных ядер самопроизвольно (спонтанно) изменять свой состав (заряд Z, массовое число A) путём испусканияэлементарных частиц или ядерных фрагментов[1]. Соответствующее явление называется радиоакти́вным распа́дом. Радиоактивностью называют также свойство вещества, содержащего радиоактивные ядра.
Установлено, что радиоактивны все химические элементы с порядковым номером, большим 82 (то есть начиная с висмута), и многие более лёгкие элементы (прометий и технеций не имеют стабильных изотопов, а у некоторых элементов, таких как индий, калий или кальций, часть природных изотопов стабильны, другие же радиоактивны).
Естественная радиоактивность — самопроизвольный распад ядер элементов, встречающихся в природе.
Искусственная радиоактивность — самопроизвольный распад ядер элементов, полученных искусственным путем через соответствующие ядерные реакции.
Специальные виды радиоактивности - Спонтанное деление,Кластерная радиоактивность,Протонная радиоактивность,Двухпротонная радиоактивность,Нейтронная радиоактивность (блин(( не знаю как полоску убрать(()Ооооо убралась))
Беккере́ль (обозначение: Бк, Bq) — единица измерения активности в СИ.
Беккерель это такая активность данного количества вещества, при которой, в среднем, за одну секунду происходит один радиоактивный распад. Через другие единицы измерения СИ беккерель выражается следующим образом:
Бк = с−1
Кюри́ (обозначение: Ки, Ci) — внесистемная единица измерения активности.
Радиоактивность вещества равна 1 Ки, если в нём каждую секунду происходит 3,7×1010 радиоактивных распадов. Таким образом:
1 Ки = 3,7×1010 Бк
1 Бк = 2,7027×10−11 Ки.
Махе — устаревшая внесистемная единица объёмной альфа-активности радиоактивного источника. Равна активности радионуклида, содержащегося в 1 л вещества и обеспечивающего посредством ионизации среды альфа-частицамиионизационный ток насыщения, равный 10−3 единицы СГС (то есть 3,336×10−13 А). Таким образом, один махе создаёт в 1 л вещества мощность экспозиционной дозы облучения, равную 1 микрорентгену в секунду, или 3,6 миллирентгена в час.
Альфа-распад
α-распадом называют самопроизвольный распад атомного ядра на дочернее ядро и α-частицу (ядро атома 4He).
α-распад, как правило, происходит в тяжёлых ядрах с массовым числом А≥140 (хотя есть несколько исключений). Внутри тяжёлых ядер за счёт свойства насыщения ядерных сил образуются обособленные α-частицы, состоящие из двух протонов и двух нейтронов. Образовавшаяся α-частица подвержена большему действию кулоновских сил отталкивания от протонов ядра, чем отдельные протоны. Одновременно α-частица испытывает меньшее ядерное притяжение к нуклонам ядра, чем остальные нуклоны. Образовавшаяся альфа-частица на границе ядра отражается от потенциального барьера внутрь, однако с некоторой вероятностью она может преодолеть его (см. Туннельный эффект) и вылететь наружу. С уменьшением энергии альфа-частицы проницаемость потенциального барьера экспоненциально уменьшается, поэтому время жизни ядер с меньшей доступной энергией альфа-распада при прочих равных условиях больше.
Правило смещения Содди для α-распада:
![]() .
.
Бета-распад
Беккерель
доказал, что β-лучи являются
потоком электронов.
β-распад — это проявление слабого
взаимодействия.β-распад (точнее,
бета-минус-распад, β − -распад) —
это радиоактивный распад, сопровождающийся
испусканием из ядра электрона
и антинейтрино.β-распад
является внутринуклонным процессом.
Он происходит вследствие превращения
одного из d-кварков в
одном из нейтронов ядра
в u-кварк;
при этом происходит превращение нейтрона
в протон с
испусканием электрона и антинейтрино:
![]()
Правило смещения Содди для β − -распада:
![]()
Гамма-распад (изомерный переход)Почти все ядра имеют, кроме основного квантового состояния, дискретный набор возбуждённых состояний с большей энергией (исключением являются ядра 1H, 2H, 3H и 3He). Возбуждённые состояния могут заселяться при ядерных реакциях либо радиоактивном распаде других ядер. Большинство возбуждённых состояний имеют очень малые времена жизни (менее наносекунды). Однако существуют и достаточно долгоживущие состояния (чьи времена жизни измеряются микросекундами, сутками или годами), которые называются изомерными, хотя граница между ними и короткоживущими состояниями весьма условна. Изомерные состояния ядер, как правило, распадаются в основное состояние (иногда через несколько промежуточных состояний). При этом излучаются один или несколько гамма-квантов; возбуждение ядра может сниматься также посредством вылета конверсионных электронов из атомной оболочки. Изомерные состояния могут распадаться также и посредством обычных бета- и альфа-распадов.
|
6. Ядерная реакция – это процесс взаимодействия атомного ядра с другим ядром или элементарной частицей, сопровождающийся изменением состава и структуры ядра и выделением вторичных частиц или γ-квантов. Первая ядерная реакция была осуществлена Э. Резерфордом в 1919 году в опытах по обнаружению протонов в продуктах распада ядер. При ядерных реакциях выполняется несколько законов сохранения: импульса, энергии, момента импульса, заряда. В дополнение к этим классическим законам сохранения при ядерных реакциях выполняется закон сохранения так называемого барионного заряда (то есть числа нуклонов – протонов и нейтронов). Ядерные реакции сопровождаются энергетическими превращениями. Энергетическим выходом ядерной реакции называется величина Q = (MA + MB – MC – MD)c2 = ΔMc2. |
где
MA
и MB
– массы исходных продуктов, MC
и MD
– массы конечных продуктов реакции.
Величина ΔM называется дефектом
масс.
Реакция слияния легких ядер при очень
высокой температуре, сопровождающаяся
выделением энергии, называется
термоядерной реакцией. Для слияния
необходимо, чтобы расстояние между
ядрами приблизительно было равно 0,000
000 000 001 см. Однако этому препятствуют
кулоновские силы. Они могут быть
преодолены при наличии у ядер большой
кинетической энергии. Особенно большое
практическое значение имеет то, что
при термоядерной реакции на каждый
нуклон выделяется намного больше
энергии, чем при ядерной реакции,
например, при синтезе ядра гелия из
ядер водорода выделяется энергия,
равная 6 МэВ, а при делении ядра урана
на один нуклон приходится »0,9 МэВ.
Управляемая термоядерная реакция -
энергетически выгодная реакция. Однако
она может идти лишь при очень высоких
температурах (порядка несколько сотен
млн. градусов). При большой плотности
вещества такая температура может быть
достигнута путем создания в плазме
мощных электронных разрядов. При этом
возникает проблема - трудно удержать
плазму. Самоподдерживающиеся термоядерные
реакции происходят в звездах. Деление
тяжелых ядер. В отличие от радиоактивного
распада ядер, сопровождающегося
испусканием α- или β-частиц, реакции
деления – это процесс, при котором
нестабильное ядро делится на два крупных
фрагмента сравнимых масс. В 1939 году
немецкими учеными О. Ганом
и Ф. Штрассманом
было открыто деление ядер урана.
Продолжая исследования, начатые Ферми,
они установили, что при бомбардировке
урана нейтронами возникают элементы
средней части периодической системы
– радиоактивные изотопы бария (Z = 56),
криптона (Z = 36) и др. Основной
интерес для ядерной энергетики
представляет реакция деления ядра
![]() В
настоящее время известны около 100
различных изотопов с массовыми числами
примерно от 90 до 145, возникающих при
делении этого ядра. Две типичные реакции
деления этого ядра имеют вид:
В
настоящее время известны около 100
различных изотопов с массовыми числами
примерно от 90 до 145, возникающих при
делении этого ядра. Две типичные реакции
деления этого ядра имеют вид: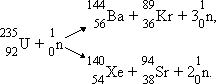
7. Элементарные частицы.
Существование элементарных частиц физики обнаружили при изучении ядерных процессов, поэтому вплоть до середины XX века физика элементарных частиц была разделом ядерной физики. Главная задача физики элементарных частиц – это исследование природы, свойств и взаимных превращений элементарных частиц.
Впервые мысль о существовании мельчайших невидимых частиц, из которых состоят все окружающие предметы, была высказана за 400 лет до нашей эры греческим философом Демокритом. Он назвал эти частицы атомами, то есть неделимыми частицами. Наука начала использовать представление об атомах только в начале XIX века, когда на этой основе удалось объяснить целый ряд химических явлений. В 30-е годы XIX века в теории электролиза, развитой М. Фарадеем, появилось понятие иона и было выполнено измерение элементарного заряда. Конец XIX века ознаменовался открытием явления радиоактивности (А. Беккерель, 1896 г.), а также открытиями электронов (Дж. Томсон, 1897 г.) и α-частиц (Э. Резерфорд, 1899 г.). В 1905 году в физике возникло представление о квантах электромагнитного поля – фотонах (А. Эйнштейн).
В 1911 году было открыто атомное ядро (Э. Резерфорд) и окончательно было доказано, что атомы имеют сложное строение. В 1919 году Резерфорд в продуктах расщепления ядер атомов ряда элементов обнаружил протоны. В 1932 году Дж. Чедвик открыл нейтрон. Стало ясно, что ядра атомов, как и сами атомы, имеют сложное строение. Возникла протон-нейтронная теория строения ядер (Д. Д. Иваненко и В. Гейзенберг). В том же 1932 году в космических лучах был открыт позитрон (К. Андерсон). Позитрон – положительно заряженная частица, имеющая ту же массу и тот же (по модулю) заряд, что и электрон. Существование позитрона было предсказано П. Дираком в 1928 году. В эти годы были обнаружены и исследованы взаимные превращения протонов и нейтронов и стало ясно, что эти частицы также не являются неизменными элементарными «кирпичиками» природы. В 1937 году в космических лучах были обнаружены частицы с массой в 207 электронных масс, названные мюонами (μ-мезонами). Затем в 1947–1950 годах были открыты пионы (то есть π-мезоны), которые, по современным представлениям, осуществляют взаимодействие между нуклонами в ядре. В последующие годы число вновь открываемых частиц стало быстро расти. Этому способствовали исследования космических лучей, развитие ускорительной техники и изучение ядерных реакций.
В настоящее время известно около 400 субъядерных частиц, которые принято называть элементарными. Наука начала использовать представление об атомах только в начале XIX века, когда на этой основе удалось объяснить целый ряд химических явлений. В 30-е годы XIX века в теории электролиза, развитой М. Фарадеем, появилось понятие иона и было выполнено измерение элементарного заряда. Конец XIX века ознаменовался открытием явления радиоактивности (А. Беккерель, 1896 г.), а также открытиями электронов (Дж. Томсон, 1897 г.) и α-частиц (Э. Резерфорд, 1899 г.). В 1905 году в физике возникло представление о квантах электромагнитного поля – фотонах (А. Эйнштейн). В 1911 году было открыто атомное ядро (Э. Резерфорд) и окончательно было доказано, что атомы имеют сложное строение. В 1919 году Резерфорд в продуктах расщепления ядер атомов ряда элементов обнаружил протоны. В 1932 году Дж. Чедвик открыл нейтрон. Стало ясно, что ядра атомов, как и сами атомы, имеют сложное строение. Возникла протон-нейтронная теория строения ядер (Д. Д. Иваненко и В. Гейзенберг). В том же 1932 году в космических лучах был открыт позитрон (К. Андерсон). Позитрон – положительно заряженная частица, имеющая ту же массу и тот же (по модулю) заряд, что и электрон. Существование позитрона было предсказано П. Дираком в 1928 году. В 1937 году в космических лучах были обнаружены частицы с массой в 207 электронных масс, названные мюонами (μ-мезонами). Затем в 1947–1950 годах были открыты пионы (то есть π-мезоны), которые, по современным представлениям, осуществляют взаимодействие между нуклонами в ядре. В последующие годы число вновь открываемых частиц стало быстро расти. Этому способствовали исследования космических лучей, развитие ускорительной техники и изучение ядерных реакций. В настоящее время известно около 400 субъядерных частиц, которые принято называть элементарными.
8.
БОЗЕ-ЭЙНШТЕЙНА РАСПРЕДЕЛЕНИЕ- функция
распределения по уровням энергии
тождеств. частиц с нулевым или целочисл.
спином при условии, что взаимодействие
частиц слабое и им можно пренебречь,
т. е. ф-ция распределения идеального
квантового газа, подчиняющегося Бозе
- Эйнштейна статистике.В
случае статистич. равновесия ср.
число ![]() таких
частиц в состоянии с энергией ei при
темп-ре T выше вырождения
температурыопределяется
Б.-Э. р.
таких
частиц в состоянии с энергией ei при
темп-ре T выше вырождения
температурыопределяется
Б.-Э. р. ![]() где
где![]() -
набор квантовых чисел, характеризующих
состояние частицы,
-
набор квантовых чисел, характеризующих
состояние частицы,![]() -
хим. потенциал.Б.- Э. р. соответствует
максимумустатистического
веса (или
энтропии) с учётом неразличимости
частиц, отвечающей требованиям
бозе-статистики. При темп-ре ниже темп-ры
вырождения бозе-газ испытывает Бозе- Эйнштейна
конденсацию, при
к-рой часть частиц Скапливается в
состоянии с нулевым импульсом, а
остальные частицы распределены согласно
Б.- Э. р. с
-
хим. потенциал.Б.- Э. р. соответствует
максимумустатистического
веса (или
энтропии) с учётом неразличимости
частиц, отвечающей требованиям
бозе-статистики. При темп-ре ниже темп-ры
вырождения бозе-газ испытывает Бозе- Эйнштейна
конденсацию, при
к-рой часть частиц Скапливается в
состоянии с нулевым импульсом, а
остальные частицы распределены согласно
Б.- Э. р. с ![]() формула, описывающая распределение по
уровням энергии тождеств. ч-ц с нулевым
или целочисл. спином при условии, что
вз-ствие ч-ц в системе слабое и им можно
пренебречь.
формула, описывающая распределение по
уровням энергии тождеств. ч-ц с нулевым
или целочисл. спином при условии, что
вз-ствие ч-ц в системе слабое и им можно
пренебречь.
В случае статистического равновесия ср. число ni таких ч-ц в состоянии с энергией ?i (выше вырождения температуры) определяется Б.— Э. р.: ni=1l(e(?i-m)/kT-1), где i — набор квант. чисел, характеризующих состояние ч-цы, m — химический потенциал
