
- •Свириденко о.Ф Конспект лекцій з фізики
- •Основи молекулярної фізики
- •Частина і. Основи молекулярно-кінетичної теорії
- •Тема 1. Основні положення і поняття мкт будови речовини
- •Приклади розв’язування задач
- •Питання для самоперевірки
- •Тема 2. Властивості ідеального газу
- •3. Мікропараметри газу
- •2. Наслідки ор мкт іг
- •7. Види термодинамічних процесів
- •Приклади розв’язування задач
- •8. Методика розв’язування графічних задач на ізопроцеси
- •Питання для самоперевірки
- •Тема 3. Властивості пари
- •1. Властивості випаровування
- •2. Випаровування рідини у герметично закритій посудині
- •3. Властивості насиченої пари
- •Приклади розв’язування задач
- •Питання для самоперевірки
- •Тема 4. Властивості рідин
- •1. Характеристика рідкого стану речовини
- •2. Поверхневий шар рідини
- •3. Спостереження явища поверхневого натягу
- •3. Поняття про в’язкість середовища
- •Приклади розв’язування задач
- •Питання для самоперевірки
- •Тема 5. Властивості Твердого стану речовини
- •2. Ізотропія та анізотропія
- •3. Механічні властивості.
- •2. Класифікація твердих тіл і їх властивості
- •4. Типи кристалів
- •Характеристика різних типів кристалів за типами їх решіток
- •1. Види деформації
- •Пружні – зникають після зняття навантаження, внаслідок чого форма і розміри тіл повністю відновлюються.
- •2. Кількісна характеристика деформації
- •3. Закон пружних деформацій (закон Гука)
- •7. Плавлення і кристалізація
- •9. Теплове розширення тіл
- •Приклади розв’язування задач
- •Питання для самоперевірки
- •Тема 1. Внутрішня енергія і способи її зміни
- •Термодинаміка (тд) вивчає теплові явища і процеси, не враховуючи молекулярну будову речовини.
- •Приклади розв’язування задач
- •ПЩо таке внутрішня енергія?Що називають тепловим двигуном?итання для самоперевірки
- •Тема 2. Закони термодинаміки
- •1. І закон термодинаміки (і зтд) – це закон збереження і перетворення енергії при теплових процесах.
- •3. Застосування і зтд до ізопроцесів
- •Приклади розв’язування задач
- •Питання для самоперевірки
- •Тема 3. Теплові машини (двигуни)
- •3. Цикл Карно
- •4. Способи підвищення ккд тм
- •5. Застосування тм
- •6. Проблеми екології довкілля, пов’язані з використанням тм
- •7. Шляхи зниження шкідливого впливу роботи тм
- •Принцип дії холодильної машини
- •Приклади розв’язування задач
- •ПЩо таке внутрішня енергія?Що називають тепловим двигуном?итання для самоперевірки
- •Рекомендовані джерела інформації
Тема 4. Властивості рідин
1. Характеристика рідкого стану речовини
1. Рідина – агрегатний стан речовини, що займає проміжне положення між твердим і газоподібним, чим пояснюється те, що рідина має деякі властивості, характерні і для твердого тіла, і для газу. Але рідина має ряд притаманних лише їй властивостей.
2. Властивості рідини:
Займає певний об’єм, бо Ēк < Ēп (обумовлено міжмолекулярною взаємодією, у мікрооб’ємі молекули розміщені у певному порядку, у макрооб’ємі такого порядку немає, кажуть, що у рідин існує ближній порядок у розміщенні молекул; таку будову називають квазікристалічною).
Текучість (рідина не зберігає форму, бо молекули „перескакують” з одного місця на інше; час між двома послідовними „перескоками” – час осілого життя – залежить від роду рідини і температури: τ ~ 10-12 ÷ 10-10 с).
Нестисливість (бо великий молекулярний тиск).
Спричиняють поверхневий натяг (пов’язано з відмінністю взаємодії молекул рідини на поверхні і всередині рідини).
В’язкість.
Пружність, крихкість (коли tдії < τ, бо час взаємодії дуже малий).
Кавітація – утворення розривів (порожнин) всередині рідини, в якій немає сторонніх речовин, при інтенсивній дії на неї (наприклад, при обертанні гребних гвинтів, поширенні в рідині ультразвукових хвиль). Такі порожнини всередині рідини довго існувати не можуть і з силою закриваються.
2. Поверхневий шар рідини
Молекулярний тиск
Властивості поверхневого шару рідини відрізняються від властивостей інших шарів рідини, тому що молекули на поверхні рідини перебувають в інших умовах, ніж молекули всередині рідини.

Кожна молекула, розміщена всередині рідини (типу молекули М1, рис.17), рівномірно оточена сусідніми молекулами і взаємодіє з ними, а рівнодійна цих сил дорівнює нулю. На молекули у поверхневому шарі рідини (типу М2) діють її сусіди результуючими силами
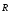 ,
які прагнуть втягти молекули всередину
рідини, оскільки кількість молекул,
що її оточують з усіх сторін неоднакова.
Але простір всередині рідини зайнятий
іншими молекулами, томуповерхневий
шар створює тиск на рідину, який
називають
молекулярним
тиском.
,
які прагнуть втягти молекули всередину
рідини, оскільки кількість молекул,
що її оточують з усіх сторін неоднакова.
Але простір всередині рідини зайнятий
іншими молекулами, томуповерхневий
шар створює тиск на рідину, який
називають
молекулярним
тиском.
Рис. 17
На практиці виміряти цей тиск майже неможливо (при внесенні тіла у рідину виникає шар молекул рідини, в якому молекулярні сили напрямлені від тіла всередину рідини, тобто стискають рідину, а на тіло не діють). Теоретичні розрахунки показують: рм ~ 108 Па.
Енергія поверхневого шару рідини
Молекули, що знаходяться на поверхні рідини, взаємодіють зі значно меншою кількістю молекул, ніж ті, що знаходяться всередині рідини. Тому у них існує надлишок потенціальної енергії ΔЕп. Її називають вільною (або поверхневою). За рахунок вільної енергії виконується робота молекулярних сил А по скороченню площі вільної поверхні рідини:
∆Еп = А = σ∆S (35)
При виконанні цієї роботи механічна енергія переходить у внутрішню.
Явище скорочення площі вільної поверхні рідини внаслідок взаємодії молекул рідини називається явищем поверхневого натягу.
Будь-яка система прагне перейти у стан з мінімальною потенціальною енергією. Цим і пояснюється скорочення поверхні рідини у вільному стані і виникнення сил поверхневого натягу. Отже, „природна” форма рідини – сфера (бо при даному об’ємі мінімальну площу із усіх тіл має сфера).
Сили поверхневого натягу
Коли сили молекулярної взаємодії „втягують” молекулу з поверхневого шару всередину рідини, то виникають сили, які намагаються „закрити вільне місце”, тим самим „стягуючи” вільну поверхню рідини. Такі сили Fн, зумовлені взаємодією молекул рідини, які спричиняють скорочення площі її вільної поверхні і напрямлені по дотичній до цієї поверхні (тобто перпендикулярно до лінії, що окреслює поверхню рідини), називаються силами поверхневого натягу


Рис. 18
Пояснення сил поверхневого натягу
Fн = σl (36)
де σ – коефіцієнт поверхневого натягу, l – довжина лінії, що охоплює вільну поверхню рідини по периметру. В залежності від форми тіла, поміщеного у рідину довжина лінії визначається так:
Прямокутник
Пластинка
Циліндр
Кільце
b

a
b

D

D

d
l = a + b
l = 2b
l = πD
l = π (D + d)
Коефіцієнт поверхневого натягу
Коефіцієнт поверхневого натягу σ виражає залежність роботи молекулярних сил по скороченню площі вільної поверхні рідини і сили поверхневого натягу від роду рідини і зовнішніх умов. Із формул (35) і (36) його можна виразити так:
σ
0 Ткре Ткрв Т
Рис. 19

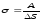 (37)
(37)
вода
або
 (38)
(38)
ефір
Звідки маємо дві одиниці вимірювання:

Коефіцієнт поверхневого натягу залежить від:
роду рідини

температури

домішок

