
- •Кафедра фармацевтической химии
- •Методические указания
- •Определение чистоты лекарственных средств
- •Учебные цели
- •Методические указания студентам
- •Основныеположения
- •Лекарственные средства: натрия хлорид, вода очищенная; индикаторы, реактивы. Приложения
- •Общие фармакопейные статьи
- •Фармацевтические субстанции
- •1. Общие положения
- •Испытания на чистоту и допустимые пределы
- •Испытания на чистоту и допустимые пределы примесей
- •Испытание на хлориды
- •Испытание на сульфаты
- •Испытания на соли аммония
- •Испытания на соли кальция
- •Определение кальция в неорганических соединениях
- •Испытание на соли железа
- •Испытания на соли цинка
- •Испытание на соли тяжелых металлов
- •Определение тяжелых металлов в растворах препаратов
- •Определение тяжелых металлов в зольном остатке органических препаратов
- •ЖелезО (офс 42-0058-07 гФxii)
- •Определение железа в растворах лекарственных средств
- •Стандартные растворы железо(III)-иона
- •ТяжелЫе металлы (офс 42-0059-07 гфxii)
- •Определение тяжелых металлов в растворах лекарственных средств
- •Определение тяжелых металлов в зольном остатке органических лекарственных средств
- •Стандартные растворы свинец-иона
- •Определение летучих веществ и воды (гф XI) Метод высушивания
- •Определение воды
- •Метод титрования реактивом к. Фишера
- •Степень окраски жидкостей (офс 42-0050-07 гф XII)
- •Метод 1
- •Метод 2
- •Приготовление исходных растворов
- •Приготовление стандартных растворов
- •Стандартные растворы
- •Приготовление эталонов
- •Эталоны коричневых оттенков (шкала в)
- •Прозрачность и степень мутности жидкостей
- •Остаточные органические растворители
- •Предельно допустимое содержание в лекарственных средствах остаточных органических растворителей 1 класса токсичности
- •Предельно допустимое содержание в лекарственных средствах остаточных органических растворителей 2 класса токсичности
- •Растворители 3 класса токсичности, которые подлежат нормированию в соответствии с требованиями настоящей офс
- •Фармакопейные статьи
- •Глюкоза
- •Испытание проводят для субстанции, предназначенной для приготовления инъекционных лекарственных форм.
- •Ксантинола никотинат
- •Натрия хлорид
- •Фармакопейная статья предприятия открытое акционерное общество «востоквит»
- •Испытание проводят для субстанции, предназначенной для приготовления стерильных лекарственных форм.
- •Испытание проводят для субстанции, предназначенной для приготовления инъекционных лекарственных форм.
- •По организации хранения в аптечных учреждениях различных групп лекарственных средств и изделий медицинского назначения
- •1. Утверждаю:
- •2. Приказываю:
- •Инструкция по организации хранения в аптечных учреждениях различных групп лекарственных средств и изделий медицинского назначения
- •1. Вводная часть
- •2. Требования к устройству и эксплуатация помещений хранения.
- •3. Общее требования к организации хранения лекарственных средств я изделий медицинского назначения.
- •4. Требования, предъявляемые к хранению различных групп лекарственных средств я изделий медицинского назначения.
- •4.1. Особенности хранения лекарственных средств, требующих защиты света.
- •4.2. Особенности хранения лекарственных средств, требующих защиты от влаги.
- •4.6. Особенности хранения лекарственных средств, требующих защиты от воздействия пониженной температуры.
- •4.7. Особенности хранения лекарственных средств, требующих защиты от воздействия газов, содержащихся в окружающей среде
- •4.8. Особенности хранения пахучих и красящих лекарственных средств и парафармацевтической продукции.
- •4.9. Особенности хранения готовых лекарственных средств.
- •5. Особенности хранения лекарственного растительного сырья.
- •6. Дезинфицирующие средства.
- •7. Общие правила подготовки лекарственных средств и изделий медицинского назначения к использованию после хранения.
- •8. Хранение изделий медицинского назначения.
- •9. Пластмассовые изделия.
- •10. Перевязочные средства и вспомогательный материал
- •11. Изделия медицинской техники.
- •12. Медицинские пиявки.
- •13. Требования к таре для лекарственных средств и изделий
Испытание проводят для субстанции, предназначенной для приготовления инъекционных лекарственных форм.
Микробиологическая чистота. В соответствии с требованиями ОФС «Микробиологическая чистота».
Количественное определение. Определение проводят методом ВЭЖХ.
Фосфатный буферный раствор с рН 5,5-5,6. 2,72 г калия фосфата однозамещенного растворяют в 700 мл воды, доводят рН раствора раствором калия гидроксида до 5,5-5,6, доводят объем раствора водой до 1000 мл, перемешивают, фильтруют и дегазируют.
Испытуемый раствор. Около 0,05 г (точная навеска) субстанции помещают в мерную колбу вместимостью 50 мл, растворяют в подвижной фазе (ПФ), доводят объем раствора ПФ до метки и перемешивают.
Стандартный раствор. Около 0,05 г (точная навеска) ГСО рибоксина помещают в мерную колбу вместимостью 50 мл, растворяют в ПФ, доводят объем раствора ПФ до метки и перемешивают.
Раствор для проверки пригодности системы. 0,002 г гипоксантина и 0,002 г гуанозина растворяют в 10 мл стандартного раствора.
Хроматографические условия
|
Колонка |
- |
15 × 0,39 см с октадецилсилил силикагелем (С18), 5 мкм; |
|
ПФ |
- |
фосфатный буферный раствор с рН 5,5-5,6; |
|
Температура колонки |
- |
50 ºС; |
|
Скорость потока |
- |
0,6 мл/мин; |
|
Детектор |
- |
спектрофотометрический, 254 нм; |
|
Объем пробы |
- |
10 мкл. |
Хроматографируют раствор для проверки пригодности системы. Порядок элюирования компонентов: гипоксантин, рибоксин, гуанозин. Разрешение (R) между соседними пиками должно быть не менее 1,25; эффективность колонки (N), рассчитанная для пика рибоксина, должна быть не менее 3400 теоретических тарелок; хвостовой фактор (Т) пика рибоксина должен быть не более 1,1.
Шесть раз хроматографируют стандартный раствор. Относительное стандартное отклонение для площади пика рибоксина должно быть не более 2 %.
Хроматографируют испытуемый и стандартный растворы.
Содержание C10H12N4O5 в субстанции в пересчете на сухое вещество в процентах (Х) рассчитывают по формуле:
S1 × а0 × Р × 100
X = ————––––––––
S0 × a1 × (100-W)
|
где |
S1 |
- |
площадь пика рибоксина на хроматограмме испытуемого раствора; |
|
|
S0 |
- |
площадь пика рибоксина на хроматограмме стандартного раствора; |
|
|
a1 |
- |
навеска субстанции в граммах; |
|
|
а0 |
- |
навеска ГСО рибоксина в граммах; |
|
|
Р |
- |
содержание C10H12N4O5 в ГСО рибоксина в процентах; |
|
|
W |
- |
потеря в массе при высушивании субстанции в процентах. |
Хранение. В сухом, защищенном от света месте.
Сульфадиметоксин (ФС 42-0278-07)
4-Амино-N-(2,6-диметоксипиримидин-4-ил)бензолсульфонамид
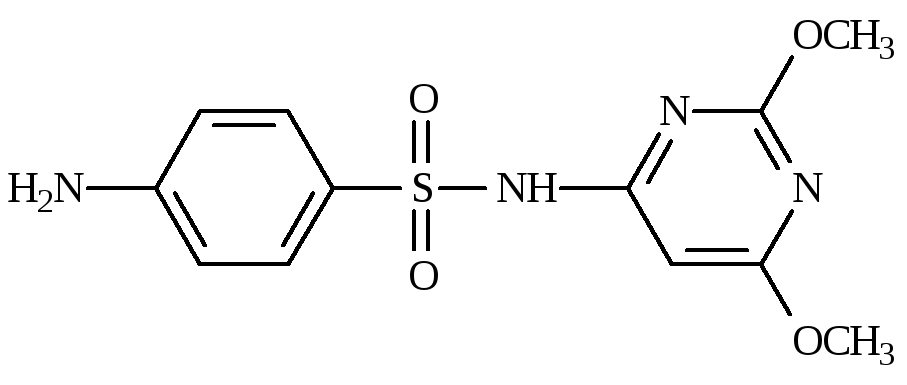
|
C12H14N4O4S |
М.м. 310,33 |
Cодержит не менее 99,0 % C12H14N4O4S в пересчете на сухое вещество.
Описание. Белый или почти белый кристаллический порошок.
Растворимость. Практически нерастворим в воде, очень мало растворим в хлороформе, мало растворим в спирте 95 %, растворим в хлористоводородной кислоте разведенной 8,3 %, легко растворим в растворах едких щелочей.
Подлинность. Инфракрасный спектр субстанции, снятый в диске с калия бромидом, в области от 4000 до 400 см-1 по положению полос поглощения должен соответствовать спектру стандартного образца сульфадиметоксина.
0,075 г субстанции помещают в мерную колбу вместимостью 100 мл, растворяют в 5 мл 0,1 М раствора натрия гидроксида и доводят объем раствора водой до метки. 5 мл полученного раствора разбавляют водой до 250 мл. По 20 мл полученного раствора помещают в две конические колбы, в первую прибавляют 0,4 мл 0,5 М раствора натрия гидроксида, а во вторую 0,4 мл хлористоводородной кислоты концентрированной.
Ультрафиолетовый спектр поглощения щелочного раствора, снятый относительно кислого раствора, в области от 240 до 280 нм должен иметь максимумы при 253 нм и 268 нм и минимум при 260 нм.
Ультрафиолетовый спектр поглощения кислого раствора, снятый относительно щелочного раствора, в области от 285 до 300 нм должен иметь максимум при 288 нм.
Раствор 0,05 г субстанции в 2 мл хлористоводородной кислоты концентрированной дает характерную реакцию на первичные ароматические амины.
Температура плавления. От 198 до 204 ºС.
Прозрачность раствора. Раствор 0,4 г субстанции в 10 мл 1 М раствора натрия гидроксида должен быть прозрачным или выдерживать сравнение с эталоном I.
Цветность раствора. Раствор, полученный в испытании на Прозрачность раствора, должен быть бесцветным или выдерживать сравнение с эталоном В9.
Кислотность. 1 г субстанции нагревают при температуре 70 ºС с 50 мл воды, свободной от углекислого газа, в течение 5 мин, быстро охлаждают и фильтруют. На титрование 25 мл фильтрата должно пойти не более 0,1 мл 0,1 М раствора натрия гидроксида (индикатор 0,1 мл 0,04 % раствора бромтимолового синего).
Посторонние примеси. Испытание проводят методом ТСХ.
Испытуемый раствор. 0,1 г субстанции растворяют в смеси спирт 96 % - раствор аммиака концентрированный 25 % (9:1) и разбавляют той же смесью до 10 мл.
Раствор сравнения. 0,005 г сульфаниламида растворяют в смеси спирт 96 % - раствор аммиака концентрированный 25 % (9:1) и разбавляют той же смесью до 100 мл.
Раствор для опрыскивания. 0,02 г диметиламинобензальдегида растворяют в 20 мл спирта 96 % и прибавляют 0,5 мл хлористоводородной кислоты концентрированной.
На линию старта пластинки со слоем силикагеля 60 F наносят 10 мкл (100 мкг) испытуемого раствора и 10 мкл (0,5 мкг) раствора сравнения. Пластинку с нанесенными пробами сушат на воздухе, помещают в камеру со смесью хлороформ – метанол – диметилформамид (20:2:1) и хроматографируют восходящим методом. Когда фронт подвижной фазы дойдет до конца пластинки, ее вынимают из камеры, сушат при температуре 100 – 105 ºС в течение 10 мин и опрыскивают раствором диметиламинобензальдегида.
На хроматограмме испытуемого раствора пятно, находящееся на уровне пятна сульфаниламида, по совокупности величины и интенсивности окраски не должно превышать пятно на хроматограмме раствора сравнения (не более 0,5 %).
Потеря в массе при высушивании. Около 1,0 г (точная навеска) субстанции сушат при температуре от 100 до 105 ºС до постоянной массы. Потеря в массе не должна превышать 0,5 %.
Хлориды. 0,5 г субстанции встряхивают в течение 3 мин со смесью 0,5 мл азотной кислоты разведенной 16 % и 9,5 мл воды и фильтруют. 4 мл фильтрата, разведенные водой до 10 мл, должны выдерживать испытание на хлориды (не более 0,01 % в субстанции).
Сульфаты. 1 г субстанции встряхивают в течение 3 мин со смесью 0,5 мл хлористоводородной кислоты разведенной 8,3 % и 19,5 мл воды и фильтруют. 10 мл фильтрата должны выдерживать испытание на сульфаты (не более 0,02 % в субстанции).
Сульфатная зола и тяжелые металлы. Сульфатная зола из 1,0 г (точная навеска) субстанции не должна превышать 0,1 % и должна выдерживать испытание на тяжелые металлы (не более 0,001 % в субстанции).
Остаточные органические растворители. В соответствии с требованиями ОФС «Остаточные органические растворители».
Микробиологическая чистота. В соответствии с требованиями ОФС «Микробиологическая чистота».
Количественное определение. Около 0,5 г (точная навеска) субстанции растворяют в смеси 75 мл воды и 10 мл хлористоводородной кислоты концентрированной и титруют нитритометрически. Конец титрования устанавливают по йодкрахмальной бумаге.
1 мл 0,1 М раствора натрия нитрита соответствует 31,03 мг C12H14N4О4S.
Хранение. Список Б. В сухом, защищенном от света месте.
ПРИКАЗ
Министерства здравоохранения Российской Федерации от 13.11.96
№ 377 Об утверждении Инструкции
