
- •Кафедра фармацевтической химии
- •Методические указания
- •Определение чистоты лекарственных средств
- •Учебные цели
- •Методические указания студентам
- •Основныеположения
- •Лекарственные средства: натрия хлорид, вода очищенная; индикаторы, реактивы. Приложения
- •Общие фармакопейные статьи
- •Фармацевтические субстанции
- •1. Общие положения
- •Испытания на чистоту и допустимые пределы
- •Испытания на чистоту и допустимые пределы примесей
- •Испытание на хлориды
- •Испытание на сульфаты
- •Испытания на соли аммония
- •Испытания на соли кальция
- •Определение кальция в неорганических соединениях
- •Испытание на соли железа
- •Испытания на соли цинка
- •Испытание на соли тяжелых металлов
- •Определение тяжелых металлов в растворах препаратов
- •Определение тяжелых металлов в зольном остатке органических препаратов
- •ЖелезО (офс 42-0058-07 гФxii)
- •Определение железа в растворах лекарственных средств
- •Стандартные растворы железо(III)-иона
- •ТяжелЫе металлы (офс 42-0059-07 гфxii)
- •Определение тяжелых металлов в растворах лекарственных средств
- •Определение тяжелых металлов в зольном остатке органических лекарственных средств
- •Стандартные растворы свинец-иона
- •Определение летучих веществ и воды (гф XI) Метод высушивания
- •Определение воды
- •Метод титрования реактивом к. Фишера
- •Степень окраски жидкостей (офс 42-0050-07 гф XII)
- •Метод 1
- •Метод 2
- •Приготовление исходных растворов
- •Приготовление стандартных растворов
- •Стандартные растворы
- •Приготовление эталонов
- •Эталоны коричневых оттенков (шкала в)
- •Прозрачность и степень мутности жидкостей
- •Остаточные органические растворители
- •Предельно допустимое содержание в лекарственных средствах остаточных органических растворителей 1 класса токсичности
- •Предельно допустимое содержание в лекарственных средствах остаточных органических растворителей 2 класса токсичности
- •Растворители 3 класса токсичности, которые подлежат нормированию в соответствии с требованиями настоящей офс
- •Фармакопейные статьи
- •Глюкоза
- •Испытание проводят для субстанции, предназначенной для приготовления инъекционных лекарственных форм.
- •Ксантинола никотинат
- •Натрия хлорид
- •Фармакопейная статья предприятия открытое акционерное общество «востоквит»
- •Испытание проводят для субстанции, предназначенной для приготовления стерильных лекарственных форм.
- •Испытание проводят для субстанции, предназначенной для приготовления инъекционных лекарственных форм.
- •По организации хранения в аптечных учреждениях различных групп лекарственных средств и изделий медицинского назначения
- •1. Утверждаю:
- •2. Приказываю:
- •Инструкция по организации хранения в аптечных учреждениях различных групп лекарственных средств и изделий медицинского назначения
- •1. Вводная часть
- •2. Требования к устройству и эксплуатация помещений хранения.
- •3. Общее требования к организации хранения лекарственных средств я изделий медицинского назначения.
- •4. Требования, предъявляемые к хранению различных групп лекарственных средств я изделий медицинского назначения.
- •4.1. Особенности хранения лекарственных средств, требующих защиты света.
- •4.2. Особенности хранения лекарственных средств, требующих защиты от влаги.
- •4.6. Особенности хранения лекарственных средств, требующих защиты от воздействия пониженной температуры.
- •4.7. Особенности хранения лекарственных средств, требующих защиты от воздействия газов, содержащихся в окружающей среде
- •4.8. Особенности хранения пахучих и красящих лекарственных средств и парафармацевтической продукции.
- •4.9. Особенности хранения готовых лекарственных средств.
- •5. Особенности хранения лекарственного растительного сырья.
- •6. Дезинфицирующие средства.
- •7. Общие правила подготовки лекарственных средств и изделий медицинского назначения к использованию после хранения.
- •8. Хранение изделий медицинского назначения.
- •9. Пластмассовые изделия.
- •10. Перевязочные средства и вспомогательный материал
- •11. Изделия медицинской техники.
- •12. Медицинские пиявки.
- •13. Требования к таре для лекарственных средств и изделий
Испытание проводят для субстанции, предназначенной для приготовления стерильных лекарственных форм.
Микробиологическая чистота. В соответствии с требованиями ОФС «Микробиологическая чистота».
Количественное определение. Около 0,3 г (точная навеска) субстанции растворяют в смеси 10 мл воды и 10 мл хлористоводородной кислоты разведенной 8,3 %. Полученный раствор титруют нитритометрически. Параллельно проводят контрольный опыт.
1 мл 0,1 М раствора натрия нитрита соответствует 27,28 мг C13H20N2O2·HCl.
Хранение. Список Б. В сухом, защищенном от света месте.
Пропранолола гидрохлорид (ФС 42-0273-07)
(RS)-1-(Изопропиламино)-3-(1-нафтилокси)пропан-2-ола гидрохлорид
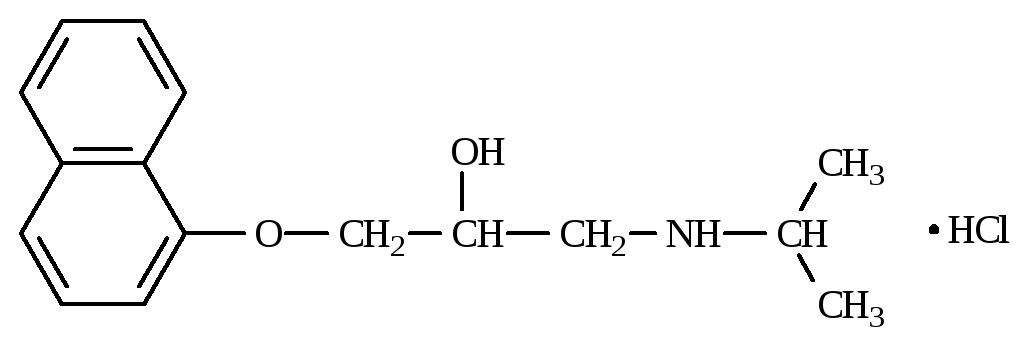
|
C16H21NO2 . HCl |
М.м. 295,81 |
Cодержит не менее 99,0 % и не более 101,0 % C16H21NO2 . HCl в пересчете на сухое вещество.
Описание. Белый или почти белый порошок.
Растворимость. Растворим в воде и спирте 96 %.
Подлинность. Инфракрасный спектр субстанции, снятый в диске с калия бромидом, в области от 4000 до 400 см-1 по положению полос поглощения должен соответствовать спектру стандартного образца пропранолола гидрохлорида.
Субстанция дает характерную реакцию на хлориды.
Температура плавления. От 163 до 166 ºС (метод 1а).
Прозрачность раствора. Раствор 1 г субстанции в 10 мл метанола должен быть прозрачным или выдерживать сравнение с эталоном I.
Цветность раствора. Раствор, полученный в испытании на Прозрачность раствора, должен выдерживать сравнение с эталоном Y6.
Кислотность или щелочность. 0,2 г субстанции растворяют в 20 мл свежепрокипяченной и охлажденной воды, прибавляют 0,2 мл раствора метилового красного и 0,2 мл 0,01 М раствора хлористоводородной кислоты; раствор становится красным. Прибавляют 0,4 мл 0,01 М раствора натрия гидроксида; раствор становится желтым.
Посторонние примеси. Определение проводят методом ВЭЖХ.
Подвижная фаза (ПФ). 1,6 г натрия лаурилсульфата и 0,31 г тетрабутиламмония дигидрофосфата растворяют в смеси 450 мл воды, 550 мл ацетонитрила и 1 мл серной кислоты концентрированной и доводят рН раствора раствором натра едкого до 3,3.
Испытуемый раствор. 0,02 г субстанции растворяют в 10 мл ПФ.
Раствор сравнения. 1 мл испытуемого раствора помещают в мерную колбу вместимостью 50 мл, доводят объем раствора ПФ до метки и перемешивают. 1 мл полученного раствора переносят в мерную колбу вместимостью 10 мл, доводят объем раствора ПФ до метки и перемешивают.
Раствор для проверки пригодности системы. 0,01 г стандартной смеси пропранолола гидрохлорида и примесей (Propranolol hydrochloride for performance test CRS, стандарт ВР) растворяют в 10 мл ПФ.
Хроматографические условия
|
Колонка |
- |
25 × 0,46 см с октадецилсилил силикагелем (С18), 5 мкм; |
|
Скорость потока |
- |
1,8 мл/мин; |
|
Детектор |
- |
спектрофотометрический, 292 нм; |
|
Объем пробы |
- |
20 мкл. |
Хроматографируют раствор для проверки пригодности системы. Полученная хроматограмма по виду и параметрам разделения должна соответствовать хроматограмме, прилагаемой к образцу стандартной смеси.
Хроматографируют раствор сравнения и испытуемый раствор. Время регистрации хроматограммы испытуемого раствора должно не менее чем в 5 раз превышать время удерживания основного пика.
На хроматограмме испытуемого раствора площадь пика любой посторонней примеси должна быть не более половины площади пика пропранолола на хроматограмме раствора сравнения (не более 0,1 %); суммарная площадь пиков посторонних примесей не должна более чем в 2 раза превышать площадь пика пропранолола на хроматограмме раствора сравнения (не более 0,4 %).
Потеря в массе при высушивании. Около 1 г (точная навеска) субстанции сушат при температуре от 100 до 105 ºС до постоянной массы. Потеря в массе не должна превышать 0,5 %.
Сульфатная зола. Не более 0,1 %. Определение проводят из точной навески субстанции около 1 г.
Тяжелые металлы. Сульфатная зола из 0,5 г субстанции должна выдерживать испытание на тяжелые металлы (не более 0,002 % в субстанции).
Остаточные органические растворители. В соответствии с требованиями ОФС «Остаточные органические растворители»
Микробиологическая чистота. В соответствии с требованиями ОФС «Микробиологическая чистота».
Количественное определение. Около 0,25 г (точная навеска) субстанции растворяют в 25 мл спирта 96 % и титруют 0,1 М раствором натрия гидроксида. Конечную точку титрования определяют потенциометри-чески.
1 мл 0,1 М раствора натрия гидроксида соответствует 29,58 мг C16H21NO2 . HCl.
Хранение. Список Б. В плотно закрытой упаковке в защищенном от света месте.
Рибоксин (ФС 42-0275-07)
9-(-D-Рибофуранозил)-1H-пурин-6(9H)-он
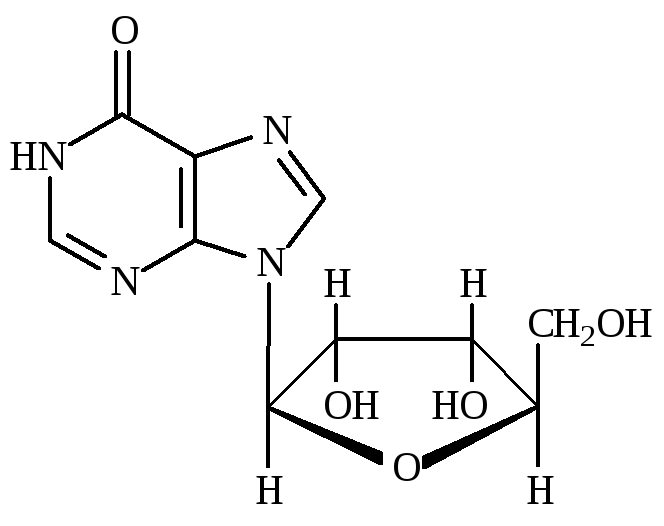
|
C10H12N4O5 |
М.м. 268,22 |
Cодержит не менее 96,0 % и не более 102,0 % C10H12N4O5 в пересчете на сухое вещество.
Описание. Белый или почти белый кристаллический порошок.
Растворимость. Умеренно (медленно) растворим в воде, очень мало растворим в спирте 96 %, практически нерастворим в хлороформе.
Подлинность. Инфракрасный спектр субстанции, снятый в диске с калия бромидом, в области от 4000 до 400 см-1 по положению полос поглощения должен соответствовать спектру ГСО рибоксина.
Время удерживания основного пика на хроматограмме испытуемого раствора (раздел «Количественное определение») должно соответствовать времени удерживания основного пика на хроматограмме стандартного раствора.
0,1 г субстанции растворяют в 20 мл воды. К 2 мл полученного раствора прибавляют 5 мл 0,1 % раствора железа(III) хлорида в хлористоводородной кислоте концентрированной и 5 мл 10 % раствора орцина в спирте 96 %. Смесь выдерживают в течение 20 мин в кипящей водяной бане; появляется зеленое окрашивание.
Прозрачность раствора. Раствор 0,1 г субстанции в 10 мл воды должен быть прозрачным или выдерживать сравнение с эталоном I.
Цветность раствора. Раствор, полученный в испытании на Прозрачность раствора, должен быть бесцветным или выдерживать сравнение с эталоном B9.
Удельное вращение. От –47 до –54 º в пересчете на сухое вещество (1 % раствор субстанции).
рН. От 4,8до 5,8 (1 % раствор).
Посторонние примеси. Определение проводят методом ВЭЖХ в условиях, описанных в разделе «Количественное определение».
Испытуемый раствор. 0,05 г субстанции растворяют в 50 мл ПФ.
Раствор сравнения. 1 мл испытуемого раствора помещают в мерную колбу вместимостью 100 мл, доводят объем раствора ПФ до метки и перемешивают.
Хроматографируют раствор сравнения и испытуемый раствор. Время регистрации хроматограммы испытуемого раствора должно не менее чем в 2 раза превышать время удерживания основного пика. Примеси гуанозина и гипоксантина на хроматограмме испытуемого раствора идентифицируют по хроматограмме раствора для проверки пригодности системы.
Сумма площадей пиков гуанозина и гипоксантина на хроматограмме испытуемого раствора не должна более чем в 2,5 раза превышать площадь пика на хроматограмме раствора сравнения (не более 2,5 %), сумма площадей пиков неидентифицированных примесей должна быть не более половины площади пика на хроматограмме раствора сравнения (не более 0,5 %).
Потеря в массе при высушивании. Около 1 г (точная навеска) субстанции сушат при температуре от 100 до 105 ºС до постоянной массы. Потеря в массе не должна превышать 1,0 %.
Сульфатная зола и тяжелые металлы. Сульфатная зола из 1 г (точная навеска) субстанции не должна превышать 0,1 % и должна выдерживать испытание на тяжелые металлы (не более 0,001 % в субстанции).
Железо. Сульфатная зола из 2 г субстанции должна выдерживать испытание на железо (не более 0,0015 % в субстанции).
Медь. 1,5 г субстанции прокаливают в фарфоровом тигле, остаток растворяют в 5 мл азотной кислоты, разбавляют водой до 15 мл и фильтруют. К 5 мл фильтрата прибавляют 5 мл 10 % раствора аммиака и фильтруют; фильтрат не должен окрашиваться в голубой цвет.
Остаточные органические растворители. В соответствии с требованиями ОФС «Остаточные органические растворители».
Бактериальные эндотоксины. Не более 0,29 ЕЭ на 1 мг субстанции.
Для проведения испытания готовят исходный раствор субстанции (концентрация 20 мг/мл), а затем разводят его не менее чем в 60 раз.
