
6 курс / Эндокринология / Эндокринология_и_метаболизм_Фелиг_Ф_,_Бакстер_Дж_Д_,_Бродус_А_Е
.pdfопределяющие такую трехфазную реакцию, не изучены. Однако принято считать, что они отражают последовательные изменения реакции нейрогипофиза на повреждение. Вначале развивается дефицит вазопрессина вследствие транзиторного паралича нейросекреторной функции. Затем по мере дегенерации клеток в кровь попадают большие количества гормона из депо. Наконец, возникающая в результате утрата жизнеспособных нейросекреторных клеток обусловливает состояние перманентной недостаточности вазопрессина. У многих больных конечная фаза постоянной полиурии не возникает, вероятно, потому, что число необратимо поврежденных клеток оказывается меньшим, чем требуется для клинически явной недостаточности антидиуретической функции. У других больных постоянная полиурия развивается сразу без промежуточной фазы олигурии. В некоторых случаях такое течение заболевания можно объяснить хирургическим удалением нейрогипофиза, но в других удовлетворительное объяснение выпадения фазы высвобождения вазопрессина из депо отсутствует.
Несахарный диабет следует дифференцировать от полиурии и полидипсии, вызываемых другими причинами (см. табл. 9—2 и табл. 9—4). Спутать его с сахарным диабетом невозможно, поскольку обычный анализ мочи наверняка обнаружит глюкозурию, определяющую диурез растворенных веществ. Отличить гипофизарный несахарный диабет от первичной полидипсии [50] и нефрогенного несахарного диабета [51] также относительно просто, если все три заболевания протекают в классической форме. При нефрогенном несахарном диабете полиурия обусловливается резистентностью почек к антидиуретическим эффектам нормальных количеств вазопрессина. Это заболевание сопровождается дегидратацией с легкой гипертоничностью и не поддается лечению ограничением жидкости (см. рис. 9—11). Однако в отличие от нейрогенного несахарного диабета оно не поддается коррекции и с помощью экзогенного вазопрессина. Полиурия при первичной полидипсии является следствием угнетения секреции вазопрессина чрезмерно большим потреблением воды. Она сопровождается сдвигом базальной осмоляльности плазмы и концентрации натрия к нижней границе нормы и поддается лечению с помощью ограничения жидкости (см. рис. 9—11). При введении экзогенного вазопрессина также исчезает полиурия, но поскольку он не влияет на основной стимул к потреблению воды, то в результате его применения может возникнуть тяжелая водная интоксикация. Дифференциальной диагностике этих трех состояний могут помочь также указания на их связь с определенным заболеванием, хирургическим вмешательством или семейным анамнезом (см. табл. 9—2).
Таблица 9—4. Дифференциальная диагностика несахарного диабета
1. Определение осмоляльности плазмы и/или концентрации натрия в условиях неограниченного потребления жидкости. Если эти показатели превышают соответственно 295 мосмоль/кг и 143 мэкв/л, диагноз первичной полидипсии исключается и дальнейшее обследование следует начинать с пункта 5 и/или 6 для разграничения нейрогенного и нефрогенного несахарного диабета. Или 2. Проведение пробы с дегидратацией. Если концентрированность мочи не увеличивается, пока осмоляльность плазмы и/или содержание натрия не достигнут соответственно 295 мосмоль/кг и 143 мэкв/л, диагноз первичной полидипсии исключается и следует переходить к пункту 5 и/или 6. Или 3. Определение отношения осмоляльности мочи и плазмы в конце пробы с дегидратацией. Если оно меньше 1,5, диагноз первичной полидипсии исключается и следует переходить к пункту 5 и/или 6. Или 4. Инфузия гипертонического солевого раствора с определением уровня вазопрессина в плазме и ее осмоляльности в различные сроки проведения пробы. Если отношение между этими двумя переменными ниже нормы, устанавливается диагноз несахарного диабета. Или 5. Проведение пробы с инфузией вазопрессина. Если осмоляльность мочи более чем на 150 мосмоль/кг превышает таковую в конце пробы с дегидратацией, диагноз нефрогенного несахарного диабета исключается. Или 6. Определение осмоляльности мочи и уровня вазопрессина в плазме в конце пробы с дегидратацией. Если отношение этих показателей не отклоняется от нормы, диагноз нефрогенного несахарного диабета исключается.
Однако на практике точная диагностика полиурического состояния не всегда столь проста и ясна. Главная трудность заключается в применении пробы с ограничением жидкости для дифференциации идиопатического несахарного диабета и первичной полидипсии. Поскольку у многих больных идиопатическим несахарным диабетом сохраняется некоторая остаточная способность повышать секрецию вазопрессина в ответ на гипертоническую дегидратацию, а при первичной полидипсии концентрационный градиент в мозговом слое почек снижен, что препятствует проявлению антидиуретической реакции на нормальное повышение уровня вазопрессина [50], постольку степень осмоляльности мочи, достигаемая в конце пробы, при обоих заболеваниях может быть сходной (см. рис.9—11).
Для преодоления этой диагностической трудности предложен ряд вспомогательных методов. Один из них заключается в определении отношения осмоляльностей мочи и плазмы в конце кратковременного периода ограничения приема жидкости [52]. В силу того что у большинства больных _несахарным диабетом концентрирование мочи возможно лишь при чрезмерной дегидратации, это отношение обычно выше у больных с первичной полидипсией. Однако у значительного числа больных оно находится в пре-
делах 1,8—2,2, т. е. в пограничной зоне, что не позволяет проводить надежного различия. Другой диагностический подход представляет собой модификацию оригинального метода, впервые предложенного Barlow и DeWardener [50] и заключающегося в сравнении максимальных значений осмоляльности мочи после ограничения приема жидкости и введения вазопрессина [53]. Значительно большее значение этого показателя после введения гормона указывает на недостаточность секреции вазопрессина. Хотя этот тест иногда и оказывается полезным, его проведение требует много времени и сил. Больше того, он также может давать нечеткие или даже ошибочные результаты в основном потому, что осмоляльность мочи иногда не достигает необходимой стабильности или равномерности к концу пробы с дегидратацией.
Более простой и надежный способ заключается в определении уровня вазопрессина в плазме или моче после соответствующего воздействия, например ограничения приема жидкости. По этим уровням обычно легче разграничить два состояния, чем по величинам осмоляльности мочи (см. рис. 9—11), поскольку последние показатели, как правило, перекрываются в силу характерных различий в чувствительности почек к гормону (см. рис. 9—и). Четкость разграничения можно еще более повысить, если уровни вазопрессина выражать в виде функции осмоляльности плазмы (см. рис. 9—3). Учитывая, что несахарный диабет обусловливается относительной, а не абсолютной недостаточностью вазопрессина, следует применять именно этот способ, поскольку с его помощью удается обычно выявить нарушение секреции гормона даже у больных со значительным сохранением функции нейрогипофиза. Диагностическая эффективность этого метода обеспечивается и тем фактом, что хроническая стимуляция или угнетение осморегуляторной системы, по-видимому, не меняют в значительной степени ее функциональных свойств. Следовательно, зависимость уровня вазопрессина в плазме от ее осмоляльности сохраняется в пределах нормы как при первичной полидипсии,. так и при нейрогенном несахарном диабете. Эти два состояния в большинстве случаев можно легко разграничить путем определения осмоляльности мочи в конце пробы с дегидратацией и сопоставления полученных данных с концентрацией вазопрессина в плазме в это время (см. рис. 9—8).
Иногда определение вазопрессина в условиях ограничения приема жидкости не дает возможности четко разграничить несахарный диабет и первичную полидипсию. Это характерно для больных, у которых в результате чрезмерной жажды и/или эффективной антидиуретической реакции осмоляльность плазмы не достигает 295 мосмоль/кг, т. е. того наименьшего уровня, при котором наверняка можно разграничить показатели секреции вазопрессина. В такой ситуации может потребоваться кратковременная внутривенная инфузия солевого гипертонического раствора с дополнительным одноили многократным определением уровня вазопрессина в плазме. У больных несахарным диабетом этот уровень может продолжать увеличиваться, но это увеличение всегда отчетливо ниже нормы по отношению к приросту осмоляльности плазмы. В отличие от этого у больных с первичной полидипсией наклон кривой, отражающей соответствующую реакцию, остается в пределах нормы. Поскольку инфузия гипертонического раствора часто сопровождается диурезом растворенных веществ, осмоляльность мочи и/или экскреция вазопрессина являются ненадежными показателями изменения секреции гормона [16] и практически не имеют диагностического значения при проведении этой пробы.
Как и следовало ожидать, у большинства больных несахарным диабетом секреция вазопрессина увеличивается в меньшей (по сравнению с нормой) степени и при действии гемодинамических, рвотных и глюкопенических стимулов. Однако в диагностическом отношении пробы с этими «неосмотическими» воздействиями, по-видимому, не обладают каким-либо преимуществом перед пробой с дегидратацией и/или инфузией гипертонического раствора. Отчасти это связано с тем, что ортостатические, рвотные и глюкопенические стимулы трудно контролировать и/или оценивать количественно, и они даже в норме вызывают весьма непостоянную реакцию вазопрессина. Проба с гипотензией, вызываемой фармакологическими средствами, позволяет точнее определить зависимость между стимулом и реакцией (см. рис. 9—4), но она громоздка и чревата потенциальной опасностью для больного. Более фундаментальной отрицательной стороной проб со всеми «неосмотическими» стимулами является реальная возможность получения как ложноположительных, так и ложноотрицательных результатов. В некоторых случаях практически не было повышения уровня вазопрессина в ответ на гипотензию или рвоту, но в то же время у обследуемых не отмечалась полиурия, а реакция на осмотические стимулы оставалась в пределах нормы. И наоборот, у некоторых больных с полиурией, не реагирующих повышением уровня вазопрессина в плазме на инфузию гипертонического солевого раствора, отмечалась от-
носительно нормальная реакция на гипотензивные, рвотные и глюкопенические стимулы. Последние наблюдения свидетельствуют о том, что в редких случаях несахарный диабет может обусловливаться избирательным или по крайней мере преимущественным поражением осморецептора, контролирующего секрецию вазопрессина.
ЛЕЧЕНИЕ
ВАЗОПРЕССИН И ЕГО АНАЛОГИ
Для лечения несахарного диабета уже давно применяют питрессина таннат в масле, который представляет собой частично очищенный экстракт гипофизов животных. Внутримышечные инъекции 5—10 ЕД каждые 2—3 дня у большинства больных достаточно эффективно снижают полиурию и полидипсию. Резистентность к препарату вследствие образования антител к нему наблюдается относительно редко. Ослабленная или извращенная антидиуретическая реакция обычно является следствием недостаточного эмульгирования смеси при ручном встряхивании или нагревании ампулы непосредственно перед использованием. Побочные эффекты препарата отмечаются редко и обычно выражаются аллергической реакцией. Основными недостатками лечения питрессином являются необходимость пожизненных инъекций и иногда приступы спазмов в животе, рвота, острые позывы на низ, повышение артериального давления и/или обесцвечивание кожи из-за случайной передозировки препарата. Водный раствор питрессина из-за кратковременности своего действия (всего лишь несколько часов) не подходит для длительного лечения несахарного диабета, но находит применение при проведении некоторых диагностических проб.
Имеется синтетический препарат лизин-вазопрессина (диапид), который можно вводить путем распыления в нос. Он обычно применяется , лишь как дополнительное средство к другим формам лечения, так как антидиуретический эффект при каждом распылении продолжается не более 4—6 ч.
В США недавно начали применять синтетический аналог вазопрессина — ДДАВП (десмопрессин) (см. рис. 9—2). Большой опыт его применения в Европе свидетельствует о многих преимуществах использования его в лечении несахарного диабета. Модификация молекулы в 1-м и 8-м положении удваивает ее антидиуретическую активность, снимает прессорное действие и значительно повышает ее устойчивость к метаболической деградации. При парентеральном введении или вдувании в нос этот препарат оказывает гораздо более длительное антидиуретическое действие чем нативный гормон [8]. У большинства больных введение его в количестве 10—25 мкг путем вдувания в нос дважды в сутки обеспечивает полную ликвидацию симптомов заболевания. Резистентность вследствие образования антител не описана, но всасыванию препарата может препятствовать ринит и/или синусит. Основным недостатком в настоящее время является его высокая стоимость. Иногда, например при беременности, когда окситоци-новое действие питрессина и возможное тератогенное действие пероральных препаратов служат противопоказанием к их применению, ДДАВП является, вероятно, наиболее предпочтительным средством.
ПЕРОРАЛЬНЫЕ ПРЕПАРАТЫ
Эффективность некоторых пероральных препаратов в лечении не-сахарного диабета [32] была обнаружена случайно. Хлорпропамид (диабинез), который чаще применяется для лечения гипергликемии, у больных с нейрогенным несахарным диабетом уменьшает выделение мочи на 30—70%. Этот эффект сопровождается пропорциональным увеличением осмоляльности мочи, коррекцией дегидратации и снижением потребления жидкости подобно тому, что происходит под действием малых доз вазопрессина. Хлорпропамид может вызывать антидиурез и у здоровых лиц или больных с первичной полидипсией, но по непонятным причинам этот эффект выражен гораздо слабее, чем у больных несахарным диабетом. Подобно вазопрессину он совершенно не эффективен при лечении больных нефрогенным несахарным диабетом, что указывает на сходство механизмов действия хлорпропамида и гормона. Основным механизмом действия хлорпропамида является, вероятно, потенцирование влияний небольших подпороговых количеств вазопрессина на почечные канальцы, однако все еще не опровергнута и воз-
можность стимуляции секреции гормона [54]. Другие вещества класса сульфонилмочевины не обладают значительным антидиуретическим действием при несахарном диабете, а в некоторых случаях могут даже несколько повышать диурез [32].
Клофибрейт (атромид-S), который чаще применяется для лечения гиперлипидемии, также снижает полиурию и полидипсию у больных несахарным диабетом. Антидиуретический эффект его максимальных доз обычно слабее, чем эффект хлорпропамида, хотя у некоторых больных он оказывается более эффективным. Механизм его действия также неясен. Подобно хлорпропамиду он неэффективен при нефрогенном несахарном диабете и оказывает лишь минимальное антидиуретическое действие у здоровых и больных с первичной полидипсией. Однако не удается показать, что клофибрейт потенцирует почечные эффекты вазопрессина, а в отношении его влияния на секрецию гормона данные противоречивы [32, 54].
Для уменьшения полиурии у больных несахарным диабетом можно применять и тиазидовые диуретики [55]. Этот внешне парадоксальный эффект наблюдается также при нефрогенном несахарном диабете, что свидетельствует об отличии механизма действия тиазидов от такового хлорпропамида и клофибрейта. Угнетая реабсорбцию натрия в восходящем колене петли Генле, тиазиды препятствуют максимальному разведению мочи. Кроме того, несколько уменьшая содержание натрия в организме, они снижают внеклеточный объем жидкости и увеличивают реабсорбцию соли и воды в проксимальных канальцах. В результате у больных несахарным диабетом несколько повышается осмоляльность мочи и пропорционально снижается ее объем. В зависимости от потребления натрия полиурия уменьшается обычно на 30—50% как при нефрогенном, так и при нейрогенном несахарном диабете. За исключением иногда развивающейся гипогликемии, тиазиды редко вызывают существенные побочные эффекты. Однако они уменьшают способность экскретировать избыточную воду и при введении больному с первичной полидипсией должны усугублять водную интоксикацию.
Точное значение пероральных препаратов в лечении несахарного диабета в настоящее время неизвестно. Порознь или в сочетании с тиазидовыми диуретиками они могут уменьшать полиурию до уровня, при котором отсутствуют жалобы практически у всех больных. Такое лечение имеет предсказуемые результаты, удобно и дешево. Однако этим преимуществам противостоит высокая частота нежелательных побочных эффектов, таких, как гипогликемия или боли в мышцах, а также нерешенность вопроса об их безопасности при длительном применении, особенно в отношении поражения коронарных сосудов и желчного пузыря. Кроме того, их, вероятно, не следует применять при беременности в силу возможного тератогенного эффекта, а также трудно и потенциально небезопасно назначать маленьким детям. В последних двух случаях наиболее безопасным и эффективным средством является, по-видимому, ДДАВП. Однако в других ситуациях большинство больных предпочитает лечение пероральными средствами, поскольку они создают наилучшее сочетание экономичности с удобством и возможностью четкой дозировки.
ВСПОМОГАТЕЛЬНЫЕ МЕРОПРИЯТИЯ
Существуют и другие методы, которые могут способствовать уменьшению полиурии как при нефрогенном, так и при нейрогенном несахарном диабете. Ограничение потребления соли снижает выделение мочи, увеличивая объем фильтрата, изоосмотически реабсорбирующегося в проксимальных отделах нефрона.
Лечение больных несахарным диабетом требует также тщательного выяснения этиологии заболевания, которое должно включать рентгенографию грудной клетки и черепа. Если при всех прочих исследованиях не обнаружена причина заболевания, то следует провести компьютерную томографию гипофизарном гипоталамической области в поисках кист или опухолей. Поскольку возможно одновременное вовлечение в патологический процесс областей, секретирующих гипоталамические рилизинг-факторы, следует также оценивать функцию передней доли гипофиза даже при отсутствии других признаков патологии турецкого седла.
ЖАЖДА
Нарушение механизма развития жажды приводит к адипсии и хронической или рецидивирующей гипернатриемии [56, 57]. Если дегидратация достигает значительной степени, у больных может снизиться интеллект, развиться хорея, азотемия, гипокалие-
мия и мышечная слабость с сопутствующим рабдомиолизом или без него. Такие приступы могут появляться в любое время, но часто провоцируются факторами окружающей среды, предрасполагающими к повышению скорости неощутимых потерь жидкости. Отсутствие восполнения этих потерь из-за повреждения осморецептора, опосредующего ощущение жажды, служит общим патогенетическим механизмом всех форм такого заболевания.
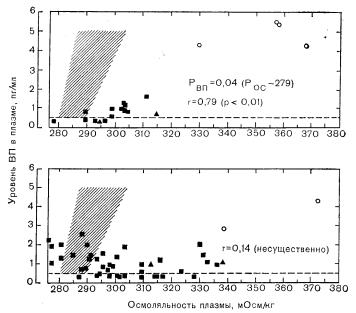
Убольшинства больных полиурии принадлежит очень незначительная роль в развитии дегидратации. Однако, вероятно, из-за близости осморецепторов, опосредующих чувство жажды и секрецию вазопрессина, часто, если не всегда, наблюдается и нарушение антидиуретической функции. Это нарушение остается обычно нераспознанным, пока не будут сделаны попытки ликвидировать гипернатриемию водной нагрузкой. При этом у больных могут отмечаться симптомы одного из двух типов. Чаще всего еще до того, как регидратация нормализует осмоляльность плазмы, происходит разведение мочи и развивается явная полиурия. Вначале предполагалось, что это нарушение является следствием чрезмерного повышения порога или сдвига «настройки» системы осморегуляции, что обычно называют эссенциальной гипернатриемией. Однако регрессионный анализ зависимости между осмоляльностью мочи или уровнем вазопрессина в плазме и осмоляльностью плазмы показал, что нарушение антидиуретической функции может обусловливаться заметным снижением наклона соответствующих кривых или чувствительности системы (рис. 9—12). Поскольку ни один из ранее описанных больных с эссенциальной гипернатриемией не был обследован с применением методов регрессионного анализа, необходимых для разграничения истинной и кажущейся «перенастройки» осмостата, постольку все еще не ясно, действительно ли у человека может существовать такая патология.
Унекоторых больных с адипсической гипернатриемией усиленная гидратация приводит к гипотоничности с потерей способности к максимальному разведению мочи. Этот парадоксальный дефект напоминает то, что наблюдается при синдроме неадекват-
Рис. 9—12. Уровень вазопрессина (ВП) в плазме как функция ее осмоляльности у двух больных с адипсической гипернатриемией.
Кружками помечены значения, полученные в условиях гипотензии [воспроизведено с разрешения из публикации Bobertson G. L. — In: Tolls G. и соавт, (eds.) Clinical Neuroendocrinology: A pathophysiological Approach. — New York, Raven Press, 1979].
ного антидиуреза и проявляется, по-видимому, двумя разными формами. При одной из них происходит длительная или постоянная секреция вазопрессина вследствие полной утраты осморегуляторной функции (рис. 9—12). У таких больных небольшие, но биологически эффективные количества вазопрессина продолжают циркулировать в крови независимо от увеличения или уменьшения степени гидратации. При втором типе дефекта разведения осмоляльность мочи остается высокой даже тогда, когда со-
держание вазопрессина в плазме уменьшается до .неопределимого уровня [57]. Причина этого нарушения неизвестна, но может заключаться в чрезмерной чувствительности почек к очень низким концентрациям вазопрессина.
У многих, если не у большинства, больных с адипсической гипернатриемией недостаточная реакция вазопрессина на изменения гидратации является следствием избирательного нарушения функции осморецептора. Нейрогипофиз и его регуляторные афференты сохраняются, по-видимому, совершенно интактными, так как реакции вазопрессина на гемодинамические, рвотные и глюкопенические стимулы обычно остаются в пределах нормы или даже превышают ее.
Отдифференцировать адипсическую гипернатриемию от других причин нарушения водносолевого равновесия обычно нетрудно (см. табл. 9—3). Этот диагноз можно поставить почти наверняка в том случае, если у находящегося в сознании взрослого человека отсутствует жажда в условиях, когда осмоляльность плазмы и концентрация натрия превышают соответственно 310 мосмоль/кг и 150 мэкв/л. В сомнительных случаях можно наблюдать за появлением жажды при стандартной инфузии гипертонического солевого раствора. Осмотический порог чувства жажды может быть слегка повышен и при первичном альдостеронизме, но с увеличением гипертоничности плазмы интенсивность ощущения жажды у этих больных не снижается.
Лечение больных с адипсической гипернатриемией — в основном вопрос правильного режима. Постоянная схема потребления воды в сочетании с ежедневным взвешиванием для наблюдения за изменением гидратации обычно оказывается достаточной мерой для поддержания осмоляльности плазмы и концентрации натрия в ней в пределах 5% отклонения от нормы. Соблюдение такого режима особенно важно для больных с нарушенной способностью к разведению мочи, так как у них часто развивается как ги- пер-, так и гипогидратация. У больных, у которых развивающаяся полиурия препятствует достижению нормальной гидратации, часто оказывается полезным применение вазопрессина или одного из пероральных средств, способствующих антидиурезу. Пероральные препараты могут приводить также к некоторому повышению потребления жидкости, хотя этот эффект в лучшем случае невелик и не может заменить других способов поддержания водопотребления. Необходимо также тщательно выяснять причину адипсии с помощью методов, аналогичных тем, которые применяются для выяснения причин развития несахарного диабета.
ГИПЕРФУНКЦИЯ ЗАДНЕЙ ДОЛИ ГИПОФИЗА
Патогенез
Гиперсекрецию вазопрессина предпочтительнее определять как неполное подавление секреции гормона на фоне гипоосмоляльности жидких сред организма. Должна существовать и повышенная секреция его лишь в условиях неизмененной осмоляльности, но, согласно современным представлениям о действии вазопрессина, при этом не следует ожидать появления сколько-нибудь существенных нарушений солевого и водного баланса. Клинически выявляемую форму гиперсекреции этого гормона составляет лишь дефект в функции осмотического порога, т. е. способности снижать секрецию вазопрессина в достаточной для поддержания максимального диуреза степени.
Встречается два вида гиперсекреции вазопрессина: в ответ на известный неосмотический стимул, например гипотензию, или в результате какого-то более глубокого нарушения осмотической регуляции секреции гормона (табл. 9—5). Гиперсекрецию первого вида можно было бы назвать адекватной, поскольку она
Таблица 9—5. Причина гипотоничности жидких сред организма
I.Недостаточная экскреция свободной воды А. Дистальная
1.Гормональная (нарушенное разведение мочи) а. Адекватная (кровопотеря, прием диуретиков, почечная недостаточность, холера) б. Неадекватная (синдром неадекватной секреции АДП) (см. табл. 9—6)
2.Нефрогенная Б. Проксимальная (нарушение экскреции растворенных веществ)
1. Гемодинамическая а. Гиповолемия, гипотензия (например, снижение уровня натрия, кровопотеря) б. «Эффективная» гиповолемия (например, застойная сердечная недостаточность, цирроз печени) в. Прочие (печеночно-почечные)
2. Уменьшение массы почек а. Острый некроз канальцев б. Хронический нефрит II. Избыточное потребление воды
А. Тяжелая первичная полидипсия (в редких случаях более 20 л/сут).
появляется в ответ на физиологический стимул и по крайней мере в небольшой степени способствует поддержанию объема и/или давления крови. Второй вид можно было бы назвать неадекватной гиперсекрецией, так как она обусловливается неизвестной или явной патологической причиной и не выполняет сколько-нибудь отчетливой гомеостатической функции. Об этой разнице между адекватным и неадекватным видами гиперсекреции вазопрессина важно помнить, поскольку патофизиология и лечение каждой из них совершенно различны.
Синдром неадекватной секреции АДГ впервые был описан у двух больных с бронхогенным раком [58]. В дальнейшем его все чаще стали обнаруживать при разнообразных злокачественных и незлокачественных заболеваниях (табл. 9—6). За исключением больных с опухолями, у которых иногда встречается эктопическая продукция гормона, патогенез его гиперсекреции остается неизвестным. Определение уровня вазопрессина в плазме показывает, что у большинства больных секреция гормона неадекватно высока по отношению к гипоосмоляльности жидких сред организма (рис. 9— 13). Однако лишь в редких случаях содержание вазопрессина в плазме превышает его уровень у нормально гидратированных взрослых лиц, находящихся в положении лежа. Таким образом, о гиперсекреции можно говорить лишь по отношению к осмоляльности плазмы и/или концентрации натрия в ней, а выявить ее с определенностью удается путем определения уровня вазопрессина лишь в условиях гипергидратации.
Функциональные исследования секреции вазопрессина у больных с синдромом неадекватной секреции АДГ показали, что этот синдром представляет собой гетерогенное расстройство, объеди-
Таблица 9—6. Причины синдрома неадекватного антидиуреза (СНА)
I.Опухоли
А. Бронхогенный рак Б. Рак двенадцатиперстной кишки
В. Рак поджелудочной железы Г. Тимома Д. Рак мочеточника Е. Лимфома
Ж. Саркома Юинга 3. Рак предстательной железы
II. Неопухолевые заболевания А. Травма Б. Легочные заболевания
1.Пневмония
2.Образование полости (аспергиллез)
3.Туберкулез
4.Дыхание под положительным давлением В. Заболевания ЦНС
1.Менингит
2.Травмы головы
3.Абсцесс мозга
4.Энцефалит
5.Синдром Гийена — Барре
6.Субарахноидальное кровоизлияние
7.Острая перемежающаяся порфирия
8.Периферическая нейропатия
9.Психоз
10.Алкогольный делирий
11.Истечение СМЖ Г. СНА при эндокринных заболеваниях
1.Аддисонова болезнь
2.Микседема

3. Гипопитуитаризм Д. «Идиопатический» СНА III. Лекарственные вещества А. Вазопрессин Б. Окситоцин В. Винкристин Г. Хлорпропамид
Д. Хлортиазид, гидрохлортиазид, гидрофторметазид и циклотиазид Е. Атромид-S
Ж. Тегретол 3. Никотин И. Фенотиазины И. Циклофосфамид (циклофосфан)
няющее по меньшей мере четыре разных типа осморегуляторных нарушений [59] (рис. 9-14). Для каждого из них характерно своеобразное изменение секреции вазопрессина при водной на-грузке и/или инфузии гипертонического солевого раствора, что,-вероятно, отражает принципиальные различия патогенетических механизмов. Тип А характеризуется большими и беспорядочными колебаниями уровня вазопрессина в плазме вне всякой связи с изменениями осмоляльности плазмы. Это наблюдается примерно у 25% больных с синдромом неадекватной секреции АДГ и связано, повидимому, с полным прекращением регуляции осморе-
Рис. 9—13. Зависимость уровня вазопрессина (ВГТ) в плазме от ее осмоляльности при синдроме неадекватного антидиуреза.
Каждая точка — один больной (воспроизведено с разрешения из публикации Robertson [16]). цептора или его прерывистой стимуляцией какими-то невыясненными неосмотическими стимулами. Чаще всего встречается тип В, регистрируемый не менее чем у 35% всех больных. Он характеризуется быстрыми изменениями уровня вазопрессина в плазме, которые тесно коррелируют с изменениями ее осмоляльности. Регрессионный анализ связи между этими двумя переменными показывает, что точность и чувствительность реакции настолько же высоки, что и у здоровых взрослых лиц, но экстраполированное пороговое значение находится ниже нормы. У больных с нарушением этого типа, что отражает, по-видимому, «перенастройку» осмостата, клинические проявления несколько отличаются от таковых при других формах синдрома неадекватной секреции АДГ. При нарушении типа С содержание вазопрессина в плазме постоянно остается на неадекватно высоком уровне до тех пор, пока осмоляльность плазмы повышается до верхней границы нормы. С этого момента уровень вазопрессина в плазме начинает повышаться в тесном соответствии с дальнейшим увеличением ее осмоляльности. Нарушение этого типа также встречается примерно у 25% всех больных с этим синдромом. Оно могло бы, по-видимому, отражать постоянную неподавляемую «утечку» вазопрессина на фоне в остальном нормальной осморегуляторной функции.
Тип D встречается гораздо реже всех остальных и отражает, вероятно, существенно иной дефект антидиуретической функции. У этих редко встречающихся больных секреция вазопрессина нормально стимулируется и подавляется изменением осмоляльности, но моча постоянно остается концентрированной. Причина столь явного расхождения между уровнем вазопрессина в плазме и концентрированностью мочи пока не известна. Это могло бы быть результатом гиперсекреции какого-то другого антидиуретического вещества, например аргинин-вазотоцина. Альтернативным объяснением является чрезмерная чувствительность некоторых больных к антидиуретическому эффекту нормально низкого уровня вазопрессина. Последнее могло бы определяться повышением сродства рецепторов или отсутствием какого-то местного антагониста, на-

пример простагландина Е. Если это так, то можно было бы считать, что синдром неадекватной секреции АДГ типа D имеет нефрогенное происхождение в отличие от других, чаще встречающихся нейрогенных форм его.
Рис. 9—14. Зависимость уровня вазопрессина (ВП) в плазме от ее осмоляльности при инфузии гипертонического солевого раствора у 4 разных больных (1, 2, 3, 4) с клиникой синдрома неадекватного антидиуреза (воспроизведено с разрешения из публикации Bobertson и соавт. [59]).
Между типом осморегуляторного нарушения и лежащей в его основе клинической патологией не существует простой или явной зависимости. Такое отсутствие корреляции могло бы указывать на то, что одно заболевание, например пневмония, вызывает этот синдром любым из нескольких патогенетических механизмов или что осморегуляторное нарушение вызывается в действительности каким-то иным фактором, чем то заболевание, с которым это нарушение на первый взгляд связано. Наиболее важным фактом является то, что бронхогенный рак может служить внешней причиной осморегуляторного нарушения любого типа, в том числе типа В — «перенастройки» осмостата. Поскольку представляется невероятным, чтобы анапластические клетки могли одновременно приобретать в норме раздельные функции к осморегуляции и продукции вазопрессина, постольку многие из этих опухолей вызывают синдром неадекватной секреции АДГ, очевидно, каким-то иным механизмом, чем эктопическая продукция гормона.
Клинические последствия неадекватной секреции вазопрессина легче всего оценить, наблюдая эффекты введения экзогенного вазопрессина здоровым людям [60]. В условиях нормального общего потребления воды, т. е. 1—2 л/сут, воспроизведение постоянного антидиуреза практически не оказывает никакого влияния, поскольку сочетание неощутимых потерь жидкости и минимального выделения мочи обычно оказывается достаточным для поддержания водного баланса. Однако даже при незначительном увеличении потребления жидкости, соответствующего повышения еѐ выделения не происходит, так как уровень вазопрессина в плазме и концентрированность мочи не снижаются при уменьшении осмоляльности плазмы, что происходит в норме. В результате начинает накапливаться избыток ежедневно принимаемой воды, что вызывает прогрессирующее уменьшение концентрации растворенных веществ в организме. Когда увеличение объема воды в организме достигает примерно 10%, начинает увеличиваться экскреция натрия в результате как снижения реабсорбции в проксимальных канальцах, так и подавления ренин-ангиотензин-альдостероновой системы. Натрийурез оказывает положительное воздействие на гиперволемию и приводит к некоторому снижению концентрированности мочи и повышению ее выделения, но одновременно усиливает гипонатриемию и гипотоничность жидких сред организма. Повышение приема натрия не нормализует ситуацию, поскольку развивающаяся в результате гиперволемия «запускает» лишь еще одну натрийуретическую реакцию. В этот период может возникнуть новое равновесное состояние, если отсутствует изменение потребления жидко-
сти. Если же потребление жидкости вновь увеличивается, возникает повторный цикл задержки воды и натрийуреза, что приводит к дальнейшему снижению осмоляльности плазмы и концентрации натрия в ней. С другой стороны, если потребление воды сокращается, вся серия событий развивается в обратном направлении и осмоляльность плазмы и концентрация натрия у ней постепенно возвращаются к своим исходным уровням.
Следует отметить, что клинические проявления гиперсекреции вазопрессина зависят почти исключительно от величины потребления жидкости. Если оно находится в пределах нормы, то неадекватная секреция гормона не будет сопровождаться явной клинической симптоматикой, как бы ни повышался уровень вазопрессина в плазме. И в условиях высокого потребления воды усиление секреции гормона сверх того минимального уровня, который требуется для концентрирования мочи, не приводит к заметному прогрессированию нарушения солевого и водного равновесия. Это объясняется тем, что скорость выделения мочи по мере увеличения ее осмоляльности с 400 до 1200 мосммоль/кг снижается лишь незначительно (см. рис. 9—9). В связи с этим гиперсекреция вазопрессина реально играет лишь пермиссивную роль по отношению к последовательности событий, приводящих к гипонатриемии. Эта роль резко отличается от роли многих других гормонов, например инсулина или соматотропина, гиперсекреция которых сама по себе достаточна для развития клинической симптоматики.
Восновном те же клинические проявления наблюдаются при синдроме неадекватной секреции АДГ, когда вазопрессин продуцируется эндогенно. Единственное существенное различие касается больных с нарушением типа В, т. е. «перенастройкой» осмостата. Поскольку у этих больных пороговая функция сохраняется, увеличение потребления воды в конце концов приводит к максимальному разведению мочи, и поэтому скорость ее экскреции оказывается достаточной для ограничения дальнейшей гипергидратации [61, 62]. В результате осмоляльность плазмы остается более или менее стабильной, хотя и на гораздо меньшем, чем в норме, уровне. Этот вариант является важным исключением из правила, согласно которому у больных с синдромом неадекватной секреции АДГ теряется способность к экскреции максимально разведенной мочи. Большинство таких случаев остается, вероятно, клинически невыясненными, так как при обследовании и лечении больных с этим синдромом далеко не всегда производят водную нагрузку и/или определение уровня вазопрессина.
Вслучаях, когда гиперсекреция вазопрессина адекватна, т. е. появляется в ответ на гемодинамический стимул, патофизиология нарушений солевого и водного равновесия отличается в двух важных отношениях. Поскольку гипотензия и/или гиповолемия являются мощными стимулами задержки натрия, натрийурез не развивается, если отсутствует сопутствующий дефект в почках или гормональных системах, регулирующих равновесие натрия (например, болезнь Аддисона или сольтеряющая форма нефрита). Увеличение потребления натрия часто оказывает терапевтическое действие, так как не только компенсирует его возможный дефицит, но и, повышая объем или давление крови, может также снижать секрецию вазопрессина до уровня, обеспечивающего увеличение экскреции воды, лишенной растворенных веществ.
Признаки, симптомы, диагностика
У больных с синдромом неадекватной секреции АДГ клинические проявления его часто немногочисленны, за исключением гипотоничности жидких сред организма. Хотя общее содержание воды в организме и увеличивается, но такие клинические признаки гиперволемии, как гипертония или отеки, отсутствуют, если одновременно нет нарушений экскреции натрия. При уменьшении осмоляльности плазмы и концентрации натрия в ней соответственно ниже 250 мосмоль/кг и 120 мэкв/л могут развиваться симптомы, характерные для нарушения деятельности ЦНС. При уменьшении осмоляльности и концентрации натрия до 230 мосмоль/кг и 110 мэкв/л и ниже сонливость, спутанность сознания и головная боль могут переходить в гемипарез, кому и даже судороги. Эти осложнения являются, вероятно, следствием отека мозга, обусловленного перераспределением воды из внеклеточного пространства под действием осмотических сил. Тяжесть симптомов может отчасти зависеть от степени гипергидратации, поскольку имеются некоторые указания на способность головного мозга постепенно противодействовать этим изменениям объема путем инактивации растворенных внутри клеток веществ пли освобождения от них [63].
Диагностика синдрома предполагает необходимость дифференцирования его не только от случаев адекватного увеличения секреции вазопрессина, но и от случаев
