
- •4 Пространственная изомерия, конфигурация и конформация.
- •5. Ассимметрический атом углерода как центр хиральности. Стереоизомерия молекул с одним центром хиральности. Оптическая активность.
- •7. Электронное строение атома углерода. Типы гибридизаций атомных орбиталей.
- •8. Сопряженные системы с открытой и замкнутой цепью на примерах бутадиента 1,3 и бензола.
- •9. Ароматичность. Критерии ароматичности.
- •10. Электронные эффекты заместителей: индуктивный и мезомерный. Электродонорные и электроакцепторные заместители и их влияние на реакционную способность соединений.
- •11. Гомо/гетеролитические разрывы ковалентной связы в органических соединениях, образующиеся при этом частицы.
- •12. Радикальные, электрофильные, нуклеофильные реагенты, классификация хим реакций по типу реагента.
- •13. Классификация хим реакций по результату: замещенеие, присоединение, элиминирование, перегруппировка, овр
- •14. Кислоты и основания по бренстеду, их классификация.
- •15. Влияние различных факторов на кислотные и основные свойства веществ. Примеры.
- •16. Спирты и фенолы. Многоатомные спирты.
- •17. Химические свойства спиртов и фенолов.
- •19. Классификации карбоновых кислот по основности, насыщенности, наличию функциональной группы, числу атомов углерода в цепи.
- •20. Химические свойства карбоновых кислот с участием карбоксильной группы: декарбоксилирование, образование солей, амидов, ангидридов, галогенгидридов, сложных эфиров.
- •21. Высшие жирные карбоновые кислоты: классификация, номенклатура, структура, физические свойства.
- •22.Дикарбоновые кислоты: щавелевая, малоновая, янтарная, глутаровая, фумаровая. Их роль в организме. Соли щавелевой кислоты - оксалаты.
- •23. Оксо- гидроксикарбоновые кислоты: пировиноградная и молочная, яблочная и щавелевая, лимонная, ацетоуксусная и β-гидроксимасляная, α-кетоглутаровая, функции в организме.
- •24. Общее представление о липидах, классификация липидов.
- •25. Простые липиды: таг, состав, номенклатура, свойства, гидролиз таг, биологическая роль.
- •27. Соединения стеройдной группы: холестерин, желчные кислоты, представление о химическом строении и биологической роли.
- •28. Углеводы, классификация углеводов, функции углеводов в организме.
- •29. Классификация и химические свойства моносахаридов, (см выше) овр моносахаридов.
- •30. Стереоизомерия моносахаридов d- и l- ряды, открытые и циклические формулы (фишера, колли-толленса, хеуорса), пиранозы и фуранозы, α и β аномеры, циклоцепная таутомерия, явление мутаротации.
- •33. Классификация полисахаридов, функции в организме.
- •34. Дисахариды, структура и свойства основных биологически важных дисахаридов: мальтозы, лактозы, сахарозы, целлобиозы.
- •35. Гомополисахариды: крахмал (амилоза и амилопектин), гликоген, целлюлоза, строение, свойства, биологическая роль.
- •36. Гетерополисахариды, гиалуроновая кислота, хондроитинсульфаты, строение, биологическая роль.
- •37. Азотистые основания пиримидиновые (тимин, урацил, цитозин) и пуриновые (аденин, гуанин), строение, лактим-лактамная таутомерия.
- •38. Нуклеозиды, строение, номенклатура, гидролиз, характер связи нуклеинового основания с углеводным остатком.
- •39. Нуклеотиды, строение, номенклатура, гидролиз, характер связей между компонентами нуклеотида.
- •40. Свободные нуклеотиды: цамф и цгмф, атф, адф, фад, над, строение, функции в организме.
- •41. Первичная структура нуклеиновых кислот, нуклеотидный состав днк/рнк.
- •42. Понятие о вторичной структуре днк. Комплементарность азотистых оснований, водородные связи в комплементарных парах.
- •43. Аминокислоты, номенклатура, классификация по полярности радикала и пищевой ценности, примеры.
- •44. Стереоизомерия аминокислот.
- •45. Кислотно-основные свойства аминокислот. Биполярные ионы, изоэлектрическая точка.
- •46. Химические свойства аминокислот, биологически важные свойства аминокислот.
- •47. Физиологически активные пептиды, примеры.
- •48. Уровни организации белковой молекулы: первичная структура белка, электронное строение пептидной связи и ее характеристика, зависимость свойств белка от первичной структуры.
- •49. Вторичная структура белков, α-спираль, β-складчатый слой, беспорядочный клубок, связи, стабилизирующие вторичную структуру белка.
- •50. Третичная и четвертичная структуры белков, связи, их стабилизирующие, особенности строения и функционирования олигомерных белков на примере гемоглобина.
- •51. Классификации белков.
- •52. Физико-химические свойства белков, растворимость, ионизация, гидратация, денатурация, ренатурация.
- •56. Классификация сложных белков.
- •57. Гемопротеины, сравнительная характеристика структур и функций миоглобина и гемоглобина.
- •53. Кооперативное связывание кислорода гемоглобином, эффект бора, влияние 2,3-бфг на сродство гемоглобина к кислороду. Эффективность транспорта кислорода регулируется Изменение рН среды
- •Механизм эффекта Бора Кооперативное взаимодействие
53. Кооперативное связывание кислорода гемоглобином, эффект бора, влияние 2,3-бфг на сродство гемоглобина к кислороду. Эффективность транспорта кислорода регулируется Изменение рН среды
Влияние рН на сродство гемоглобина к кислороду носит название эффекта Бора. При закислении среды сродство снижается, при защелачивании – повышается.
При повышении концентрации протонов (закисление среды) в тканях возрастает освобождение кислорода из оксигемоглобина. В легких после удаления угольной кислоты (в виде СО2) из крови и одновременном увеличении концентрации кислорода высвобождаются ионы Н+ из гемоглобина.
Реакция взаимодействия кислорода с гемоглобином упрощенно имеет вид:
![]()
Изменение сродства гемоглобина к кислороду в тканях и в легких при изменении концентрации ионов H+ и О2 обусловлено конформационными перестройками глобиновой части молекулы. В тканях ионы водорода присоединяются к остаткам гистидина, образуя восстановленный гемоглобин (H-Hb) с низким сродством к кислороду. В легких поступающий кислород "вытесняет" ион водорода из связи с остатком гистидина гемоглобиновой молекулы.
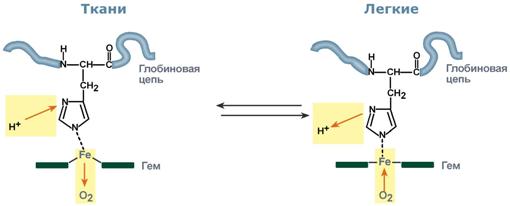
Механизм эффекта Бора Кооперативное взаимодействие
Взаимовлияние протомеров олигомерного белка друг на друга называется кооперативное взаимодействие.
В легких такое взаимодействие субъединиц гемоглобина повышает его сродство к кислороду и ускоряет присоединение кислорода в 300 раз. В тканях идет обратный процесс, сродство снижается и ускорение отдачи кислорода также 300-кратное.

Схема кооперативного взаимодействия субъединиц гемоглобина
Объясняется такой феномен тем, что в легких при присоединении первой молекулы кислорода к железу (за счет 6-й координационной связи) атом железа втягивается в плоскость гема, кислород остается вне плоскости. Это вызывает перемещение участка белковой цепи и изменение конформации первого протомера. Такой измененный протомер влияет на другие субъединицы и облегчает связывание кислорода со второй субъединицей. Это меняет конформацию второй субъединицы, облегчая присоединение последующих молекул кислорода и изменение других протомеров.
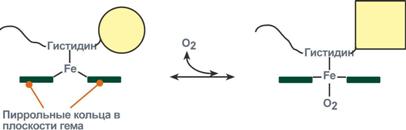
Изменение формы субъединиц гемоглобина при присоединении кислорода
Роль 2,3-дифосфоглицерата
2,3-Дифосфоглицерат образуется в эритроцитах из 1,3-дифосфоглицерата, промежуточного метаболита гликолиза, в реакциях, получивших название шунт Раппопорта.

Реакции шунта Раппопорта
2,3-Дифосфоглицерат располагается в центральной полости тетрамера дезоксигемоглобина и связывается с β-цепями, образуя поперечный солевой мостик между атомами кислорода 2,3-дифосфоглицерата и аминогруппами концевого валина обеих β-цепей, также аминогруппами радикалов лизина и гистидина.

Расположение 2,3-дифосфоглицерата в гемоглобине
Функция 2,3-дифосфоглицерата заключается в снижении сродства гемоглобина к кислороду. Это имеет особенное значение при подъеме на высоту, при нехватке кислорода во вдыхаемом воздухе. В этих условиях связывание кислорода с гемоглобином в легких не нарушается, так как концентрация его относительно высока. Однако в тканях за счет 2,3-дифосфоглицерата отдача кислорода возрастает в 2 раза.
