
- •Классификация аминокислот.
- •Окисление жирных кислот с четным числом углеродных атомов
- •Физико-химические свойства аминокислот.
- •Пути превращения углеводов. Реакции гликолиза.
- •Первичная структура белка. Характеристика пептидной связи.
- •Пентозофосфатный путь и его значение.
- •Вторичная структура белка. Альфа- спираль и бета – складчатый слой.
- •Мобилизация гликогена при мышечной работе.
- •Третичная структура белка и силы ее стабилизирующие.
- •Работа пируватдегидрогеназного комплекса.
- •Четвертичная структура белка. Понятия о денатурации и деструкции.
- •Работа цикла трикарбоновых кислот.
- •Моносахариды. Структура и функция.
- •Синтазная система синтеза жирных кислот.
- •Кооперативный эффект связывания кислорода гемоглобином.
- •Окисление жирных кислот с нечетным числом углеродных атомов.
- •Реакции глюконеогенеза.
- •Отличия ферментов от неорганических катализаторов.
- •Классификация ферментов с примерами реакций на каждый класс.
- •Биохимия мышечного сокращения. Характеристика белков мышц.
- •Влияние температуры, pH и концентрации фермента на скорость ферментативной реакции.
- •Реакции трансаминирования, их биологическая роль.
- •Пути превращения аминокислот в организме человека. Глюкогенные и кетогенные аминокислоты.
- •Влияние концентрации субстрата на скорость ферментативной реакции. Уравнение Михаэлиса-Ментен.
- •Ингибирование ферментов. Конкурентное ингибирование. Использование конкурентного ингибирования для лечения заболеваний.
- •Синтез кетоновых тел, их роль для организма человека.
- •Ингибирование ферментов. Неконкурентное ингибирование.
- •Цикл мочевины.
- •Аллостерические ферменты.
- •Глюкозо-аланиновый путь, его важность для спортсмена.
- •Активный центр фермента и его свойства.
- •Биохимия мышц. Источники энергии для мышечного сокращения.
- •1 Кофакторы и коферменты. Классификация.
- •Гормоны гипоталамуса и гипофиза.
- •Способы определения активности фермента. Единицы измерения. Понятие об удельной и молярной активности.
- •Гормоны надпочечников (коркового и мозгового слоя)
- •Изоферменты.
- •Биосинтез белка. Стадии активации и инициации.
Классификация ферментов с примерами реакций на каждый класс.
По
типу катализируемых реакций ферменты
подразделяются на 6 классов согласно
иерархической классификации ферментов.
Каждый класс содержит подклассы, так
что фермент описывается совокупностью
четырёх чисел, разделённых точками.
Например, пепсин имеет название ЕС
3.4.23.1. Первое число грубо описывает
механизм реакции, катализируемой
ферментом: КФ
1: Оксидоредуктазы,
катализирующие перенос электронов, то
есть окисление или восстановление.
Пример: каталаза, алкогольдегидрогеназа.
Реакции, катализируемые оксидоредуктазами,
в общем виде выглядят так: A− + B → A + B−.
Где A — восстановитель (донор электронов),
а B — окислитель (акцептор электронов)
В биохимических превращениях
окислительно-восстановительные реакции
иногда выглядят сложнее. 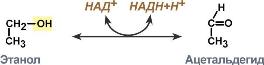 .
Здесь в качестве окислителя выступает
НАД+, а глицеральдегид-3-фосфат является
восстановителем. КФ
2: Трансферазы,
катализирующие перенос химических
групп с одной молекулы субстрата на
другую. Среди трансфераз особо выделяют
киназы, переносящие фосфатную группу,
как правило, с молекулы АТФ. Реакции,
катализируемые трансферазами, в общем
случае выглядят так: A—X + B ↔ A + B—X.
Молекула A здесь выступает в качестве
донора группы атомов (X), а молекула B
является акцептором группы. Часто в
качестве донора в подобных реакциях
переноса выступает один из коферментов.
Многие из катализируемых трансферазами
реакций являются обратимыми.
.
Здесь в качестве окислителя выступает
НАД+, а глицеральдегид-3-фосфат является
восстановителем. КФ
2: Трансферазы,
катализирующие перенос химических
групп с одной молекулы субстрата на
другую. Среди трансфераз особо выделяют
киназы, переносящие фосфатную группу,
как правило, с молекулы АТФ. Реакции,
катализируемые трансферазами, в общем
случае выглядят так: A—X + B ↔ A + B—X.
Молекула A здесь выступает в качестве
донора группы атомов (X), а молекула B
является акцептором группы. Часто в
качестве донора в подобных реакциях
переноса выступает один из коферментов.
Многие из катализируемых трансферазами
реакций являются обратимыми. 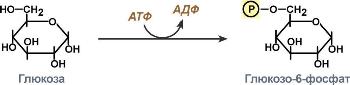 КФ
3: Гидролазы,
катализирующие гидролиз химических
связей. Пример: эстеразы, пепсин, трипсин,
амилаза, липопротеинлипаза. Общий вид
реакции, катализируемой гидролазой,
выглядит следующим образом: A-B + H2O →
A-OH + B-H. Проявляют активность при наличии
неизменённых сульфгидрильных SH— групп,
если таковые занимают определённое
положение в полипептидной цепи.
Каталитическое действие заключается
в соединении гидролаз с расщепляемым
веществом и последующим отщеплением
продуктов реакции с высвобождением
самих гидролаз. Механизм имеет много
общего с действием трансфераз. Гидролазы
переносят отщепляемые группы на воду,
но некоторые способны переносить их и
на другие молекулы. Часть гидролаз
выделена в кристаллической форме
(уреаза, пепсин, трипсин, химотрипсин и
др.).
КФ
3: Гидролазы,
катализирующие гидролиз химических
связей. Пример: эстеразы, пепсин, трипсин,
амилаза, липопротеинлипаза. Общий вид
реакции, катализируемой гидролазой,
выглядит следующим образом: A-B + H2O →
A-OH + B-H. Проявляют активность при наличии
неизменённых сульфгидрильных SH— групп,
если таковые занимают определённое
положение в полипептидной цепи.
Каталитическое действие заключается
в соединении гидролаз с расщепляемым
веществом и последующим отщеплением
продуктов реакции с высвобождением
самих гидролаз. Механизм имеет много
общего с действием трансфераз. Гидролазы
переносят отщепляемые группы на воду,
но некоторые способны переносить их и
на другие молекулы. Часть гидролаз
выделена в кристаллической форме
(уреаза, пепсин, трипсин, химотрипсин и
др.). 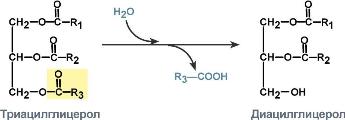 КФ
4: Лиазы,
катализирующих реакции негидролитического
и неокислительного разрыва различных
химических связей (C—C, C—O, C—N, C—S и
других) субстрата, обратимые реакции
образования и разрыва двойных связей,
сопровождающиеся отщеплением или
присоединением групп атомов по её месту,
а также образованием циклических
структур.
КФ
4: Лиазы,
катализирующих реакции негидролитического
и неокислительного разрыва различных
химических связей (C—C, C—O, C—N, C—S и
других) субстрата, обратимые реакции
образования и разрыва двойных связей,
сопровождающиеся отщеплением или
присоединением групп атомов по её месту,
а также образованием циклических
структур. 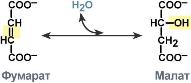 КФ
5: Изомеразы,
катализирующие структурные или
геометрические изменения в молекуле
субстрата с образованием изомерных
форм.
КФ
5: Изомеразы,
катализирующие структурные или
геометрические изменения в молекуле
субстрата с образованием изомерных
форм.  КФ
6: Лигазы,
катализирующие образование химических
связей C—C, C—S, C—O и C—N между субстратами
за счёт реакций конденсации, сопряжённых
с гидролизом АТФ. Пример: лигаза
КФ
6: Лигазы,
катализирующие образование химических
связей C—C, C—S, C—O и C—N между субстратами
за счёт реакций конденсации, сопряжённых
с гидролизом АТФ. Пример: лигаза 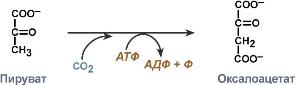 КФ
7: Транслоказы,
катализирующие перенос ионов или молекул
через мембраны или их разделение в
мембранах. Например, при переносе
протонов из матрикса митохондрии в
межмембранное пространство через
комплекс I электрон-транспортной цепи
(7.1.1.2) происходит восстановление убихинона
до убихинола, и реакция описывается
следующей схемой: NADH + CoQ + 6 H+[side 1] = NAD+ +
CoQH2 + 7 H+[side 2]. Второй пример — АТФ-синтаза,
катализирующая реакцию переноса протонов
из межмембранного пространства
митохондрии в матрикс с образованием
при этом молекулы АТФ из АДФ и
неорганического фосфата, реакция
описывается схемой[3]: АДФ + Фн + 4 H+[side 1]
→ АТФ + H2O + 4 H+[side 2]. Второе число в
наименовании фермента отражает подкласс,
третье — подподкласс, а четвёртая —
порядковый номер фермента в его
подподклассе. Будучи катализаторами,
все ферменты ускоряют как прямую, так
и обратную реакции, поэтому, например,
лиазы способны катализировать и обратную
реакцию — присоединение по двойным
связям.
КФ
7: Транслоказы,
катализирующие перенос ионов или молекул
через мембраны или их разделение в
мембранах. Например, при переносе
протонов из матрикса митохондрии в
межмембранное пространство через
комплекс I электрон-транспортной цепи
(7.1.1.2) происходит восстановление убихинона
до убихинола, и реакция описывается
следующей схемой: NADH + CoQ + 6 H+[side 1] = NAD+ +
CoQH2 + 7 H+[side 2]. Второй пример — АТФ-синтаза,
катализирующая реакцию переноса протонов
из межмембранного пространства
митохондрии в матрикс с образованием
при этом молекулы АТФ из АДФ и
неорганического фосфата, реакция
описывается схемой[3]: АДФ + Фн + 4 H+[side 1]
→ АТФ + H2O + 4 H+[side 2]. Второе число в
наименовании фермента отражает подкласс,
третье — подподкласс, а четвёртая —
порядковый номер фермента в его
подподклассе. Будучи катализаторами,
все ферменты ускоряют как прямую, так
и обратную реакции, поэтому, например,
лиазы способны катализировать и обратную
реакцию — присоединение по двойным
связям.
