
Alkenes
.pdf
Алкены
СnH2n
H2C |
|
CH2 |
H2C |
|
CH |
H2C |
|
CH |
||
|
|
|
||||||||
|
|
|
||||||||
этилен |
пропен CH3 |
|
|
H2C |
|
CH3 |
||||
|
|
|
||||||||
этен |
|
|
|
бутен-1 |
||||||
Алкены |
1 |

Номенклатура и изомерия алкенов
1 |
2 |
|
|
1 |
4 |
|
4 |
|
||||
|
|
H3C |
|
CH3 |
H |
|
|
CH |
||||
H C |
|
CH |
|
|||||||||
|
|
|
|
|
|
2 3 |
3 |
|||||
2 |
3 |
4 |
2C |
|
C 3 |
|
C |
|
C |
|
||
|
|
|
|
|||||||||
|
|
H2C |
|
CH3 |
|
1 |
|
|
||||
|
|
|
|
|
||||||||
|
|
|
|
|
|
|||||||
|
|
|
|
|||||||||
бутен-1 |
|
H |
|
H |
H3C |
|
|
H |
|
|||
|
|
|
|
|
цис-бутен-2 |
транс-бутен-2 |
||||||
|
|
|
|
|
Z-бутен-2 |
E-бутен-2 |
|
|||||
1 |
2 |
|
|
|
|
|
|
|
|
|
4 5 |
|||
H C |
|
CH |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H C |
|
CH |
H |
H2C CH3 |
|||||||||
|
|
|
||||||||||||
|
2 |
3 |
4 |
2 |
|
|
2 |
|
|
3 |
|
|
||
|
|
|
|
|
|
|||||||||
|
|
|
CH |
|
CH3 |
1 C |
C |
|||||||
|
|
|
|
5 |
|
CH3 |
||||||||
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
H3C |
|
||||||
|
|
|
|
|
H C |
Е-3-метилпентен-2 |
||||||||
|
|
|
|
3 |
6 |
|
|
|||||||
5-метилгексен-1
Алкены |
2 |

Физические свойства алкенов
С2-С4 – газы; С5-С17 – жидкие; >С18 – твёрдые
Алкен Этилен С2Н4
Пропен С3Н6 Цис-бутен-2 С4Н8 Транс-бутен-2 С4Н8 Гексен-1 С6Н12 Децен-1 С10Н20
Т.пл., С Т.кип., С
-169 -104
-186 -47
-139 4
-105 1
-140 63.5
-87 171
Алкены |
3 |
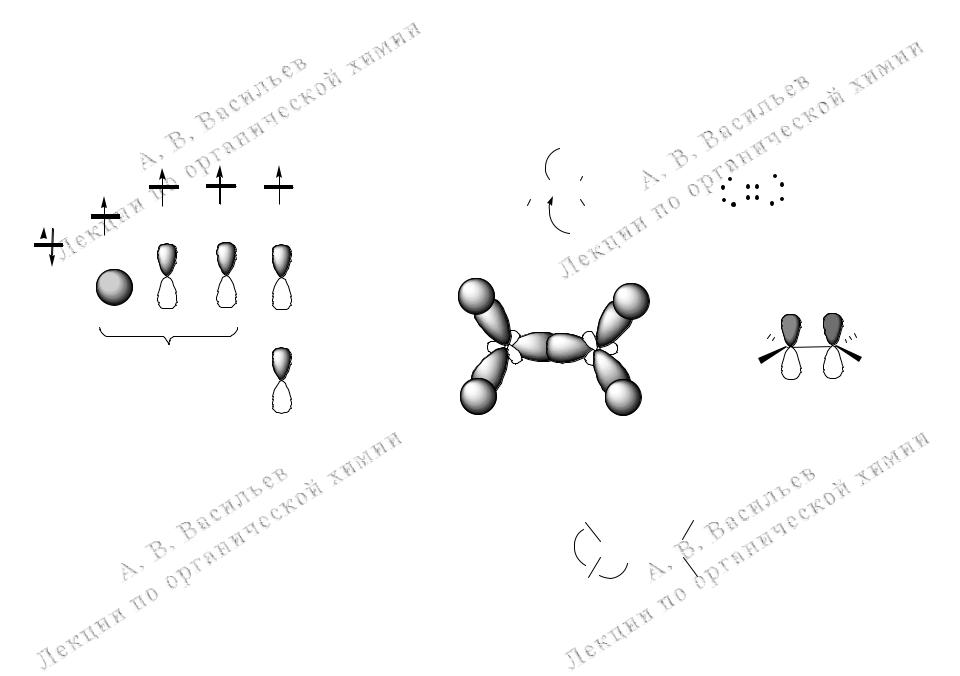
sp2-Гибридизация атома углерода. Строение этилена
2p 2p 2p
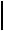 2s 1s2
2s 1s2 
s + 2 p
3

sp2-гибридные орбитали p-орбиталь
-связь
H H sp2 C
C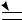 Csp2
Csp2
|
H |
H |
|
|
-связь |
s |
H |
s |
|
H |
|
sp2 |
sp2sp2 |
|
sp2 |
||
sp |
2 C |
C |
|
sp2 |
|
H H
s -связи, s
образуемые sp2-орбиталями
H |
1.33Å |
|
|
116.6o |
|
||
C |
|
C |
|
|
|||
H |
121.7o |
|
|
H |
H |
C |
C |
H |
H |
p p
H


 H
H
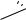 C C
C C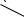
H H
-связь -
перекрывание p-орбиталей
H
1.076Å
H
Алкены |
4 |

Способы получения алкенов
1. Реакции отщепления (элиминирования)
C C
 C
C C
C
-XY
X Y
X = Y = H
X = Y = Hlg
X = H, Y = Hlg
X = H, Y = OH X = H, Y = +NR3
1.1 Дегидрирование алканов (промышленный способ получения алкенов)
|
|
|
Cr O , 450oC |
|
|
|
|
|
|
|
2 |
3 |
|
|
|
|
|
H2 |
|||
H3C |
|
CH3 |
|
|
H2C |
|
CH2 |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|||||
Алкены |
5 |
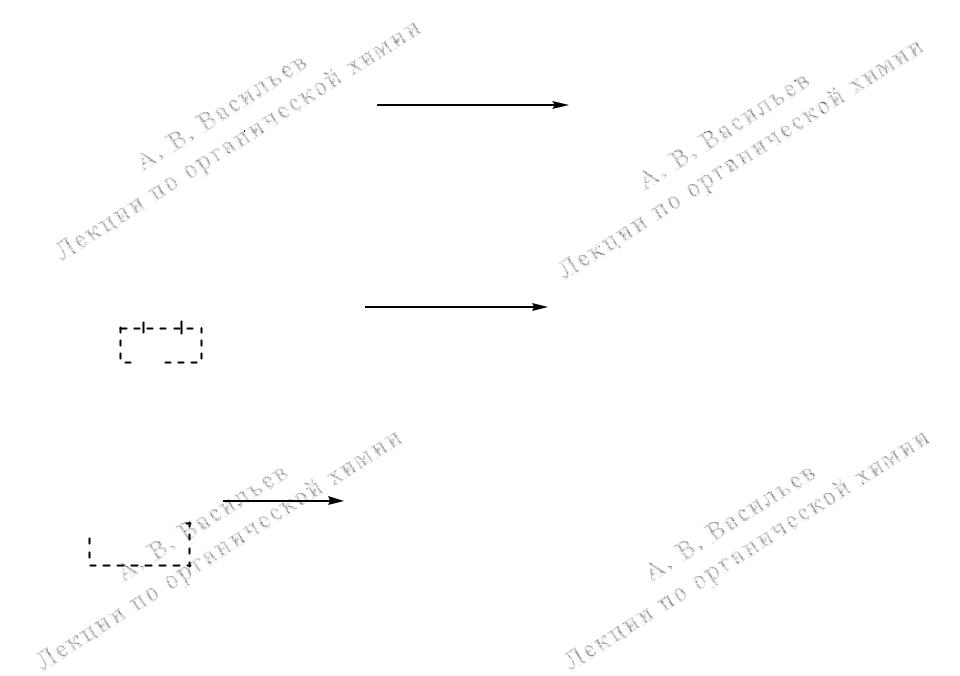
1.2 Дегалогенирование вицинальных дигалогеналканов
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3CH2OH |
|
|
|
|
|
|
H3CHC |
|
|
|
|
|
CH2 |
|
|
|
Zn |
или CH3CO2H |
H3CHC |
|
CH2 |
|
|
ZnBr2 |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
to |
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пропен |
||||||
|
|
|
|
Br Br |
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1,2-дибромпропан
1.3 Дегидрогалогенирование галогеналканов
|
|
H |
|
|
|
CH3CH2OH |
|
|
|
|
|
|
|
|
|
|||
H3C |
|
C |
|
CH2 |
|
|
KOH |
|
H3CHC |
|
CH2 |
|
|
KCl |
|
|
|
H2O |
|
|
|
|
|
|
|
|
|
||||||||||
to
Cl H 2-хлорпропан
1.4 Дегидратация спиртов
H C |
|
|
|
CH |
|
H2SO4 |
H C |
|
CH |
|
|
|
H O |
||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 180oC |
2 |
|
|
2 |
2 |
|||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
H OH
Реагенты для дегидратации спиртов: H2SO4, H3PO4, Al2O3, ThO2, цеолиты; реакция протекает при нагревании 100 – 350 С
Алкены |
6 |

Правило Зайцева (1875 г.) |
Александр |
Михайлович |
|
|
Зайцев (1841-1910), |
|
русский химик. |
При отщеплении галогеноводородовот галогеналканов или воды от спиртов водород преимущественноотрывается от наименеегидрогенизированного(имеющего меньшее число
атомов водорода) атома углерода, при этом образуется алкен с наибольшим числом заместителей при двойной связи.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
KOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
CH3 |
|
|
|
|
CH2 |
|
|
|
C |
|
CH3 |
|
|
CH3 |
|
|
|
CH |
|
|
CH |
|
CH3 |
|
|
CH3 |
|
|
CH2 |
|
CH |
|
CH2 |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
бутен-2 (80%) |
|
|
бутен-1 (20%) |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br |
|
|
|
|
|||||||||||||||||||||||||||||
|
наименее гидрогенизированный |
по правилу Зайцева |
|
|
против правила Зайцева |
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
атом углерода |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
CH3 |
|
|
H C |
|
|
|
|
|
|
CH |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2SO4 |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
||||||||||
H3C |
|
|
C |
|
|
CH2 |
|
|
CH3 |
|
C |
|
CH |
|
|
CH3 |
|
|
|
|
|
H2C |
|
|
C |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
|
|
H2C |
|
CH3 |
|||||||||||||||||||
|
|
|
|
OH |
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2-метилбутен-2 (90%) |
|
|
2-метилбутен-1 (10%) |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
по правилу Зайцева |
|
|
против правила Зайцева |
|||||||||||||||||||||||
Алкены |
7 |

Объяснение правила Зайцева.
В результате реакций дегидрогалогенирования и дегидратации образуются термодинамически более стабильные, наиболее замещённые алкены.
Ряд термодинамической стабильности алкенов:
R2C CR2 > R2C
CR2 > R2C CHR > R2C
CHR > R2C CH2 > RHC
CH2 > RHC CHR > RHC
CHR > RHC CH2
CH2
Алкены |
8 |
1.5 Пиролиз тетраалкиламмониевых солей по Гофману (1851 г.).
Реакция идёт против правила Зайцева!
Август Гофман
(1818-1892),
немецкий
химик
|
|
|
|
|
|
|
|
H |
to |
|
|
|
|
|
|
|
|||||
CH3 |
|
CH2 |
|
|
|
|
|
C |
|
CH3 |
|
CH3 |
|
CH2 |
|
CH |
|
CH2 |
|||
|
|
|
|
|
|
- NMe3, - H2O |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
NMe3 OH |
|
бутен-1 (100%) |
|
||||||||||
отщепление по Гофману, против правила Зайцева
Стерические факторы в отщеплении по Гофману
вид вдоль связи С1-С2 |
вид вдоль связи С2-С3 |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
Me N |
|
неблагоприятное |
||||||
H CH C |
|
|
H H |
|
|
H 3 |
|
|
|
|
CH |
||||
|
|
|
|||||||||||||
|
анти- |
стерическое |
|||||||||||||
3 2 |
|
|
|
|
|
|
|
|
|
|
|
|
3 |
||
H |
|
|
|
H |
отщепление |
H |
|
|
|
|
|
CH3 |
перекрывание |
||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
NMe3 |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
H |
|
|
|||||||
по Гофману |
|
|
по Зайцеву |
|
|||||||||||
Алкены |
9 |
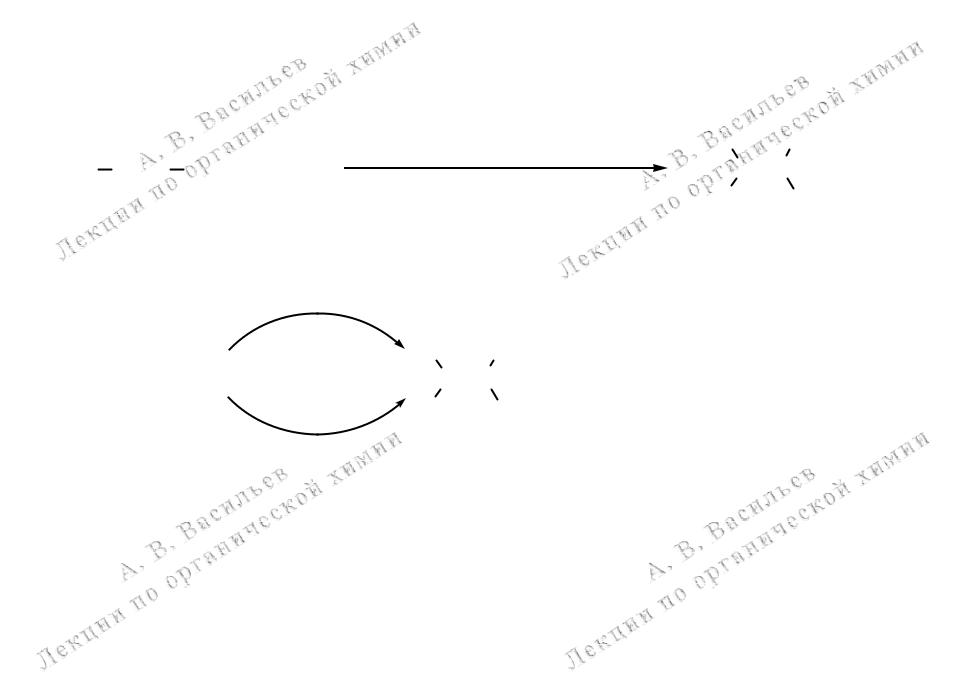
2. Частичное гидрирование алкинов
Катализатор Линдлара:
Pd, PbO, CaCO3
R C C R' + H2
C R' + H2
|
|
|
|
|
|
Na-NH3 |
|
|
|
|
R |
|
C |
|
C |
|
R' |
R |
|
|
H |
|
|
|
H |
C |
|
C |
||||
|
||||||||||
|
|
|
|
|||||||
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
R' |
|
|
|
|
|
|
|
LiAlH4 |
транс-алкен |
|||
R R'
C C
C
H H
цис-алкен
Алкены |
10 |
