
Arenes
.pdf
Производные бензола
H
H C H
C  C
C
H C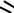 C C H
C C H
H
- арены
бензол С6H6
H |
|
H |
|
H |
H |
||
C |
|||
HC |
CH |
|
|
HC |
CH |
H |
|
C |
H |
||
H |
|
H |
|
|
|
Арены |
1 |

История открытия бензола и установления его строения
1825 г. – М. Фарадей открыл бензол в конденсате светильного газа
1834 г. – Э. Митчерлих установил эмпирическую формулу бензола
СnHn
1845 г. – А. Гофман выделил бензол из каменноугольной смолы
1860-е гг. – выдвижение гипотез о строении бензола
|
|
|
H |
|
HC |
|
|
|
|
CH |
||||
H |
|
|
|
|
|
|
|
|
|
|||||
C |
H |
|
CH |
|
||||||||||
|
|
|||||||||||||
C |
|
C |
|
|
|
|||||||||
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
C |
H |
HC |
|
|
|
|
CH |
|||||
|
|
|
||||||||||||
|
||||||||||||||
H |
C |
|
|
|
|
|
|
|
|
|||||
|
|
C |
||||||||||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
H |
|
|
|||||||||
|
|
|
|
|
H |
|||||||||
Дьюар (1867 г.) |
Ладенбург (1869 г.) |
|||||||||||||
Арены |
2 |

Структура бензола Кекуле (1865 г.)
|
|
H |
|
|
|
|
|
|
|
|
|
|
H |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H C |
|
H |
||||||
C H |
|
|
|
|
|
|
|
|
|||||||||||||||
C |
|
|
C |
|
|
|
|
|
|
|
|
C |
C |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H C C C H |
|
|
|
|
|
|
|
H C C |
C H |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
Фридрих Август Кекуле |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|||
|
|
H |
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1829-1896),немецкий химик. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Бензол – правильный шестиугольник с альтернирующими простыми и двойными связями
Арены |
3 |
Номенклатура и изомерия аренов
CH3
метилбензол (толуол)
орто-
CH3
CH3
1,2-диметилбензол, орто-диметилбензол, орто-ксилол
Cl NO2
хлорбензол нитробензол
мета-
пара-
CH3
CH3
CH3 CH3
1,3-диметилбензол, 1,4-диметилбензол, мета-диметилбензол, пара-диметилбензол, мета-ксилол пара-ксилол
Арены |
4 |

Физические свойства аренов
Арены – ароматические соединения – первоначально выделялись из ароматических масел, бальзамов, ладанов. Многие арены обладают специфическим, приятным запахом
Арен |
Т.пл., С |
Т.кип., С |
бензол |
5.5 |
80 |
толуол |
-95 |
111 |
орто-ксилол |
-25 |
144 |
мета-ксилол |
-48 |
139 |
пара-ксилол |
13 |
138 |
Арены |
5 |
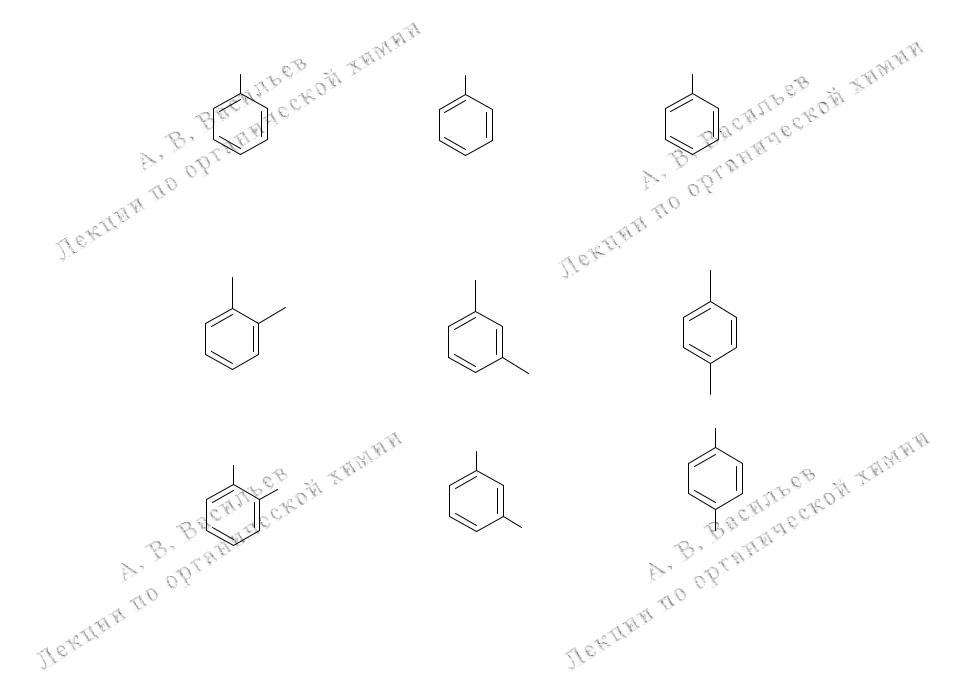
Электронное строение молекулы бензола
sp2-гибридные атомы углерода
H H
H
 H
H
H H
-связи,
образуемые sp2-орбиталями
H 1.397Å
H 
 H
H
120o
H H
H
p-орбитали образуют -связи
Перекрывание 6-ти р-орбиталей образует единую 6-ти -электронную ароматическую систему бензольного кольца
sp2-гибридные атомы углерода
Круг внутри шестиугольника бензола - это 6-ть -электронов
Арены |
6 |
Энергия сопряжения бензола
|
|
|
|
|
|
+ |
H2 |
|
|
|
|
|
|
|
|
|
|
Hэксперим. = -120.5 кДж/моль |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
циклогексен |
|
|
|
|
|
|
циклогексан |
(-28.8 ккал/моль) |
||||||||||||
|
|
|
|
|
|
|
||||||||||||||
|
|
|
+ |
3H |
|
|
|
|
|
|
|
|
|
|
|
Hрассчет. = -120.5 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
= -361.5 кДж/моль |
гипотетический |
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
циклогексан |
(-86.4 ккал/моль) |
||||||||||||||||
циклогексатриен-1,3,5 |
|
|
|
|
|
|
|
|
|
|
E (делок.) = -208.4 - (-361.5) = |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
= 153.1 кДж/моль |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(36.6ккал/моль) |
|
|
+ |
3H2 |
|
|
|
|
|
|
|
|
|
|
|
Hэксперим. = -208.4 кДж/моль |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
бензол |
|
|
|
|
|
|
циклогексан |
(-49.8 ккал/моль) |
||||||||||||
|
|
|
|
|
|
|
||||||||||||||
Молекула бензола содержит на 36.6 ккал/моль энергии меньше, чем гипотетический циклогексатриен-1,3,5, т.е. бензол стабильнее на эту величину.
Это – энергия сопряжения (делокализации) -электронов!
Арены |
7 |

Правило ароматичности Хюккеля (1930 г.)
Циклические, плоские, сопряженные полиеновые системы являются ароматическими,если они содержат (4n + 2) электронов (n = 0, 1, 2, 3 и т.д.), т.е. 2, 6, 10, 14 и т.д. электронов.
Системы, содержащие (4n) электронов (n = 0, 1, 2, 3 и т.д.) , т.е. 4, 8, 12 и т.д. электронов, являются антиароматическими.
Системы, не удовлетворяющие данным критериям, являются
неароматическими.
бензол |
|
|
|
циклобутадиен |
|
|
циклооктатетраен |
||
|
|
|
|
|
8 -электронов |
||||
6 -электронов |
|
|
|
4 -электрона |
|
|
|||
|
|
|
|||||||
|
|
|
|
|
неплоская система |
||||
|
|
|
|
|
|||||
4n+2 (при n = 1) |
|
|
|
4n (при n = 1) |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
неароматический |
||
ароматический |
|
антиароматический |
|
|
|||||
|
|
|
|
||||||
Ароматические системы являются очень стабильными и обладаютособыми химическими и физическими свойствами!
Арены |
8 |
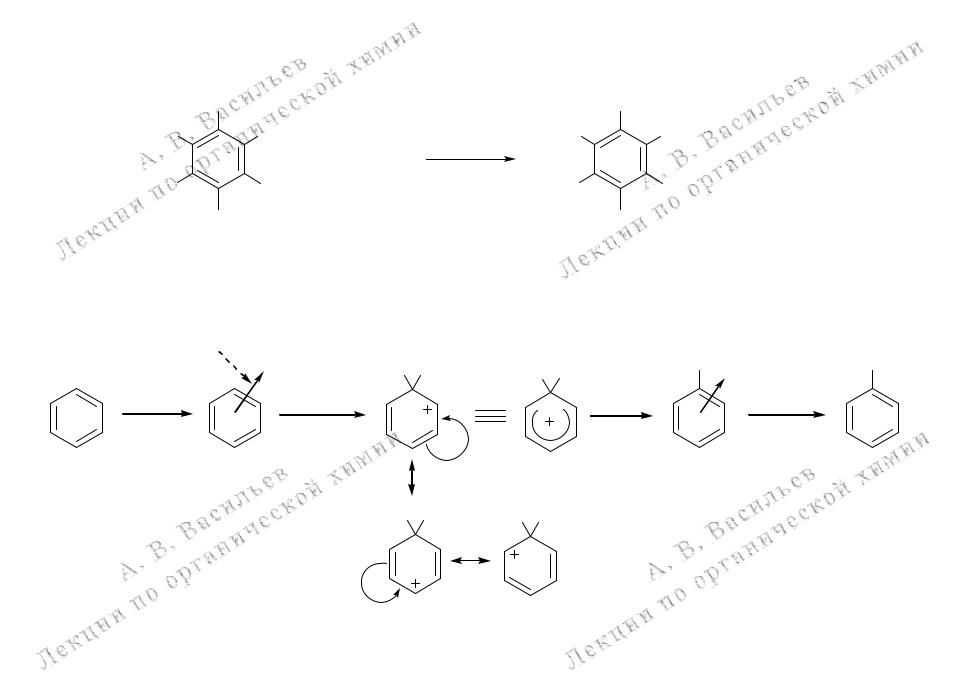
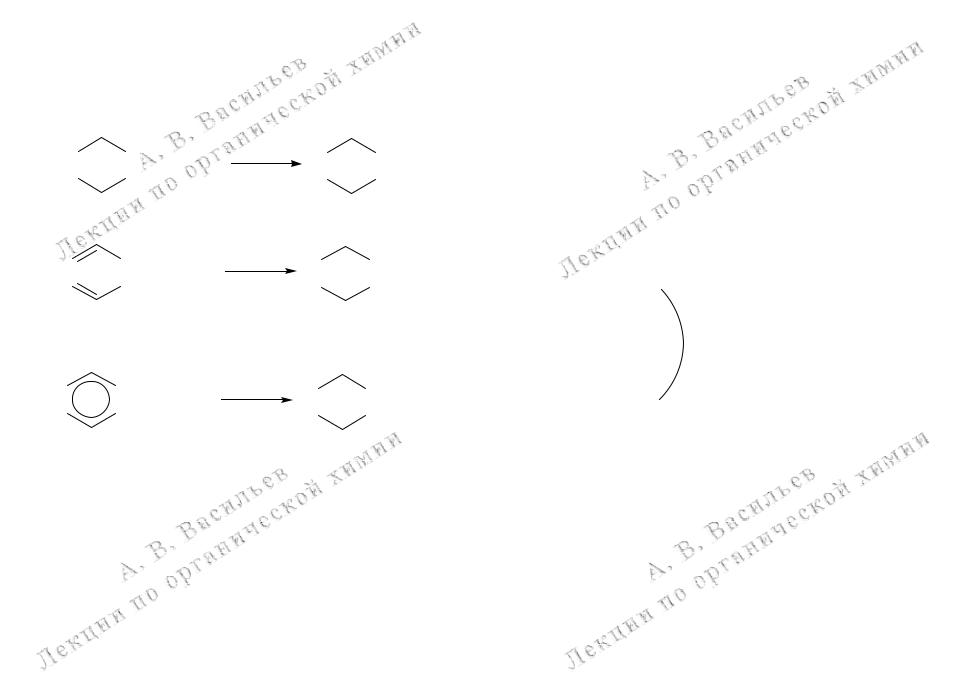
Реакции электрофильного ароматического замещения (SEAr) бензола
|
H |
|
|
E |
H |
H |
E+ |
H |
H |
|
+ |
|
+ H+ |
|
H |
H |
электрофил |
H |
H |
|
H |
|
|
H |
Обобщенный механизмреакции SEAr
смещение |
|
|
|
|
|
-электронов |
|
|
|
E |
E |
E+ |
H |
E |
H E |
||
E+ |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
-H+ |
-комплекс 1 |
|
|
-комплекс |
-комплекс 2 |
продукт |
|
|
|
|
|
реакции |
|
H |
E |
H E |
|
замещения |
резонансные структуры -комплекса
Арены |
9 |
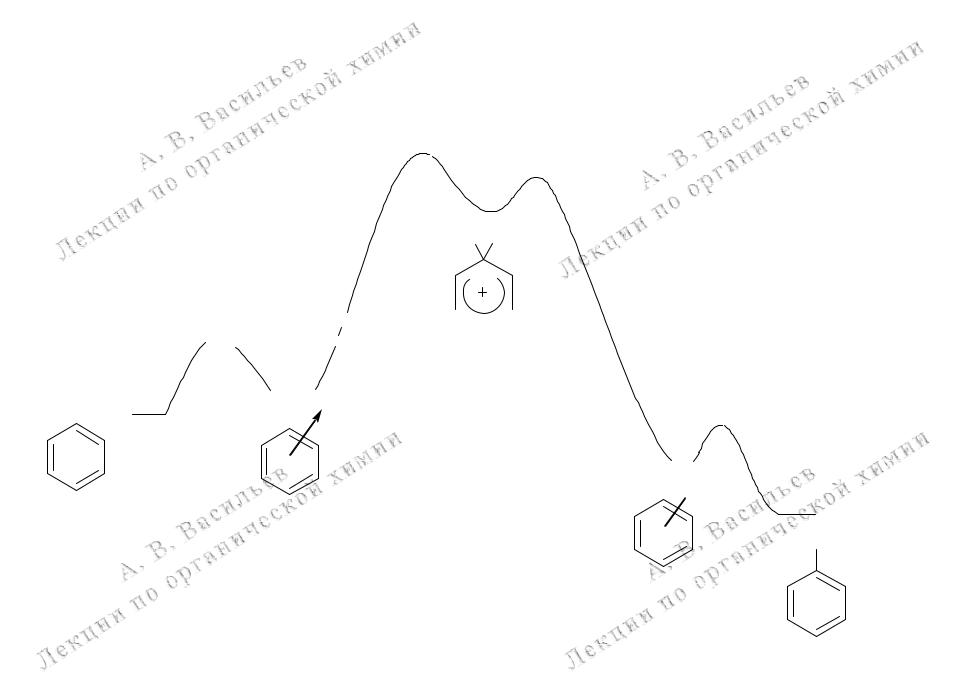
Энергетическая диаграмма реакции электрофильного ароматического замещения (SEAr)
ПС2
ПС3
H E
ПС1 







 -комплекс
-комплекс











 E+
E+
+ E+
-комплекс 1
ПС - переходное состояние
ПС4
E







 H
H
E
-комплекс 2
+ H+
Арены |
10 |
