
- •Дипломная работа
- •Введение
- •2.Литературный обзор
- •2.1.Загрязнение вод нефтепродуктами
- •2.2.Общие сведения о эмульсиях и их устойчивость
- •2.2.1 Типы и классификация эмульсии
- •2.2.2. Устойчивость эмульсии
- •2.2.3. Деэмульгирование
- •2.3.Коалесценция эмульсии
- •2.3.1 Механизм протекания коалесценции
- •2.3.2.Математическая модель коалесценции.
- •2.3.3.Сорбционно-коалесцирующий материал
- •2.4. Мембранный метод
- •2.4.1.Мембранные методы достоинства и недостатки
- •2.4.2.Ультрафильтрация для удаления нетепродуктов
- •2.4.3.Природа мембраны и среды для ультрафильтрации
- •2.4.4.Коалесценция на мембране
- •2.5.Выводы
- •3. Методическая часть
- •3.1. Описание экспериментальной установки
- •3.1.1.Общая схема установки
- •3.1.2.Мембранно-коалесцентный аппарат
- •3.2. Используемые материалы и рективы
- •3.2.1. Моторное масло
- •3.2.2. Мембраны
- •3.2.3.Сорбционно – коалесцирующие материалы
- •3.3.Методика экспериментальной работы
- •3.3.1.Методика приготовления эмульсий
- •3.3.2. Методика анализа концентрации нефтепродуктов в воде
- •3.4. Методика расчетов
- •4.Экспериментальная часть
- •4.1.Основные параметры процесса
- •4.2.Устойчивость эмульсий
- •4.3.Разделение эмульсии при комбинации «Мегасорба» и мембран в «Мегасорбе»
- •4.4.Разделение эмульсии на мембранах
- •4.5.Сравнение производительности установок
- •5.Вывод
- •Список литературы
3.4. Методика расчетов
Концентрацию нефтепродуктов (мг/дм3) в анализируемой воде вычисляем, используя формулу:
С = K · L (11)
где С - концентрация нефтепродуктов в анализируемой пробе воды, мг/дм3;
К - коэффициент преобразования, мг/(дм3 мм); L - длина окрашенного индикаторного слоя ИТ – НП, мм.
Таблица 3.4.1.
Коэффициенты преобразования для различных диапазонов
|
Диапазон измерения |
Коэффициент преобразования |
|
0,05 - 0,6 мг/дм3 |
0,026 |
|
0,5 - 6 мг/дм3 |
0,18 |
|
5 - 50 мг/дм3 |
1,8 |
Для определения размеров капель в водомасляной эмульсии использовался микроскоп Levenhuk 40L и цифровая камера DCM-35 с разрешением 0,3 МПикс. (размер кадра – 640х480 Пикс.). Микроскоп подключался к компьютеру через программу ScopePHoto и делался кадр, затем производился расчет размера капель в программе Excel.
При расчете значений удельной производительности мембраны и селективности используются следующие формулы:
 (12)
где
Q
– производительность при давлении 3
бара; n
– количество мембран (n
= 4); r
– радиус мембраны (r
= 5 мм), h-высота
мембран(h=800
мм)
(12)
где
Q
– производительность при давлении 3
бара; n
– количество мембран (n
= 4); r
– радиус мембраны (r
= 5 мм), h-высота
мембран(h=800
мм)
Для расчета коэффициента очистки при сорбционно – коалесцентном разделении используем формулу:
. (13)
(13)
где Кф. – коэффициент очистки; С – концентрация масла в пермеате, мг/л; Сисх – концентрация масла в исходной эмульсии, мг/л.
4.Экспериментальная часть
4.1.Основные параметры процесса
В результате исследований на лабораторной установке были выявлены основные параметры процесса.
Эксперименты по определению оптимального рабочего давления проводились при комбинации «Мегасорба» и мембран. В результате экспериментов оптимальное давление выбрано 3 бара и удельная производительность мембран при заданном давлении составляет:
 ,
,
где Q – производительность при давлении 3 бара; n – количество мембран (n = 4); r – радиус мембраны (r = 5 мм), h-высота мембран(h=800 мм)
Эксперименты по определению оптимальной производительности проводились только на «Мегасорбе». В результате экспериментов была выбрана производительность 52 л/ч.
Скорость в аппарате при данной производительности равна:
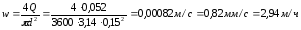
где Q – выбранная оптимальная производительность – 52 л/ч; d – диаметр аппарата, d = 150 мм = 0,15 м.
При исследовании процесса разделения водо-маслянных эмульсий необходимо изучение зависимостей производительности, концентрации пермеата и коэффициента разделения от времени проведения эксперимента при различных концентрациях исходных эмульсий 2 мг/л, 5 мг/л и 20 мг/л.
4.2.Устойчивость эмульсий
При исследовании процесса разделения водо-маслянных эмульсий необходимо убедиться в устойчивости эмульсии.
При помощи программы измеряли размер и количество капель эмульсии масло в воде в течении времени при концентрациях 5 и 20 мг/л.
Ниже представлены графики зависимости количества капель эмульсии от размера частиц в разные периоды времени при исходной концентрации 5мг/л.

Рис.4.2.1.Зависимость количества капель от размера частиц при t=30мин и Сисх= 5мг/л

Рис.4.2.2.Зависимость количества капель от размера частиц при t=60мин и Сисх= 5мг/л
 \
Рис.4.2.3.Зависимость
количества капель от размера частиц
при t=120мин
и Сисх=
5мг/л
\
Рис.4.2.3.Зависимость
количества капель от размера частиц
при t=120мин
и Сисх=
5мг/л

Рис.4.2.4.Зависимость количества капель от размера частиц при t=180мин и Сисх= 5мг/л

Рис.4.2.5.Зависимость количества капель от размера частиц при t=240мин и Сисх= 5мг/л

Рис.4.2.6.Зависимость количества капель от размера частиц при t=3,5суток и Сисх= 5мг/л
Объединив выше указанные графики на рисунке 4.2.7. показана зависимость размера капель эмульсии с концентрацией 5 мг/л от времени

Рис. 4.2.7. Зависимость размера капель эмульсии с концентрацией 5 мг/л от времени.
Ниже представлены графики зависимости количества капель эмульсии от размера частиц в разные периоды времени при исходной концентрации 20мг/л.
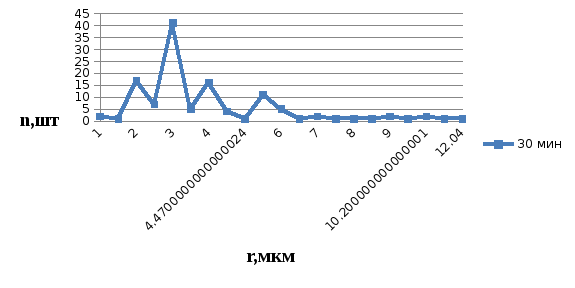
Рис.4.2.8.Зависимость количества капель от размера частиц при t=30мин и Сисх= 20мг/л

Рис.4.2.9.Зависимость количества капель от размера частиц при t=60мин и Сисх= 20мг/л

Рис.4.2.10.Зависимость количества капель от размера частиц при t=120мин и Сисх= 20мг/л

Рис.4.2.11.Зависимость количества капель от размера частиц при t=180мин и Сисх= 20мг/л

Рис.4.2.12.Зависимость количества капель от размера частиц при t=230мин и Сисх= 20мг/л

Рис.4.2.13.Зависимость количества капель от размера частиц при t=3,5суток и Сисх= 20мг/л
Объединив выше указанные графики на рисунке 4.2.14. показана зависимость размера капель эмульсии с концентрацией 20 мг/л от времени

Рис.4.2.15.Зависимость размера капель эмульсии с концентрацией 20 мг/л от времени.
В результате исследований можно сделать вывод о достаточной устойчивости эмульсии, что дает нам возможность работать с данной эмульсией.
