
- •Список теоретических вопросов к экзамену
- •Вопрос 2) Св-ва волновой функ. Понятие об уравнении Шредингера. Что такое узловые поверхности? Охарактеризуйте квантовыми числами следующее состояние электронов (в основном состоянии): ….
- •Вопрос 4) Принцип Паули и правило Хунда. Сколько максимально электронов может быть в электронном слое, электронной оболочке, на орбитали ? Какую форму имеют s-, p-, d- орбитали ?
- •Вопрос 5) Энергия электрона в многоэлектронном атоме. Энергический ряд атомных орбиталей. Напишите электронные формулы атомов …, и иона …. Какие степени окисления может иметь … в соединениях?
- •Вопрос 6) Современная формулировка периодического закона. Энергия ионизации и сродство к электрону, закономерности в их изменении по периодам и группам периодической системы.
- •Вопрос 7) Атомные и ионные радиусы, как их определяют? Как изменяются радиусы в радах: …
- •Вопрос 8) Атомные и ионные радиусы, как их определяют? Основные закономерности их изменения по периодам и группам периодической системы.
- •Вопрос 9) Относительная сила кислот и оснований (схема Косселя) на примерах … .
- •Вопрос 10) Основные положения метода валентных связей при описании химической связи. Валентные возможности атомов ….
- •Вопрос 11) Донорно – акцепторный механизм образования ковалентной связи на примерах молекул … , и ионов ….
- •Вопрос 12) Гибридизация атомных орбиталей при описании химической связи. Варианты гибридизации с участием s-, p- и d- орбиталей. Какие из приведенных молекул линейные: … ?
- •Вопрос 13) Гибридизация атомных орбиталей при описании химической связи. Варианты гибридизации с участием s-, p- и d- орбиталей. Какие из преведенных молекул плоские: … ?
- •Вопрос 14) Гибридизация атомных орбиталей при описании химической связи. Изобратите схемы перекрывания атомных орбиталей при образования связей в молекулах: …
- •Вопрос 15) Образование кратных связей. Δ- и π- связи, их особенности. Изобратите схемы перекрывания атомных орбиталей при образования связей в молекулах: …
- •Вопрос 16) Процедура наложения валентных схем в методе валентных связей для объяснения дробной кратности связи на примерах молекул … и иона …
- •Вопрос 17) Модель отталкивания локализованных электронных пар (метод Гиллеспи). Основные положения на примере молекул ….
- •Вопрос 19) Основные положения метода молекулярных орбиталей (мо лкао). Объясните парамагнитные св-ва … и найдите кратность связи в … и …
- •Вопрос 20) Основные положения метода валентных связей при описании химической связи в комплексных соединениях. Рассмотрите на примерах … и …
- •Вопрос 21) Основные положения теории кристаллического поля при описании химической связи в комплексных соединениях. Рассмотрите на примерах … и …
- •Вопрос 24) Классификация окислительно – восстановительных реакций. Преведите по 2 примера реакций каждого типа (не используйте уравнения из задания №5).
- •Вопрос 25) Типичные восстановители в овр. Каковы продукты их окисления? Приведите примеры. Классификация овр.
- •Вопрос 26) Типичные окислители в овр. Каковы продукты их восстановления? Классификация овр. Приведите примеры.
- •Вопрос 27) Общие сведения о комплексных соединениях: комплексообразователь, лиганды, координационное число, внутренняя и внешняя сферы. Классификация комплексных соединений. Приведите примеры.
- •Вопрос 28) Классификация комплексных соединений: по виду координируемых лигандов, по заряду комплексного иона, по классам соединений. Номенклатура комплексных соединений. Приведите примеры.
- •Вопрос 29) Закон Гесса, условия его выполнения. Энтальпии образовании, сгорания, атомизации (определение).
- •Вопрос 30) Закон Гесса. Следствия из закона Гесса. При каких условиях выполняется этот закон?
- •Вопрос 31) Стандартные термодинамические характеристики. Понятие о стандартном состоянии индивидуальных жидких и кристаллических в-в, газов и растворов. Закон Гесса.
- •Вопрос 32) Энтальпия и энергия Гиббса, их физический смысл, связь между ними.
- •Вопрос 34) Критерий самопроизвольного протекания реакций, энтальпийный и энтропийный факторы процесса. Какие реакции протекают самопроизвольно в водных растворах?
- •Вопрос 35) Химическое равновесие. Истинное (устойчивое) и кажущееся (кинетическое) равновесие, их признаки. Приведите примеры.
- •Вопрос 36) Химическое равновесие. Принцип Ле-Шателье – Брауна и смещение равновесия. Рассмотрите на примере реакции ……
- •Вопрос 37) Константа химического равновесия. Соотношение величин Кр и Кс для газовых равновесий. Связь и константы равновесия.
- •Вопрос 38) Равновесие диссоциации ассоциированных (слабых) электролитов на примере .... Степень диссоциации, константа диссоциации. Закон разбавления Оствалда.
- •Вопрос 39) Принципы построения шкалы стандартных термодинамических функций образования ионов в водных растворах. Как определить стандартную энтальпию образования …. В водном растворе.
- •Вопрос 40) Шкалы величин рН и рОн. Вычисление рН растворов неассоциированных электролитов на примерах ….
- •Вопрос 41) Равновесие диссоциации воды. Ионное произведение воды. Шкалы величин рН и рОн.
- •Вопрос 43) Буферные растворы и их св-ва. Расчет рН буферного раствора состава ….
- •Вопрос 44) Равновесие растворения и диссоциации малорастворимого электролита. Произведение растворимости. Связь пр и растворимости (на примере …..).
- •Вопрос 45) Условия выпадения осадка и растворения малорастворимых электролитов. Связь пр с растворимостью на примере ….
- •Вопрос 46) Произведение растворимости как константа равновесия растворения и диссоциации малорастворимого соединения. Связь пр с растворимостью на примере ….
- •Вопрос 47) Польный (необратимый) гидролиз. Взаимное усиление гидролиза (совместный гидролиз). Приведите примеры.
- •Вопрос 49) Гидролиз солей одновременно по катиону и аниону (обратимый гидролиз). Расчет константы гидролиза, степени гидролиза и рН растворов таких солей на примере …
- •Вопрос 50) Гидролиз солей по катиону. Способы подавления гидролиза. Расчет константы гидролиза, степени гидролиза и рН растворов солей, гидролизованных по катиону на примере ….
- •Вопрос 51) Гидролиз солей по аниону. Способы подавления гидролиза. Расчет константы гидролиза, степени гидролиза и рН растворов солей, гидролизованных по аниону на примере ….
Вопрос 43) Буферные растворы и их св-ва. Расчет рН буферного раствора состава ….
Буферными растворами называют такие электролитные системы, рН которых не меняется при разбавлении и мало меняется при добавлении небольших количеств сильных кислот и оснований.
Буферные р-ры на кислую область – смеси растворов слабых кислот и их солей.
Буферные растворы на щелочную область – смесь водного раствора аммиака (NH4OH) и солей аммония.
Пусть
у нас р-р слабой одноосновной к-ты и её
соли (НА+NаА).
В р-ре имеются след. равновесия: НА
![]() Н+
+
А-
; NаА
Н+
+
А-
; NаА
![]() Nа+
+ А-
.
Nа+
+ А-
.
Наличие в р-ре ионов А- за счет полностью диссоциирующей соли NаА ведет к смещению равновесия диссоциации НА влево (подавлению и без того незначительной диссоциации к-ты НА). Пусть о бщая концентрация к-ты равна Ск-ты; общая конц. соли Ссоли; степень диссоциации к-ты α. Равновесие концентрации равны:
[А-] = Ссоли + [Н+] = Ссоли + α.Ск-ты ≈ Ссоли ; так как: α<<1
[НА] = Ск-ты − [Н+] = Ск-ты – α.Ск-ты ≈ Ск-ты .
Константа
дисс. к-ты:
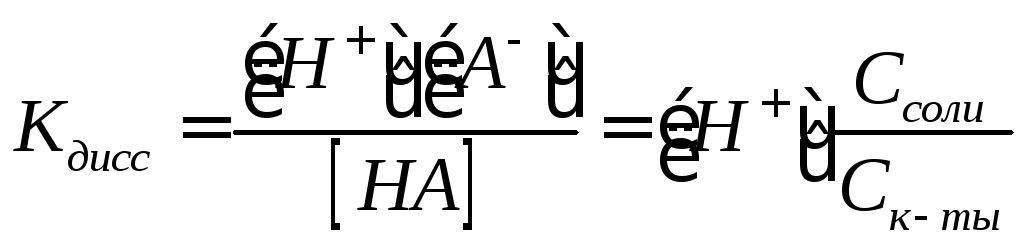 . Отсюда:
. Отсюда:
![]() .
.
Как видно:
1) при разбавлении р-ра водной ведет к одинаковому уменьшению Ск-ты и Ссоли , а отношение Ск-ты/Ссоли не изменится и рН станет прежним.
2) добавим в буферный р-р несколько капель НСl, при этом часть соли NаА превратится в к-ту НА; в результате Ск-ты немного возрастает, а Ссоли – уменьшится, а отношение Ск-ты/Ссоли и соответственно рН буферного р-ра изменится мало.
3) Подобное произойдет при вливании в буферную смесь нескольких капель р-ра NаОН: Ссоли возрастает, Ск-ты мало уменшится, а отношение Ск-ты/Ссоли и соответственно рН буферного р-ра изменится мало.
Вопрос 44) Равновесие растворения и диссоциации малорастворимого электролита. Произведение растворимости. Связь пр и растворимости (на примере …..).
KtnAm
(k)
![]() KtnAm
KtnAm
![]() nKtm+
+ mAn-
nKtm+
+ mAn-
насыщ.р-р насыщ.р-р
В водных растворах все малорастворимые электролиты не ассоциированы. Другими словами, средняя стадия написанного равновесия отсутствует.
KtnAm
(k)
![]() nKtm+
+ mAn-
nKtm+
+ mAn-
Соответствующая константа равновесия с учетом того, что концентрация индивидульаного кристаллического в-ва равна единице, принимает вид:
Kравн = [Ktm+]n.[An-]m = произведение растворимости (ПР).
Таким образом, произведение растворимости (ПР) есть константа равновесия растворения и диссоциации малорастворимого электролита. Оно численно равно произведению концентраций (активностей) ионов в степенях стехиометрических коэффициентов в насыщенном водном растворе данного малорастворимого электролита. Пусть растворимость электролита равна Р моль/л. Тогда:
[Ktm+]
= nP;
[An]
= mP;
ПР = [Ktm+]n.[An-]m
= (nP)n(mP)m
= nn.mm.Pn+m
.
Отсюда находим связь
ПР с растворимостью:
![]() .
.
Если ПК > ПР – выпадет осадок, ПК < ПР − осадок растворится, ПК = ПР − установится равновесие. (ПК = [Ktm+]n.[An-]m. ПК – произведение концентраций).
