
- •ЗАМЕЩЕННЫЕ КАРБОНОВЫЕ КИСЛОТЫ
- •КЛАССИФИКАЦИЯ. НОМЕНКЛАТУРА
- •В зависимости от положения дополнительной функциональной гр. по отношению к СООН-гр. замещенные карбоновые
- •ГАЛОГЕНОКАРБОНОВЫЕ КИСЛОТЫ
- •Способы получения α-галогензамещенные:
- •β-галогензамещенные:
- •Физические свойства
- •Реакции нуклеофильного замещения атомов галогенов
- •Реакции по карбоксильной группе:
- •ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ
- •Способы получения
- •Широко распространенные в природе α-гидроксикарбоновые к-ты могут быть
- •β-Гидроксикарбоновые кислоты получают:
- •γ- и -гидроксикарбоновые кислоты получают специальными методами.
- •Фенолкарбоновые кислоты синтезируют карбоксилированием фенолов.
- •Строение α-гидроксикарбоновые к-ты (кроме гликолевой НОСН2СООН) содержат асимметрический С-атом.
- •Физические свойства
- •Реакции по гидроксильной группе.
- •Реакции с участием ОН- и СООН- групп
- •γ- и δ-Гидроксикарбоновые к-ты при нагревании в кислой среде вступают в р-цию
- •α-гидроксикислоты при кипячении с разб. минеральными к-тами подвергаются расщеплению с образованием альдегидов и
- •Важнейшие представители
- •Гликозиды галловой кислоты – танины, содержатся в листьях чая, в кофейных зернах,
- •ОКСОКАРБОНОВЫЕ КИСЛОТЫ
- •Способы получения
- •– окислением α-гидроксикислот:
- •β-Оксокарбоновые к-ты могут быть получены гидролизом их сложных эфиров
- •Физические свойства
- •α-оксокислоты под действием разб. минеральных к-т декарбоксилируются с образованием альдегидов, а при действии
- •β-оксокислоты и их производные вследствие
- •β-оксокислоты и их соли термически нестабильные - легко распадаются при нагревании (декарбоксилируются).
- •Сложные эфиры β-оксокислот существуют в виде равновесной смеси двух таутомерных форм – оксо-формы
- •АУЭ является С-Н и О-Н кислотой средней силы, поэтому он реагирует с сильными
- •Соли АУЭ легко вступают в р-ции алкилирования и ацилирования,
- •Кетонное расщепление – осуществляют под действием кислот или разбавленных щелочей
- •Кислотное расщепление – осуществляется под действием конц. растворов щелочей и
- •Синтез кетонов и карбоновых кислот на основе АУЭ
- •Необходимо иметь ввиду:
- •Напр., рассмотрим схему синтеза пентан-2-она и бутановой кислоты.
- •Полная последовательность превращений:
- •кетонное расщепление
- •Важнейшие представители Пировиноградная кислота – бесцв. ж. с запахом уксусной кислоты.
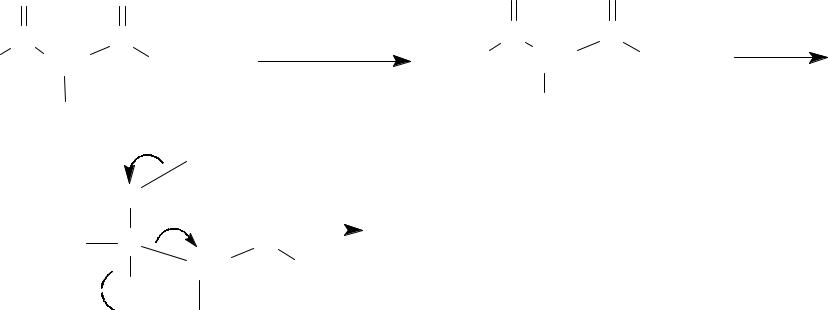
Кислотное расщепление – осуществляется под действием конц. растворов щелочей и
приводит к образованию солей алкилуксусных кислот:
O
CH3 C CH R'
 CH3
CH3
O
C OC2H5
H
O
C


 O Na CH R'
O Na CH R'
OO
NaOH |
CH C |
CH C |
ONa NaOH |
|
3 |
|
|
C2H5OH R'
O |
|
|
CH3COONa |
|
|
|
R' |
|
CH2COONa |
||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|||||
C |
|
|
|
||||||||
|
|
|
|
|
|
||||||
ONa |
|
|
|
|
|
||||||
Синтез кетонов и карбоновых кислот на основе АУЭ
Планирование синтеза:
1)получение АУЭ сложноэфирной конденсацией этилацетата;
2)алкилирование АУЭ используя соответствующий алкилгалогенид;
3)Кетонное или кислотное расщепление алкилАУЭ.

Необходимо иметь ввиду:
•при кетонном расщеплении в синтезируемом кетоне сохраняется фрагмент ацетона;
•при кислотном расщеплении в синтезируемом продукте сохраняется фрагмент уксусной кислоты.
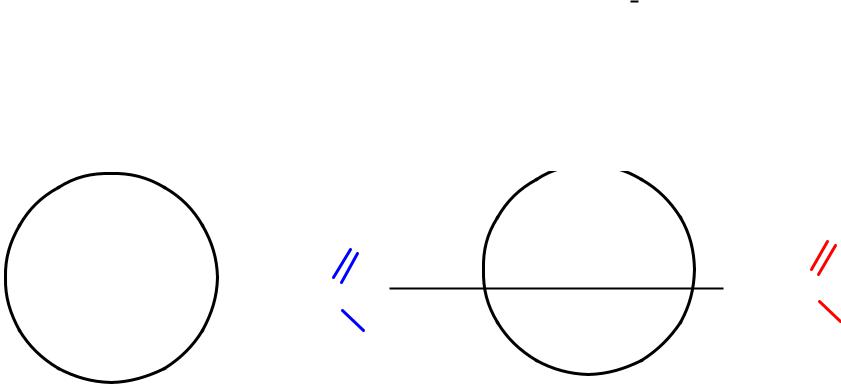
Напр., рассмотрим схему синтеза пентан-2-она и бутановой кислоты.
Для правильного выбора алкилирующего агента в синтезируемом кетоне выделим фрагмент ацетона, а в синтезируемой кислоте – фрагмент уксусной кислоты.
|
H2 |
H2 |
|
O |
|
H2 H2 |
|
O |
|
|
|
|
|
|
|
|
|||
Очевидно, что в качестве алкилирующего агента необходимо |
|||||||||
H C |
C C |
|
C |
|
H3C |
C C |
|
C |
|
|
|
||||||||
использовать3 |
этилбромид |
|
|
|
OH |
||||
|
|
|
|
CH3 |
|
|
|
||

Полная последовательность превращений:
O |
C2H5O Na |
O |
H |
|
O |
|
H3C C |
C |
Na |
||||
H3C C |
|
C |
||||
OC2H5 |
|
|
|
|
OС2H5 |
|
|
Na |
АУЭ |
|
|
||
этилацетат |
|
|
|
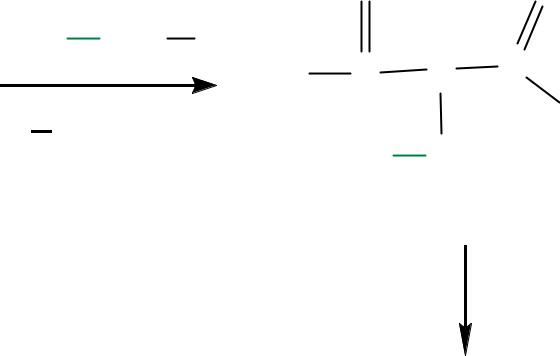
H3C CH2
NaBr
O |
H |
O |
|
Br H3C C |
C |
||
C |
H3C CH2
OС2H5
продукт С-алкилирования (этилАУЭ)
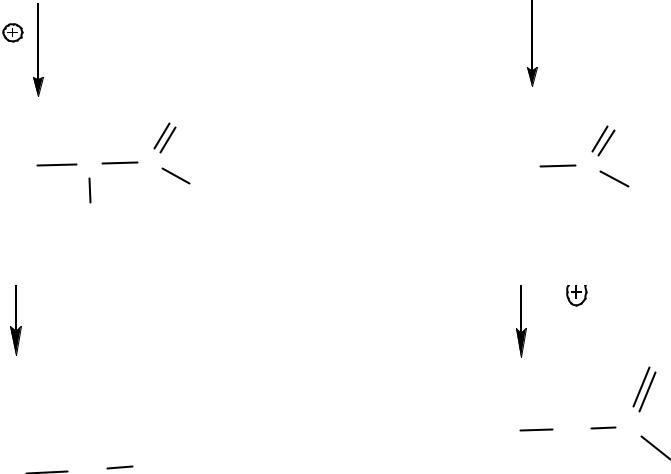
кетонное расщепление |
кислотное расщепление |
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- CH3СОONa |
|
H2O, H |
|
- C2H5OH |
|
|
|
NaOH конц. |
||||||||||||||||||||
|
|
|
|
- C2H5OH |
||||||||||||||||||||||
|
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
|
|
|
O |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
||
H3C |
|
|
|
|
C |
|
|
C |
OH |
|
|
|
H2C |
C |
ONa |
|||||||||||
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
H3C |
|
CH2 |
|
|
H3C |
|
|
CH2 |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
этилацетоуксусная кислота |
этилацетат натрия |
|||||||||||||||||||||||||
|
t |
|
|
|
|
|
|
|
- CO2 |
|
|
|
|
|
|
|
|
|
|
|
|
H |
O |
|||
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
H |
H |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
H2 |
H2 |
|
CH3 |
H3C |
|
|
C2 |
C2 C |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
H3C |
|
|
C |
|
C |
C |
|
|
|
|
|
|
|
|
|
|
ONa |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
пентан-2-он |
|
|
|
бутановая кислота |
|||||||||||||||||||||
метилпропилкетон |
этилуксусная кислота |
|

Важнейшие представители Пировиноградная кислота – бесцв. ж. с запахом уксусной кислоты.
Растворима в воде, имеет важное биологическое значение, содержится во всех тканях организма. Образуется как промежуточный продукт в процессах молочно-кислого и спиртового брожения, в биосинтезе аминоксилот.
Простогландины – важнейшие биорегуляторы.
O
COOH
HO
OH
