- •1. Предмет и задачи неорганической химии. Роль в системе естественных наук
- •3. Основные стехиометрические законы
- •4. Важнейшие классы и номенклатура неорганических веществ
- •5. Развитие учения о строении атома
- •6. Строение электронных оболочек атомов
- •7. Периодическая система элементов как форма отражения периодического закона
- •8. Периодичность свойств химических элементов
- •9. Основные типы химической связи
- •10. Ковалентная химическая связь. Основные положения метода валентных связей
- •11. Геометрия структур с ковалентным типом связи
- •12. Основы метода молекулярных орбиталей
- •13. Ионная и металлическая связь
- •14. Водородная связь
- •15. Кристаллическое, жидкое и аморфное состояние веществ
- •16. Скорость химических реакций. Константа скорости и ее физический смысл
- •17. Влияние температуры на скорость химической реакции. Основные положения теории активации Аррениуса
- •18. Влияние катализатора на скорость химической реакции
- •19. Химическое равновение. Принцип Ле-Шаталье
- •20. Основы химической термодинамики. Энтальпия системы
- •21. Понятие об энтропии
- •22. Соотношение между величиной изменения энергии Гиббса и величинами энтропии и энтальпии
- •23. Дисперсные системы. Коллоидные растворы
- •24. Растворимость веществ
- •25. Состав растворов. Способы выражения состава растворов
- •26. Основные положения теории электролитической диссоциации
- •27. Степень диссоциации электролитов. Факторы, определяющие степень диссоциации
- •28. Теория сильных электролитов. Истинная и кажущаяся степень диссоциации сильных электролитов
- •29. Основания, кислоты и соли с точки зрения теории электролитической диссоциации
- •30. Обменные реакции в растворах электролитов
- •31. Условия образования и растворения осадков
- •1) Условие выпадения осадка:
- •2) Условие растворения осадка:
- •32. Диссоциация воды. Константа диссоциации, ионное произведение воды
- •33. Гидролиз солей. Механизм гидролиза
- •34. Окислительно-восстановительные реакции. Основные типы окислительно-восстановительных реакций
- •35. Принцип электронного баланса
- •36. Метод полуреакций
- •37. Электрохимические процессы. Эдс гальванического элемента
- •38. Стандартные электродные потенциалы. Уравнение Нернста
- •39. Электрохимический ряд напряженности металлов
- •40. Электролиз водных растворов и расплавов
- •41. Химические процессы, протекающие на электродах
- •42. Основные положения координационной теории
- •43. Строение комплексного соединения
- •44. Устойчивость комплексных соединений
- •45. Водород и его свойства
- •46. Элементы VII а группы. Их характеристика
- •47. Галогены. Общая характеристика галогенов
- •48. Характер химической связи в молекулах галогенов. Их физические и химические свойства
- •49. Галогенводороды. Физические и химические свойства
- •50. Кислородсодержащие соединения галогенов
- •51. Общая характеристика элементов via группы (халькогены)
- •52. Физические свойства халькогенов
- •53. Химические свойства простых веществ (халькогенов)
- •54. Физические и химические свойства гидридов типа h2э в ряду h2o – h2Te
- •55. Соединения кислорода с водородом. Их свойства, общие принципы получения, применение
- •56. Кислые и средние халькогениды. Их свойства, общие принципы получения, применение
- •57. Оксиды халькогенов, их свойства, принципы получения, применение
- •58. Сернистая, селенистая, теллуристая кислоты. Строение, свойства и их солей
- •59. Серная, селеновая, теллуровая кислоты. Строение, свойства и их солей
- •60. Свойства разбавленной и концентрированной серной кислоты. Олеум. Соли и их практическое применение
- •61. Сульфаты и гидросульфаты. Купоросы и квасцы. Их применение
- •62. Полисерные, перексосерные, политионовые кислоты. Химические свойства. Соли и их практическое применение.
- •63. Общая характеристика элементовVa группы.
- •65. Гидриды типа эн3 элементов va группы.
- •66. Аммиак, его физические и химические свойства.
- •67. Оксиды азота, строение их молекул, химические свойства, способы получения, применение.
- •68. Азотистая кислота, ее соли.
- •69. Азотная кислота и ее соли.
- •I. Кислотно-основные свойства.
- •II. Окислительно-восстановительные свойства.
- •70. Кислородсодержащие соединения фосфора.
- •71. Кислородсодержащие кислоты фосфора и их соли.
- •Метафосфорная кислота
- •Ортофосфорная кислота h3po4
- •Полифосфорная кислота
- •Фосфористая кислота h3po3
- •72. Общая характеристика элементов ivа группы.
- •73. Строение и свойства простых веществ элементов ivа группы
- •74. Гидриды типы эн4 в ряду сн4 – PbH4
- •75. Кислород содержащие соединения углерода
- •76. Угольная кислота и ее соли
- •77. Кислородсодержащие соединения кремния
- •78. Кремневые кислоты и их соли
- •79. Общая характеристика металлов
- •80. Щелочные металлы. Их физические и химические свойства
- •81. Общая характеристика и свойства оксидов, пероксидов, гидроксидов и солей щелочных металлов.
- •82. Щелочноземельные металлы. Общая характеристика элементов. Физические и химические свойства простых веществ.
- •83. Общая характеристика оксидов, гидроксидов, солей элементов iiа группы.
- •84. Алюминий, его физические и химические свойства. Амфотерность алюминия. Алюминаты. Получение алюминия и его солей.
- •85. Металлы ivа группы. Сопоставление их физических и химических свойств со свойствами углерода и кремния.
- •86. Общая характеристика p- элементов. Физические и химические свойства простых веществ.
- •87. Общая характеристика элементов групп меди и цинка.
- •88. Общая характеристика элементов группы хрома.
- •89. Общая характеристика элементов группы марганца.
- •90. Общая характеристика элементов семейства железа.
41. Химические процессы, протекающие на электродах
В гальваническом элементе – анодом является электрод, погруженный в раствор с меньшой концентрацией, катодом является электрод, погруженный в раствор с большей концентрацией. Составим электрохимическую схему концентрационного гальванического элемента, образованного двумя серебряными пластинами, погруженными в растворы нитрата серебра разных концентраций С1 и С2 (причем С1 < С2):
А (–) Аg | АgNО3 || АgNO3 | Аg (+) К
С1 < С2
Процессы, протекающие на электродах:
А (–) Ag 0 – ē = Ag + окисление
К (+) Ag + + ē = Ag 0 восстановление
Поскольку анодом и катодом является один и тот же металл, то ЭДС такого элемента может быть определена по формуле:
ЭДС
=
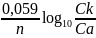
где Сk – концентрация раствора на катоде, моль/л;
Сa – концентрация раствора на аноде, моль/л.
В ходе работы такого гальванического элемента, концентрация первого раствора С1 (Сa) будет постепенно увеличиваться, а второго раствора С2 (Сk) уменьшаться. По уравнению ЭДС будет уменьшаться. Через некоторое время концентрации С1 и С2 станут одинаковыми, а ЭДС – равной нулю.
42. Основные положения координационной теории
Основные положения «Координационной теории» Вернера
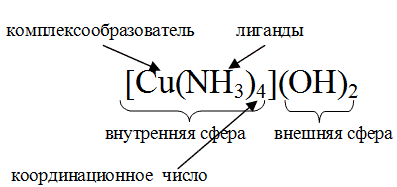
1. В любом комплексном соединении есть внутренняя и внешняя сфера.Внутренняя сфера называется «комплексным ионом» и заключается в квадратные скобки. В химических реакциях или в кристаллической структуре комплексный ион выступает как самостоятельная единица: K3[Fe(CN)6] ↔ 3K+ + [Fe(CN)6]3─
2. Центральный атом внутренней сферы называется комплексообразователем (КО) или ядром комплекса. Роль комплексообразователя выполняют чаще всего катионы металлов, напр. [Fe(CN)6]3─, [Co(NH3)6]2+, реже нейтральные атомы - Ni(CO)4 или анионы - [NH4]+.
3. Ионы или молекулы, которые координируются вокруг центрального атома во внутренней сфере, называются лигандами (от латинского liganda - «то, что связано») или аддендами (от латинского addenda - «то, что добавлено»).
4. Координационное число – это число лигандов, которое удерживается комплексообразователем. Координационное число обычно бывает больше, чем степень окисления КО:
Заряд центрального иона координационного числа
+1 2
+2 4, 6
+3 6, 4
+4 8
Координационное число (к.ч.) зависит от: 1) природы КО и лигандов; 2) размеров КО и лигандов.
5.Число мест во внутренней сфере, которые занимает один лиганд, называется координационной емкостью лиганда. Монодентатный лиганд связан с комплексообразователем только одним из своих атомов: NH3, OH─.
Бидентатный лиганд – двумя атомами: CO32-, SO42-, C2O42- и т.д.
Полидентатные лиганды связаны с комплексообразователем тремя и более атомами (например, ЭДТА занимает 6 мест во внутренней сфере).
6. Заряд комплексного иона численно равен алгебраической сумме зарядов всех составляющих его ионов. С другой стороны, заряд внутренней сферы равен по абсолютному значению и противоположен по знаку заряду внешней сферы.
В целом, комплексные соединения – электронейтральны.
43. Строение комплексного соединения
Комплексное соединение – химическое вещество, в состав которого входят комплексные частицы.
Комплексообразователь – центральный атом комплексной частицы. Обычно комплексообразователь – атом элемента, образующего металл, но это может быть и атом кислорода, азота, серы, иода и других элементов, образующих неметаллы. Комплексообразователь обычно положительно заряжен; заряд комплексообразователя может быть также отрицательным или равным нулю.
Лиганды (Адденды) – атомы или изолированные группы атомов, располагающиеся вокруг комплексообразователя. Лигандами могут быть частицы, до образования комплексного соединения представлявшие собой молекулы (H2O, CO, NH3 и др.), анионы (OH-, Cl-, PO43-др.), а также катион водорода H+.
Внутренняя сфера комплексного соединения – центральный атом со связанными с ним лигандами.
Внешняя сфера комплексного соединения – остальные частицы, связанные с комплексной частицей ионной или межмолекулярными связями, включая водородные.
Координационное число – число связей, образуемых центральным атомом с лигандами.