- •Часть 2. Кислородсодержащие классы органических соединений
- •Омск – 2016
- •Кандидат биологических наук, доцент и.В. Конева – доцент кафедры математических и естественнонаучных дисциплин фгбоу впо ОмГау им. П.А. Столыпина
- •Предисловие
- •Основные положения протонной теории кислот и оснований:
- •Факторы, влияющие на кислотные свойства органических соединений
- •1. Природа элемента в кислотном центре
- •2. Стабильность аниона за счёт сопряжения
- •3. Влияние радикала на стабильность аниона
- •4. Влияние растворителя на стабильность аниона
- •Гидроксисоединения
- •Классификация спиртов
- •I. По количеству –он групп спирты:
- •Классификация фенолов по количеству –он групп
- •Химические свойства спиртов
- •2. Реакция нуклеофильного замещения (sn).
- •Химические свойства фенолов
- •3. Реакция нитрования фенола:
- •4. Реакция сульфирования фенола: (sе )
- •Контрольные вопросы
- •Типовые задания
- •Тестовые задания для самоконтроля
- •Контрольные задания
- •Литература Основная литература
- •Дополнительная литература
- •Электронные образовательные ресурсы
- •1.2. Карбонильные соединения
- •Химические свойства
- •Контрольные вопросы
- •Типовые задания
- •Тестовые задания для самоконтроля
- •Электронные образовательные ресурсы
- •1.3 Карбоксильные соединения. Карбоновые кислоты. Гидроксикислоты. Кетонокислоты
- •I. По количеству карбоксильных групп
- •1. Одноосновные (монокарбоновые) кислоты:
- •2. Поликарбоновые кислоты, содержащие две или более
- •II. В зависимости от наличия младших функциональных групп в радикале карбоновой кислоты
- •1. Гидроксикислоты, содержащие группу –он:
- •Строение карбоксильной группы
- •Химические свойства карбоновых кислот
- •Реакции галогенирования (реакции в сн-кислотном центре):
- •Пути превращения ацетоуксусной кислоты в организме:
- •Медико-биологическое значение карбоновых кислот
- •Контрольные вопросы
- •Типовые задания
- •Кислота, дихлоруксусная кислота, уксусная кислота.
- •Тестовые задания для самоконтроля Выберите один правильный ответ
- •Контрольные задания
- •Литература Основная литература
- •Дополнительная литература
- •Электронные образовательные ресурсы
- •1.7 Контрольная работа «кислородсодержащие классы органических веществ» Контрольные вопросы
- •Типовые задания вариант билета рубежной контрольной работы «кислородсодержащие классы органических соединений».
- •Электронные образовательные ресурсы
- •2. Инструкция по охране труда и пожарной безопасности для студентов при работе в лабораториях кафедры химии
- •2.1. Общие требования безопасности
- •2.2. Требования безопасности перед началом работы
- •2.3. Требования безопасности во время работы
- •2.4. Требования безопасности в аварийных ситуациях
- •32.05.01 Медико-профилактическое дело
- •Демонстрационный вариант зачетной работы по дисциплине «Химия биополимеров»
- •Демонстрационный вариант билета зачетной работы Билет № 1
- •В пятибалльную систему оценки зачетной работы
- •Заключение
- •Глоссарий
- •Ответы на тестовые задания
- •Литература Основная литература
- •Дополнительная литература
- •Приложения
Контрольные вопросы
Карбоновые кислоты, их классификация, номенклатура, изомерия.
Электронное строение карбоксилат-аниона.
Химические свойства карбоновых кислот. Реакции диссоциации, галогенирования, декарбоксилирования, этерификации.
Медико-биологическое значение карбоксильных соединений.
Гидроксикислоты и кетонокислоты, их строение, изомерия, номенклатура.
Химические свойства гидрокси- и кетонокислот. Реакции диссоциации, декарбоксилирования, этерификации.
Реакции окисления молочной кислоты, β-гидроксимасляной кислоты, яблочной кислоты. Пути превращения β-гидроксимасляной кислоты в организме. Реакция окислительного декарбоксилирования пировиноградной кислоты.
Медико-биологическое значение гидрокси- и кетонокислот и их производных. Салициловая кислота и фармпрепараты на ее основе, их получение и применение в медицине.
Типовые задания
Задание 1. Опишите влияние заместителей на кислотные свойства карбоновых кислот. Расположите соединения в ряд по уменьшению кислотности: уксусная кислота, дихлоруксусная кислота, трихлоруксусная кислота.
Решение. Электронодонорные заместители снижают кислотность, электроноакцепторные заместители – усиливают. Галогены относят к электроноакцепторным заместителям, причем увеличение числа атомов галогена усиливает кислотность. Таким образом, соединения по уменьшению кислотности располагаются в ряд: трихлоруксусная
Кислота, дихлоруксусная кислота, уксусная кислота.
Задание 2. Реакции этерификации протекают in vivo. Из предложенных реакций выберите реакцию этерификации:
1) C2H5 – OH + C2H5 – OH → C2H5 – O – C2H5 + Н2О |
2) NaOH + СН3 – СООН → CH3 – COONa + Н2О |
3) C2H5 – OH + CH3 – COOH ↔ CH3 – CO – O – C2H5 + H2O |
4) C2H5 – OH → C2H4 + Н2О. |
Решение:
При взаимодействии карбоновых кислот со спиртами в присутствии кислотных катализаторов образуются сложные эфиры, а реакция называется – этерификацией:
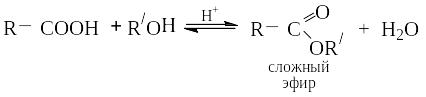 Ответ:
3.
Ответ:
3.
Задание 3. Предложите схему синтеза молочной кислоты из 2-хлорпропановой кислоты. Обладает ли полученная кислота оптической активностью? Какой продукт образуется при нагревании молочной кислоты? Напишите схему реакции.
Решение:
Гидроксикислоты получают из галогенкарбоновых кислот в результате обработки их щелочью с последующим взаимодействием образующейся соли гидроксикислоты с кислотой:
Для гидроксикислот характерна оптическая изомерия, связанная с наличием асимметрических углеродных атомов. Многие гидроксикислоты, например молочная, яблочная, винная, изолимонная, имеют в молекуле хиральные центры. Так, молочная кислота существует в трех формах: две оптически активные, т.е. энантиомеры (зеркальные изомеры), а третья – оптическая неактивная, являющаяся рацемической смесью энантиомеров. Молочная кислота, выделенная из мышечной ткани, является L-энантиомером. D-молочная кислота образуется из сахаров при помощи особых бактерий-возбудителей брожения. Под действием молочнокислых бактерий образующаяся молочная кислота является рацемической смесью обоих энантиомеров и не проявляет оптической активности:
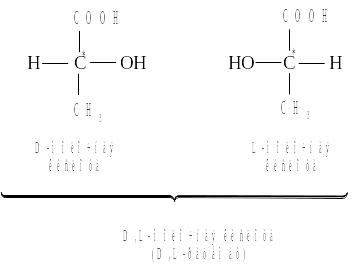
Так как молочная кислота относится к α-гидроксикислотам, то она при нагревании образует устойчивый шестичленный циклический диэфир-лактид:
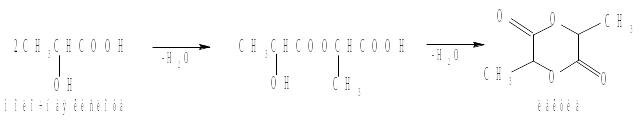
Задание 3. Какое соединение образуется при нагревании
β-гидроксимасляной кислоты?
Решение:
β-гидроксимасляная кислота относится к β-гидроксикислотам, а этим кислотам при нагревании или под действием минеральных кислот характерны реакции дегидратации с образованием α,β-ненасыщенных кислот:
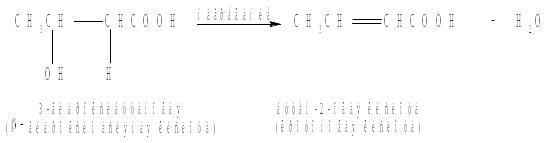
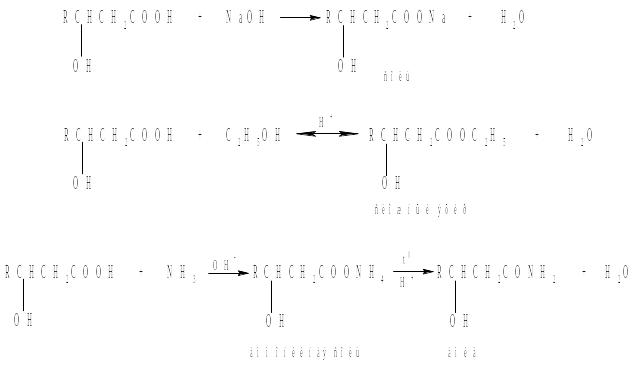
Задание 4. Напишите схему реакций взаимодействия β-гидроксикислоты с гидроксидом натрия, этанолом и аммиаком. Назовите продукты реакции.
Решение:
Наличие в молекуле гидроксикислот карбоксильной и гидроксильной групп приводит к тому, что эти соединения вступают в реакции, свойственные как спиртам, так и кислотам. С гидроксидом натрия, этанолом и аммиаком реакции идут по карбоксильной группе: