
- •Лабораторный практикум по химии
- •Ведение
- •Цель работы
- •Теоретические сведения
- •Важнейшие законы химии
- •Подготовка к работе
- •Типовая задача
- •Рабочее задание
- •Отчёт о выполнении работы включает:
- •Задание для самостоятельной работы
- •Цель работы
- •Теоретические сведения
- •Молярная масса газа (из 2.1.) равна
- •Подготовка к работе Изучите теоретические вопросы и пример решения типовой задачи:
- •Рабочее задание Задание 1. Определение молекулярной массы углекислого газа
- •Результаты опыта по определению молекулярной массы со2
- •Отчёт о выполнении работы включает:
- •Задание для самостоятельной работы
- •Цель работы
- •Теоретические сведения
- •Данные для расчета молярной массы эквивалента
- •Отчёт о выполнении работы включает:
- •Задание для самостоятельной работы
- •Соединений Цель работы
- •Теоретические сведения
- •Подготовка к работе
- •Рабочее задание Задание 1. Изучение свойств оснóвных оксидов
- •Задание 2. Изучение свойств кислотных оксидов
- •Задание 3. Получение и изучение свойств гидроксидов
- •Задание 4. Составление уравнений реакций получения солей
- •Отчёт о выполнении работы включает:
- •Задание для самостоятельной работы
- •И химическая связь Цель работы
- •Теоретические сведения
- •Подготовка к работе
- •Рабочее задание Задание 1. Изучение химических свойств элементов третьего периода периодической системы и их оксидов
- •Задание 2. Изучение особенностей изменения химических свойств в ряду простых веществ Si, Ge, Sn, Pb
- •Задание 3. Сравнение химической активности брома и йода
- •Задание 4. Изучение механизма образования ковалентной связи
- •Отчёт о выполнении работы включает:
- •Задание для самостоятельной работы
- •Темы рефератов
- •Цель работы
- •Теоретические сведения
- •Подготовка к работе
- •Типовая задача
- •Задание 2. Определение теплоты нейтрализации сильной кислоты сильным основанием
- •Отчёт о выполнении работы включает:
- •Задание для самостоятельной работы
- •Подготовка к работе
- •Типовая задача
- •Рабочее задание
- •Реагирующих веществ
- •Зависимость скорости реакции от температуры
- •Задание 4. Влияние температуры на смещение химического равновесия
- •Цель работы
- •Теоретические сведения
- •Реакция среды характеризуется через водородный показатель pH. При решении задач будем пользоваться формулой
- •Подготовка к работе
- •Рабочее задание Задание 1. Решение расчётных задач по общим свойствам растворов
- •Задание 2. Проведение практически необратимых реакций двойного обмена
- •Задание 3. Измерение рН раствора электролита и вычисление степени его диссоциации
- •Задание 4. Гидролиз солей
- •Отчёт о выполнении работы включает:
- •Задание для самостоятельной работы
- •Цель работы
- •Теоретические сведения
- •Подготовка к работе
- •Типовые задачи
- •Рабочее задание Задание 1. Влияние реакции среды на окислительные свойства перманганата калия
- •Задание 2. Количественная характеристика электрохимической активности металлов
- •Задание 3. Измерение эдс гальванического элемента
- •Задание 4. Действие разбавленных кислот на металлы
- •Отчёт о выполнении работы включает:
- •Задание для самостоятельной работы
- •Цель работы
- •Теоретические сведения
- •Подготовка к работе
- •Типовая задача 1
- •Типовая задача 2
- •2) Активный анод (медный электрод):
- •Рабочее задание Задание 1. Изучение механизма коррозионных процессов коррозия меди в атмосфере йода
- •Коррозия при контакте двух металлов
- •Коррозия металла в результате различного доступа кислорода
- •Задание 3. Защита металлов от коррозии Защитные свойства металлических покрытий
- •Задание 4. Электролиз водных растворов
- •Отчет о выполнении работы включает:
- •Задание для самостоятельной работы
- •Цель работы
- •Теоретические сведения
- •Молекулы пав обозначены общепринятым символом
- •Подготовка к работе
- •Типовая задача
- •Рабочее задание Задание 1. Получение и стабилизация суспензии мела в воде
- •Задание 2. Получение и стабилизация эмульсии масла в воде
- •Задание 4. Получение золя гидроксида железа (III)
- •Задание 5. Коагуляция коллоидного раствора Fe(oh)3
- •Задание 6. Получение геля кремниевой кислоты
- •Химический анализ Цель работы
- •Теоретические сведения
- •Рабочее задание Задание 1. Качественные реакции обнаружения ионов
- •Отчёт о выполнении работы включает:
- •Задание для самостоятельной работы
- •Цель работы
- •Теоретические сведения
- •Подготовка к работе
- •Рабочее задание Задание 1. Получение углеводородов простой перегонкой нефти
- •Задание 2. Окисление органических соединений
- •Задание 3. Получение высокомолекулярных соединений (полимеров)
- •Задание 4. Химические свойства полимеров
- •А) Реакция каучуков
- •Б) Деполимеризация полиметилметакрилата
- •Отчёт о выполнении работы включает:
- •Задание для самостоятельной работы
- •Заключение
- •Библиографический список
- •394006 Воронеж, ул. 20-летия Октября, 84
Цель работы
▪ Изучить классификацию, методы получения и характерные свойства гетерогенных дисперсных систем.
▪ Установить причины устойчивости и условия коагуляции коллоидных систем.
Теоретические сведения
Гетерогенными называются системы, состоящие из двух (или более) веществ, в которых дисперсная фаза распределена в непрерывной дисперсионной среде.
В отличие от истинных растворов (молекулярных и ионных), являющихся однофазными, равновесными, термодинамически устойчивыми, гетерогенные дисперсные системы (двух- и более фазные) принципиально неустойчивы, однако некоторые из них длительное время могут сохранять устойчивость и не разрушаться.
Причиной принципиальной неустойчивости гетерогенных дисперсных систем (ГДС) является большая свободная поверхностная энергия:
ΔG = σ ∙ S, (11.1)
где σ – удельная свободная поверхностная энергия, называемая поверхно-
стным натяжением на границе раздела: жидкость – газ;
S – общая площадь поверхности всех частиц дисперсной фазы.
Свободная поверхностная энергия самопроизвольно стремится к уменьшению. Если это происходит за счёт уменьшения площади поверхности частиц дисперсной фазы (слипание частиц), то ГДС разрушается.
С другой стороны, уменьшение ΔG за счёт уменьшения поверхностного натяжения приводит к стабилизации ГДС. Это наблюдается за счёт самопроизвольного процесса адсорбции ионов и молекул на границе раздела фаз. Адсорбция – преимущественное концентрирование веществ в поверхностном слое по сравнению с объемом. Вещества, снижающие свободную поверхностную энергию за счёт адсорбции, называются поверхностно-активными (ПАВ).
Органические ПАВ имеют дифильное строение: их молекулы содержат полярные группы (-ОН, -COONa, -NH2 и др.) и достаточно большой углеводородный радикал (рис. 11.1).

-
гидрофобная часть молекулы –
углеводородный радикал R
гидрофильная часть
(– OH, – COONa, –NH2 и др.)
Рис. 11.1. Схема строения молекулы поверхностно-активного вещества
Адсорбция ПАВ влияет на смачивание твёрдой поверхности жидкостью.
ПАВ, имеющие в своём составе гидрофильные и гидрофобные группы, располагаются на межфазной поверхности в соответствии с правилом уравнивания полярностей, таким образом, чтобы полярная часть молекулы была обращена к полярной фазе, а неполярная часть – к неполярной (рис. 11.2).
вода (п) бензол (нп) воздух (нп)
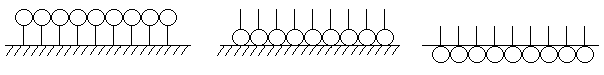
Уголь(нп) глина (п) вода(п)
Молекулы пав обозначены общепринятым символом
Рис. 11.2. Схема адсорбции ПАВ на полярной (п) и неполярной (нп) поверхности
Все полярные гидрофильные поверхности должны хорошо адсорбировать ПАВ из неполярных или слабополярных жидкостей и наоборот.
