
- •Основы наук о жизни
- •Введение
- •Требования к начальным знаниям студентов
- •Требования в области естественнонаучных дисциплин
- •Общие указания к выполнению практическиХ работ
- •Практическая работа № 1 устройство микроскопа и его использование
- •Теоретические положения
- •Практическая работа № 2 строение растительной клетки
- •Теоретические положения
- •Задания
- •1 ‑ Клеточная оболочка; 2 ‑ цитоплазма; 3 ‑ мембрана; 4 ‑ вакуоль;
- •5 ‑ Тонопласт (мембрана вакуоли); 6 ‑ ядро; 7 ‑ ядрышки
- •Задания
- •Результаты наблюдений
- •Классификация ферментов
- •Задания
- •Результаты наблюдений
- •Практическая работа № 5 влияние солей тяжелых металлов на коагуляцию растительных и животных белков
- •Теоретические положения
- •Задания
- •Задания
- •Практическая работа № 7 составление пищевых цепей
- •Теоретические положения
- •Задания
- •Задания
- •Практическая работа № 9 контроль качества питьевой воды
- •Теоретические положения
- •1. Определение запаха воды Задания
- •Характер запаха определите по табл. 12.
- •2. Определение вкуса воды
- •3. Определение цветности воды (интенсивности окрашивания)
- •Задания
- •4. Определение мутности и прозрачности воды
- •Задания
- •Определение прозрачности
- •Задания
- •5. Определение жесткости воды
- •Способы умягчения воды
- •Определение карбонатной жесткости воды
- •Определение общей жесткости воды
- •Определение кальциевой и магниевой жесткости воды
- •Заключение
- •Библиографический список
- •Строение растительной клетки
- •Основные различия животной и растительной клеток
- •Наблюдение плазмолиза и деплазмолиза в живых растительных клетках
- •Основные различия клеток прокариот и эукариот
- •1 ‑ Сужающая пирамида; 2 ‑ перевернутая пирамида
- •Принцип действия фотоэлектроколориметра кфк-2
- •Оглавление
- •Хорохордина Елена Алексеевна, Рудаков Олег Борисович Основы наук о жизни
- •3 94006 Воронеж, ул. 20-летия Октября, 84
Задания
1. Положите лист элодеи на предметное стекло, нанесите на лист каплю пероксида водорода, закройте покровным стеклом и рассмотрите препарат под микроскопом.
2. Положите лист элодеи на предметное стекло, нанесите на лист несколько капель ледяной уксусной кислоты, затем каплю пероксида водорода, закройте покровным стеклом и рассмотрите препарат под микроскопом.
3. Подержите лист элодеи несколько секунд в кипящей воде, затем положите на предметное стекло, нанесите на лист каплю пероксида водорода, закройте покровным стеклом и рассмотрите препарат под микроскопом.
4. Подержите лист элодеи несколько секунд в воде комнатной температуры, нанесите на него каплю пероксида водорода, закройте покровным стеклом и рассмотрите препарат под микроскопом.
5. Положите лист элодеи на предметное стекло, нанесите на лист несколько капель 96%-го этилового спирта, затем каплю пероксида водорода, закройте покровным стеклом и рассмотрите препарат под микроскопом.
6. Результаты наблюдений по каждому пункту задания занесите в табл. 4.
Таблица 4
Результаты наблюдений
Каталитический эффект |
Предварительная обработка реактивами |
|||
Реакция расщепления |
ледяной уксусной кислотой |
водой температуры кипения +100 оС |
водой комнатной температуры |
96%-м этиловым спиртом |
|
|
|
|
|
7. Сделайте вывод об условиях работы каталазы. Повторите опыт по каждому пункту задания, используя лист другого растения.
8. Ответьте на вопросы:
1. Что такое ферменты?
2. В чем выражается специфичность ферментов?
3. Как проявляется активность фермента в живых и мертвых тканях? Почему?
Практическая работа № 5 влияние солей тяжелых металлов на коагуляцию растительных и животных белков
Цель работы: на конкретных примерах изучить действие ионов тяжелых металлов на животные и растительные белки, являющиеся основным строительным материалом клеток живых организмов.
Теоретические положения
Белки – основная структурная единица клеток. Это полимеры, мономерами которых являются аминокислоты. В состав белков входит 20 аминокислот. В каждой из аминокислот содержится аминогруппа (-NH2), карбоксильная группа (-COOH) и радикал (R). Строение радикалов отличается у различных аминокислот. Соединение аминокислот в молекуле белка происходит благодаря образованию пептидной связи: аминогруппа одной аминокислоты соединяется с карбоксильной группой другой аминокислоты:
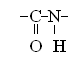
Соединение, состоящее из нескольких аминокислот, называют пептидом. Выделяют первичную, вторичную, третичную и четвертичную структуры белков. Первичная структура белка определяется последовательностью аминокислот в полипептидной цепи. Именно порядок чередования аминокислот в данной белковой молекуле определяет ее особые физико-химические и биологические свойства.
Вторичная структура представляет собой белковую нить, закрученную в виде спирали. Между карбоксильными группами на одном витке спирали и аминогруппами на другом витке возникают водородные связи, которые слабее ковалентных, но при их большом числе обеспечивают образование прочной структуры.
Третичная структура – это клубок (глобула), в который свертывается спираль. Он образуется в результате взаимодействия различных остатков аминокислот. Для каждого белка характерна своя форма (П. 3.1.).
Некоторые белки имеют четвертичную структуру. Она характерна для сложных белков. Несколько глобул объединены и удерживаются вместе благодаря ионным, ковалентным и другим нековалентным связям. Например, белок гемоглобин состоит из четырех глобул, каждая из которых соединена с железосодержащим гемом. Под влиянием внешних факторов (изменение температуры, солевого состава среды, рН, под действием радиации и других факторов) слабые химические связи, поддерживающие молекулу белка (вторичную, третичную, четвертичную структуры), разрываются, при этом изменяются структура и свойства белка.
Этот процесс называется денатурацией. Денатурация может быть обратимой и необратимой. При устранении факторов, вызывающих денатурацию, развернутая полипептидная цепь самопроизвольно закручивается в спираль, а последняя укладывается в третичную структуру. Явление обратимой денатурации белков лежит в основе раздражимости – неотъемлемого свойства всех живых организмов.
Необратимую денатурацию можно наблюдать при нагревании белка куриного яйца: бесцветная жидкость превращается в твердое вещество белого цвета.
Белки бывают простые и сложные. Простые состоят из аминокислот, например, альбумины, глобулины, фибриноген, миозин и др. В состав сложных белков, кроме аминокислот, входят и другие органические соединения, например жиры, углеводы, образуя липопротеиды, гликопротеиды и другие.
Белки выполняют следующие функции:
ферментативную (амилаза расщепляет углеводы);
структурную (входят в состав мембран клетки);
рецепторную (родопсин способствует лучшему зрению);
транспортную (гемоглобин переносит кислород или диоксид углерода);
защитную (иммуноглобулины участвуют в образовании иммунитета);
двигательную (актин, миозин, участвуют в сокращении мышечных волокон);
гормональную (инсулин превращает глюкозу в гликоген);
энергетическую (при расщеплении 1 г белка выделяется 4,2 ккал энергии).
Белки легко осаждаются солями металлов (свинца, меди, серебра, ртути и др.), образуя с ними прочные солеобразные и комплексные соединения. В отличие от высаливания солями щелочных и щелочноземельных металлов для осаждения солями тяжелых металлов требуются небольшие концентрации последних. В случае применения уксуснокислого свинца и СuSO4 избыток солей вызывает растворение образованного ими осадка. Такое растворение вызывается адсорбцией избытка ионов металла и перезарядкой белкового комплекса, вследствие чего в раствор переходит комплекс измененного белка с металлом. Благодаря тому же механизму добавление достаточного количества хлористого натрия вызывает растворение ртутного соединения белка.
Белковые осадки, полученные действием солей тяжелых металлов, нерастворимы в первоначальном растворителе, то есть в воде или слабых растворах солей.
Таким образом, осаждение белков солями тяжелых металлов следует отнести к необратимым реакциям осаждения, связанным с денатурацией белка. Осадки от солей тяжелых металлов, как правило, нерастворимы даже после удаления солей диализом или растворения водой.
Свойством белков связывать тяжелые металлы пользуются в медицинской практике, употребляя белки (молоко, яйца) как противоядие при отравлении солями ртути (сулема), свинца (от недоброкачественной посуды) или меди (от окисления медной посуды), пока эти соли не успели всосаться.
Реакции осаждения белков солями тяжелых металлов идут обычно полно (особенно в присутствии щелочных металлов), и ими пользуются не только для выделения белков из раствора, но и для освобождения жидкостей от белков.
Литература: [1, гл. 2, § 2.1.2]; [2, гл. 2, §2.3.3]; [6, гл. VI, §17].
