
Химические свойства алкадиенов–1,3
Характерными реакциями всех алкадиенов являются реакции присоединения. Наиболее важными среди них являются:
1. Реакции гидрирования.
Эти реакции имеют ступенчатый характер. Варьируя соотношение реагентов, может получать либо алкен, либо алкан в соответствии со схемой
C
 H2=CH-CH2CH3
H2=CH-CH2CH3
CH2=CH-CH=CH2 +H2;[Ni];(((( +H2;[Ni];(((( CH3CH2CH2CH3
CH3CH=CH-CH3
Катализаторами этих реакций являются Ni, Pt, Pd. Особенностью этих реакций является конкуренция 1,4– и 1,2–присоединения. Это связано с наличием двух реакционных центров у поверхностного интермедиата, образующегося в результате реализации механизма реакции
H 2
+ S 2 [H]адс.
2
+ S 2 [H]адс.
C H2=CHCH=CH2 + S [CH2=CHCH=CH2]адс.


![]()
[CH2=CHCH=CH2]адс. + [H]адс.
CH3-CH=CH-CH2 адс.
 [CH3-CH2-CH=CH2]адс.
CH3-CH2-CH=CH2
+ S
[CH3-CH2-CH=CH2]адс.
CH3-CH2-CH=CH2
+ S
![]()
[CH3-CH=CH-CH3]адс. CH3-CH=CH-CH3 + S
где S – свободная поверхность катализатора.
2. Реакции электрофильного присоединения
а) Галогенирование
При реализации этой реакции образуется смесь продуктов 1,2– и 1,4–присоединения, например:
B rCH2CHBrCH=CH2
20% (40oC) 80% (-80 oC)
CH2=CHCH=CH2 + Br2
BrCH2CH=CHCH2Br
80% (40oC) 20% (-80 oC)
Образование продуктов конкурирующего галогенирования объясняется следующим механизмом:
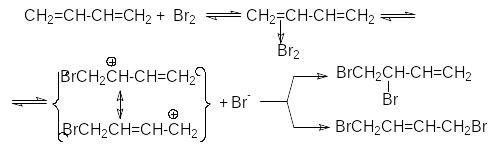
Можно видеть, что промежуточный карбкатион имеет два реакционных центра, что и обусловливает образование продуктов конкурентного галогенирования.
При углублении реакции образуются продукты исчерпывающего галогенирования:
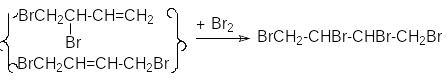
Изменение состава продуктов первичного галогенирования при изменении температуры обусловлено изменением характера факторов, определяющих соотношение продуктов. Так, в области высоких температур конкурирующие реакции быстро достигают положения равновесия, и состав продуктов будет определяться соотношением их равновесных концентраций. Таким образом, в области высоких температур осуществляется термодинамический контроль состава продуктов. В области низких температур из-за высокой экзотермичности каждой из конкурирующих реакций их равновесия существенно смещены в сторону продуктов, а скорости их слишком малы, чтобы заметно приблизиться к состоянию равновесия. Поэтому обе реакции протекают в условиях практической необратимости, когда состав продуктов определяется соотношением их скоростей. Это область кинетического контроля состава продуктов.
Энергетический профиль реакции бромид-аниона с промежуточным карбкатионом иллюстрирует факторы, управляющие такого рода процессами.
М ожно
видеть, что образование продукта
1,4–присоединения термодинамические
более выгодно, т.к. теплота Н1,4
– более электроотрицательна, чем Н1,2.
Поэтому в области термодинамического
контроля предпочтительно образуется
продукт 1,4–присоединения. В то же время
энергетический барьер образования
продукта 1,2–присоединения (Е1,2)
ниже, чем энергетический барьер
образования продукта 1,4–присоединения
(Е1,4).
Поскольку система легче преодолевает
более низкий барьер, то в области
кинетического контроля преобладающим
будет продукт 1,2–присоединения.
ожно
видеть, что образование продукта
1,4–присоединения термодинамические
более выгодно, т.к. теплота Н1,4
– более электроотрицательна, чем Н1,2.
Поэтому в области термодинамического
контроля предпочтительно образуется
продукт 1,4–присоединения. В то же время
энергетический барьер образования
продукта 1,2–присоединения (Е1,2)
ниже, чем энергетический барьер
образования продукта 1,4–присоединения
(Е1,4).
Поскольку система легче преодолевает
более низкий барьер, то в области
кинетического контроля преобладающим
будет продукт 1,2–присоединения.
В целом вероятность термодинамического контроля возрастает с ростом температуры и времени реакции. Наоборот, вероятность кинетического контроля тем больше, чем ниже температура и время реакции.
б) Реакции гидрогалогенирования.
П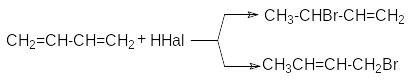 ри
реализации этих реакций образуются
продукты конкурентного галогенирования:
ри
реализации этих реакций образуются
продукты конкурентного галогенирования:
Механизм образования продуктов может быть представлен следующими стадиями:

В области высоких температур состав продуктов определяется термодинамическим контролем и доминирующим продуктом является продукт 1,4–присоединения. В области низких температур состав продуктов определяется кинетическим контролем и основным продуктом является продукт 1,2–присоединения. Таким образом наблюдается полная аналогия между реакциями галогенирования и гидрогалогенирования 1,3-алкадиенов.
в) Полимеризация
Стехиометрически полимеризация сопряженных алкадиенов описывается следующими уравнениями

Полимеризация сопряженных алкадиенов имеет важное практическое значение для синтеза каучуков. Реакция может осуществляться по свободнорадикальному, карбанионному и карбкатионному механизмам в зависимости от типа инициирующей системы. В промышленной практике наиболее широко реализуется стереорегулярная полимеризация под действием катализаторов Циглера-Натта.
Механизм радикальной полимеризации может быть представлен на примере 1,4–присоединения.
Инициирование
I2 2I
Р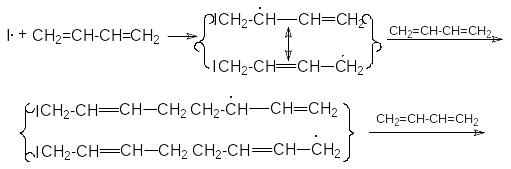 азвитие
цепей
азвитие
цепей
… … …. …. ….. ….
Таким образом, в результате актов многократного присоединения растущего радикала к алкадиену происходит рост цепи будущего полимера. Обрыв цепей осуществляется рекомбинацией или диспропорционированием макрорадикалов. Можно видеть, что растущие радикалы обладают двойственной реакционной способностью, что открывает возможность образования 1,4– и 1,2–полимера. Обычно при свободнорадикальной полимеризации доминирующим является 1,4–полимер с примесью 1,2–полимера, причем первый в основном состоит из транс-изомера. В качестве инициаторов этих реакций используют пероксиды или азобисизобутиронитрил.
В![]() присутствии металлического натрия
осуществляется полимеризация по
анион-радикальному механизму:
присутствии металлического натрия
осуществляется полимеризация по
анион-радикальному механизму:
![]()
Обозначая
м ожно
представить последующий путь полимеризации
совокупностью стадий:
ожно
представить последующий путь полимеризации
совокупностью стадий:
Полимеризация обычно протекает на поверхности металла, поэтому из-за стерических требований к реакции преимущественно образуется 1,2–полимер.
Полимеризация по Циглеру-Натта приводит к образованию стереорегулярного каучука, причем в основном образуются цис-полиалкадиены.
Натуральный каучук представляет собой эластичную при низких температурах, пластичную и клейкую при более высоких температурах массу, которую получают при нагревании млечного сока растений – каучуконосов, таких как гевея. Первое практическое применение натурального каучука нашел Макинтош (1823) – при пропитывании тканей раствором каучука он получил водонепроницаемый материал. Наибольшее значение для широкого использования каучука имело открытие Гудьира (1839). Он обнаружил, что при обработке каучука серой или серосодержащими соединениями получается материал с превосходными механическими свойствами. Так была впервые получена резина. Сера, реагируя по аллильному водороду и двойной связи образует мостики, связывающие между собой полимерные цепи.
Э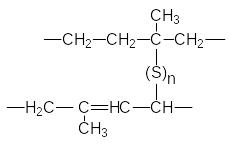 тот
процесс называется вулканизацией. При
исследовании строения натурального
каучука было показано, что он является
полимером изопрена. Позже на основе
рентгеноструктурного анализа было
установлено, что натуральный каучук
имеет строение цис-полиизопрена. В
природе встречается также транс-полиизопрен,
называемый гуттаперчей, который является
твердым хрупким материалом и поэтому
не находит широкого практического
применения.
тот
процесс называется вулканизацией. При
исследовании строения натурального
каучука было показано, что он является
полимером изопрена. Позже на основе
рентгеноструктурного анализа было
установлено, что натуральный каучук
имеет строение цис-полиизопрена. В
природе встречается также транс-полиизопрен,
называемый гуттаперчей, который является
твердым хрупким материалом и поэтому
не находит широкого практического
применения.
В СССР впервые синтетический каучук был получен на основе бутадиена–1,3 при катализе Na или K (1932) – метод С.В. Лебедева.
Промышленная партия стереорегулярного полиизопрена была выпущена у нас в стране в 1963 – так называемый каучук СКИ-3. По своим свойствам этот каучук не уступает натуральному.
В 1956 году под руководством советского химика Долгоплоска был разработан метод стереорегулярной полимеризации 1,3–бутадиена и получения на его основе цис-полибутадиенового каучука (дивинилкаучук, СКД). По эластичности СКД не уступает СКИ-3, но превосходит его в устойчивости при низких температурах и износостойкости.
Спектр практического использования каучуков существенно расширен за счет синтеза сополимеров бутадиена со стиролом, бутадиена с акрилонитрилом и др.
3. Реакции диенового синтеза
Алкадиены–1,3 могут присоединяться к двойной (или тройной) связи с образованием циклического продукта (циклоприсоединение [2+4]).

Такие реакции называются диеновым синтезом или реакцией Дильса-Альдера. Соединения, содержащие двойную или тройную связь и вступающие с 1,3–алкадиенами в реакцию диенового синтеза называются диенофилами. Реакционная способность диенофилов увеличивается при активировании их кратной связи электроноакцепторными группами.
В реакции Дильса-Альдера происходит исчезновение трех старых -связей и появление новых: одной -связи и двух -связей. Поскольку прочность -связей существенно выше, чем прочность -связей реакция Дильса-Альдера экзотермична. Это обусловливает ее обратимость при высоких температурах.
Условием успешного протекания реакции является такая геометрия реагентов, при которой оба конца диена ориентированы на углеродные атомы кратной связи диенофила. При этом происходит согласованный процесс образования новых и разрыва старых связей с синхронным перемещением всех -электронов циклической системы

Поскольку диен может реагировать в s-цисоидной конформации, реакции некоторых диенов являются стерически запрещенными. Примером таких диенов являются приведенные ниже структуры
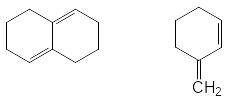
С точки зрения молекулярно-орбитального рассмотрения циклоприсоединение является согласованным, разрешенным по симметрии процессом. Из нижеприведенной молекулярно-орбитальной картины можно видеть, что симметрия ВЗМО бутадиена и НСМО этилена, а также ВЗМО этилена и НСМО бутадиена одинакова. В результате энергия возмущения велика и реакция циклизации может протекать как согласованный процесс.
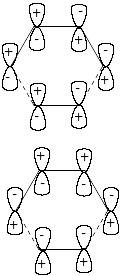
ВЗМО диена (II)
НСМО алкена
НСМО диена (*III)
ВЗМО алкена
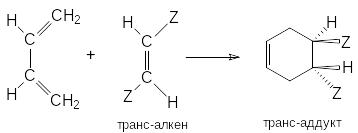
Реакция Дильса-Альдера высокостереоспецифична, что проявляется в сохранении конфигурации диена и диенофила в продукте циклизации. Это наглядно видно на примере цис– и транс–дизамещенных алкенов, используемых в качестве диенофилов:
Области применения диенового синтеза
Р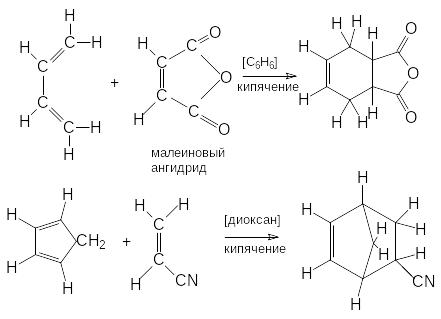 еакция
Дильса-Альдера находит широкое применение
для синтеза сложных соединений. Это
можно проиллюстрировать рядом реакций:
еакция
Дильса-Альдера находит широкое применение
для синтеза сложных соединений. Это
можно проиллюстрировать рядом реакций:
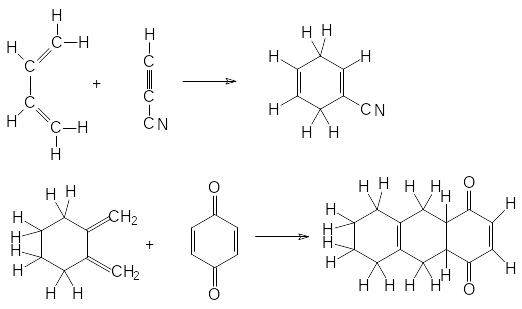
Как правило наиболее реакционноспособными диенофилами являются алкены, у которых двойная связь сопряжена с электроноакцепторными группами. К числу наиболее известных диенофилов относятся следующие соединения
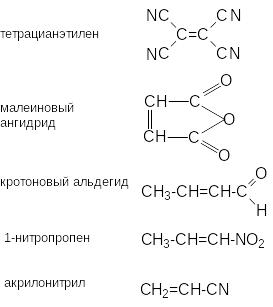
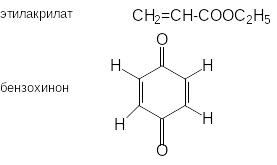
Поскольку комплементарная электронная природа обоих реагентов является главным условием протекания реакции циклоприсоединения, то наиболее реакционноспособными диенами в реакциях с перечисленными диенофилами являются диены, содержащие при двойных связях электронодонорные группы.
1,2-Алкадиены (аллены)
