
- •Лекция 14.Комплексные соединения
- •1.Понятие о комплексном соединении
- •2.Структура комплексных соединений
- •3.Номенклатура комплексных соединений
- •4.Классификация комплексных соединений
- •4.1.Комплексные соединения, содержащие
- •4.2.Комплексные соединения, содержащие ионные лиганды
- •4.3. Циклические комплексные соединения
- •4.4. Многоядерные комплексные соединения
- •5.Изомерия комплексных соединений
- •6.Равновесия в растворах комплексных соединений
- •7.Квантово-механические методы трактовки химической связи в комплексных соединениях
- •7.1. Метод валентных связей
- •7.2. Теория кристаллического поля
- •8.Способность элементов периодической системы к комплексообразованию
- •9. Применение комплексных соединений
8.Способность элементов периодической системы к комплексообразованию
Способность элементов к комплексообразованию зависит от прочности связи, возникающей между атомами комплексообразователя и лигандов. В свою очередь прочность связи в значительной степени определяется электронным строением атома элемента - комплексообразователя, а в конечном итоге положением его в периодической системе.
Следует также учесть, что на результаты взаимодействия комплексообразователя и лигандов оказывает заметное влияние природа лигандов. Комплексообразователь может энергично взаимодействовать с одними лигандами и в то же время вообще не реагировать с другими лигандами, электронная структура которых оказывается не подходящей для этого.
Способность элементов к комплексообразованию, также как и другие их химические свойства, изменяется периодически. У элементов, находящихся в начале периода, эта способность незначительна, потом возрастает и достигает максимума у элементов восьмой В группы. При дальнейшем продвижении в периоде способность к комплексообразованию уменьшается и у благородных газов практически исчезает. В коротких периодах максимальная способность к комплексообразованию также наблюдается у элементов, размещенных в середине периода.
Рассмотрим, например, как изменяется способность к комплексообразованию у элементов в четвертом периоде. Калий практически не образует комплексных соединений. Для кальция известны некоторые комплексы, хотя в целом, он так же малоактивен как комплексообразователь. У скандия, являющегося переходным элементом, способность к комплексообразованию выражена уже гораздо сильнее, чем у кальция.
Известны
комплексные ионы
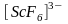 ,
,
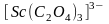 ,
,
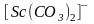 .
.
Элементы:
титан, ванадий, хром и марганец являются
хорошими комплексообразователями и
образуют много различных комплексных
ионов:
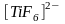 ,
,
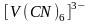 ,
,
 ,
,
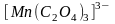 и др.
и др.
Железо,
медь и цинк являются самыми типичными
комплексообразователями. Они образуют
практически все типы комплексных
соединений:
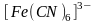 ,
,
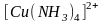 ,
,
 и др.
и др.
Галлий, германий и мышьяк являются еще довольно хорошими комплексообразователями. Однако их способность к комплексообразованию заметно меньше.
У селена способность к комплексообразованию уже значительно меньше, но его комплексные соединения все-таки известны.
Бром является слабым комплексообразователем, а криптон комплексных соединений практически не образует.
С точки зрения электростатической теории (ТКП) большей способностью к комплексообразованию обладают те элементы, которые имеют наиболее выраженную поляризующую способность и одновременно могут сами в значительной степени поляризоваться. Именно такими свойствами обладают переходные металлы (ионы) и, в особенности, металлы восьмой В группы и близких к ней подгрупп.
Метод валентных связей периодическое изменение способности элементов к комплексообразованию объясняет, основываясь на представлениях о гибридизации орбиталей. Наиболее прочные химические связи образуются тогда, когда для этого используются не только s-, р-орбитали, но и d-орбитали. Это успешно реализуется в случае переходных металлов, имеющих частично заполненные d-орбитали.
