
- •5. Основы химической кинетики
- •1) Скорость гомогенных реакций
- •1.1)Закон действующих масс (з.Д.М.)
- •1.2) Молекулярность и порядок реакции
- •1.3) Интегрирование дифференциальных кинетических уравнений
- •1.4) Классификация реакций по степени сложности
- •1.5) Зависимость скорости реакции от температуры.
- •1.6) Принцип а. Ле-Шателье
- •2) Скорость гетерогенных реакций
- •2.1) Скорость растворение твердого тела в жидкости
- •3) Гомогенный и гетерогенный катализ
- •6. Растворы
- •1) Способы выражения концентрации растворов
- •2) Физические и химические процессы при растворении.
- •3.4) Закон распределения и коэффициент распределения
- •4) Законы ф.-м. Рауля. Эбулиоскопия и криоскопия
- •5) Растворы электролитов
- •5.1) Электролитическая диссоциация
- •5.2) Сильные и слабые электролиты. Степень диссоциации и константа диссоциации. Закон разведения Оствальда.
- •7) Гидролиз солей. Константа и степень гидролиза
- •10. Поверхностные явления
- •1) Адгезия, когезия, сорбция: адсорбция и абсорбция. Физическая адсорбция. Хемосорбция. Величина адсорбции
- •2) Механизм адсорбции
- •3) Термодинамика поверхностных явления
- •3.1) Поверхностное натяжение твёрдых тел. Принцип Гиббса-Кюри
- •3.2) Поверхностное натяжение растворов
- •4) Изотерма адсорбции Лэнгмюра, эмпирическое уравнение Фрейндлиха.
- •8. Основы электрохимии
- •1) Электродные потенциалы. Возникновение скачка потенциала на поверхности раздела "металл-раствор". Равновесны потенциал.
- •2) Теория гальванического элемента
- •2.1) Медно-цинковый элемент Якоби-Даниэля
- •2.2) Термодинамика гальванического элемента
- •3) Водородный показатель. Понятие о стандартных потенциалах. Ряд напряжений
- •4) Типы электродов и цепей
- •4.1) Окислительно-восстановительные электроды и цепи
- •5) Электролиз
- •5.1) Общие положения
- •5.2) Последовательность разряда ионов в водных растворах
- •5.3) Количественные законы электролиза (законы м. Фарадея). Удельный расход энергии
- •5.4) Поляризация. Напряжение разложения и перенапряжение
- •5.5) Практические приложение электролиза
- •6) Химические источники тока (хит)
- •6.1) Общие положения
- •6.2) Первичный хит - гальванические элементы
- •6.3) Вторичные хит-аккумуляторы
- •6.4) Топливные элементы
- •9. Коррозия металлов и методы борьбы с ней
- •1) Классификация процессов коррозии
- •2) Химическая коррозия (газовая и жидкостная)
- •3) Гальванокоррозия (микро- и макро)
- •4) Электрокоррозия
- •5) Атмосферная и почвенная коррозия
- •6) Методы борьбы с коррозией
4) Электрокоррозия
При электрокоррозии идет процесс электролиза под действием электрического тока от внешнего источника.
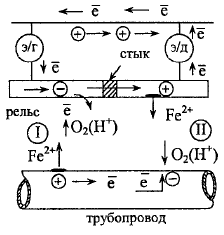 Рассмотрим
коррозию стального трубопровода во
влажной почве под воздействием так
называемых «блуждаощих» токов,
ответвляющихся, например, от рельсов
электрифицированного транспорта,
работающего на постоянном токе
использующего рельсы в качестве обратного
(обычно отрицательного) провода.
Ответвление возможно преимущественно
на стыках, где омическое сопротивление
большое, а изоляция рельсов от грунта
недостаточна. Блуждающие токи могут
возникнуть и от телеграфа (заземление).
Рассмотрим
коррозию стального трубопровода во
влажной почве под воздействием так
называемых «блуждаощих» токов,
ответвляющихся, например, от рельсов
электрифицированного транспорта,
работающего на постоянном токе
использующего рельсы в качестве обратного
(обычно отрицательного) провода.
Ответвление возможно преимущественно
на стыках, где омическое сопротивление
большое, а изоляция рельсов от грунта
недостаточна. Блуждающие токи могут
возникнуть и от телеграфа (заземление).
Возникают два электролизных участка: 1, где рельс (слева от стыка) играет роль катода (-), а участок трубопровода под ним - роль анода (+);
II - справа от стыка, рельс - анод (+), трубопровод- катод (-). Трубопровод как бы электрически подключается параллельно рельсу.
Процессы:
катод
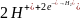 или
или
 ; анод
; анод
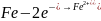 .
.
Слева от стыка разрушается трубопровод, справа - рельс. Электрокор- розии подвергаются водопроводные, газовые, тепловые и др. трубы.
5) Атмосферная и почвенная коррозия
Рассмотрим коррозионное разрушение стальных проводов а атмосферных условиях.
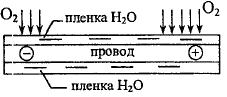 На
проводах адсорбируется влага, причём
количество выпадающей влаги зависит
от относительной влажности воздуха Н.
На
проводах адсорбируется влага, причём
количество выпадающей влаги зависит
от относительной влажности воздуха Н.
Если
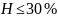 ,
то воздух считается весьма сухим, при
,
то воздух считается весьма сухим, при
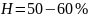 - нормальная влажность, при
- нормальная влажность, при
 - весьма высокая влажность. Заметное
ускорение коррозии у большинства
металлов начинается в интервале
- весьма высокая влажность. Заметное
ускорение коррозии у большинства
металлов начинается в интервале
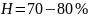 .
.
В адсорбированной влега растворяются CO2 и SO2 , содержащиеся в атмосфере города в больших количествах, влага на поверзности провода превращается в электролит.
Далее получает развитие процесс макрогальванокоррозия с неравномерной аэрацией:
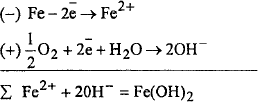
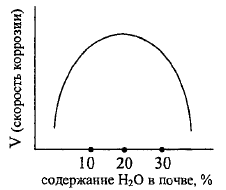
Почвенная коррозия - коррозийное разрушение металлов в почве. Повышенная агрессивность наблюдается у кислых почв. Наименее активны сухие песчаные - с большим омическим сопротивлением.
6) Методы борьбы с коррозией
Методы борьбы с коррозией различны и многообразны:
- Антикоррозийное легирование металла - введение в металл легирующих добавок, чтобы повысить коррозионную стойкость основноп) металла.
- Защитные покрытия.
а) Металлические покрытия (защитные металлы -Zn, Cd, Al, Cr, Sn, Pb, Ni, Си, Ag, Au, Pt): анодные покрытия - металлы менее благородные, чем защищаемый (например, оцинкованное железо); катодные-более (например, белая жесть - железо, покрытое оловом). Защитные металлические покрытия наносятся гальваническим путем, методом горячего покрытия, под давлениием сжатого воздуха - металлизация, диффузионным способом алитирование (в случае Al); путем плакирования, т.е. покрытия листового материала тонким слоем другого материала — с последующим пропусканием через прокатные валки; путем контактного покрыпия ской реакции замещения и т.д. — с использовакием химической реакции замещения и т.д.
б) Неметаллические покрытия - органические и неорганические. К орга- ническим покрытиям относятся всевозможные лаки и краски, покрытие ме- талла резиной (гуммирование), бакелитом, битумом, асфальтом3 предохрани- тельные смазки невысыхающимки минеральными маслами- солидолом или техническим вазелином (при длительном хранении или транспортировке). Неорганические покрытия — эмалирование, торкретирование (покрытие тон- ким слоем бетона-торкретом).
в) Химические покрытия — обработка поверхности защищаемого металла химическими реагентами с целью получения на нем пленки его химического соединения, стойкой против коррози. По своему составу защитные пленки подразделяются на оксидные: оксидирование - термическое (воронение, синение), химическое, анодирование;B фосфатные, хроматные. Применяет- ся также азотирование и цианирование. - Ингибиторы (замедлители) коррозии. С коррозией металлов бо- рются, изменяя химический состав коррозионной среды с целью уменышения агрессивности. Например, добавка к воде десятых долей процента хромата натрия Na2Cr4 заметно снижает скорость коррозии железа и стали. Такое же действие оказывают гексаметафосфат натрия (NaPO3)6. NazSiO3 и NANO2. В случае алюминия- добавки NaSiOз и гексафторсиликата калия
