
- •5. Основы химической кинетики
- •1) Скорость гомогенных реакций
- •1.1)Закон действующих масс (з.Д.М.)
- •1.2) Молекулярность и порядок реакции
- •1.3) Интегрирование дифференциальных кинетических уравнений
- •1.4) Классификация реакций по степени сложности
- •1.5) Зависимость скорости реакции от температуры.
- •1.6) Принцип а. Ле-Шателье
- •2) Скорость гетерогенных реакций
- •2.1) Скорость растворение твердого тела в жидкости
- •3) Гомогенный и гетерогенный катализ
- •6. Растворы
- •1) Способы выражения концентрации растворов
- •2) Физические и химические процессы при растворении.
- •3.4) Закон распределения и коэффициент распределения
- •4) Законы ф.-м. Рауля. Эбулиоскопия и криоскопия
- •5) Растворы электролитов
- •5.1) Электролитическая диссоциация
- •5.2) Сильные и слабые электролиты. Степень диссоциации и константа диссоциации. Закон разведения Оствальда.
- •7) Гидролиз солей. Константа и степень гидролиза
- •10. Поверхностные явления
- •1) Адгезия, когезия, сорбция: адсорбция и абсорбция. Физическая адсорбция. Хемосорбция. Величина адсорбции
- •2) Механизм адсорбции
- •3) Термодинамика поверхностных явления
- •3.1) Поверхностное натяжение твёрдых тел. Принцип Гиббса-Кюри
- •3.2) Поверхностное натяжение растворов
- •4) Изотерма адсорбции Лэнгмюра, эмпирическое уравнение Фрейндлиха.
- •8. Основы электрохимии
- •1) Электродные потенциалы. Возникновение скачка потенциала на поверхности раздела "металл-раствор". Равновесны потенциал.
- •2) Теория гальванического элемента
- •2.1) Медно-цинковый элемент Якоби-Даниэля
- •2.2) Термодинамика гальванического элемента
- •3) Водородный показатель. Понятие о стандартных потенциалах. Ряд напряжений
- •4) Типы электродов и цепей
- •4.1) Окислительно-восстановительные электроды и цепи
- •5) Электролиз
- •5.1) Общие положения
- •5.2) Последовательность разряда ионов в водных растворах
- •5.3) Количественные законы электролиза (законы м. Фарадея). Удельный расход энергии
- •5.4) Поляризация. Напряжение разложения и перенапряжение
- •5.5) Практические приложение электролиза
- •6) Химические источники тока (хит)
- •6.1) Общие положения
- •6.2) Первичный хит - гальванические элементы
- •6.3) Вторичные хит-аккумуляторы
- •6.4) Топливные элементы
- •9. Коррозия металлов и методы борьбы с ней
- •1) Классификация процессов коррозии
- •2) Химическая коррозия (газовая и жидкостная)
- •3) Гальванокоррозия (микро- и макро)
- •4) Электрокоррозия
- •5) Атмосферная и почвенная коррозия
- •6) Методы борьбы с коррозией
6) Химические источники тока (хит)
6.1) Общие положения
Существуют три типа ХИТ - первичные (гальванические элементы), вторичные (аккумуляторы) и топливные элементы.
В гальванических элементах активные вещества, необходимый для работы элемента, закладываются в него при монтаже.
В основу работы аккумулятора положена высоко-обратимая химическая реакция окисления-восстановления, которую можно проводить как в прямом направлении (работа гальванического элемента, переход химической энергии в электрическую), так и в обратном.
Топливный элемент - это ХИТ длительного действия, начинающий и прекращающий работу с началом и прекращением подачи активных веществ к электродам.
6.2) Первичный хит - гальванические элементы
Марганцево-цинковый элемент Лекланше.
Электрохимическая цепь:
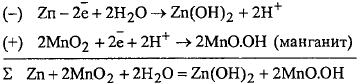 Процессы
при разряде:
Процессы
при разряде:
Оксидно-ртутный элемент (ОРЭ).
Электрохимическая цепь:
Процессы при разряде:
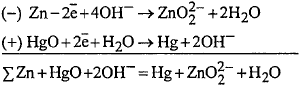
6.3) Вторичные хит-аккумуляторы
Свинцовый (кислотный) аккумулятор.
Гальваническая цепь незаряженного аккумулятора:
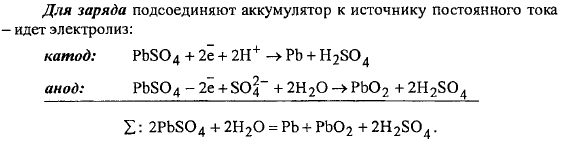
Гальваническая цепь заряженного аккумулятора:
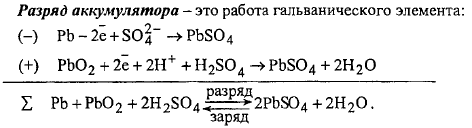
Щелочной железо-никелевый аккумулятор.
Гальваническая цепь незаряженного аккумулятора:
Гальваническая цепь заряженного аккумулятора:
![]()
6.4) Топливные элементы
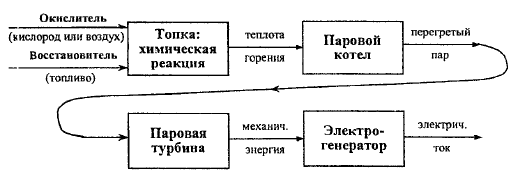
 Более
рациональным представляется другой
путь - превращение химической энергии
топлива непосредственно в электроэнергию,
минуя стадии теплоты и механической
энергии, с помощью топливного элемента:
Более
рациональным представляется другой
путь - превращение химической энергии
топлива непосредственно в электроэнергию,
минуя стадии теплоты и механической
энергии, с помощью топливного элемента:
Топливный элемент - то разновидность гальванического элемента, в котором активным материалом отрицательного электрода может служить топливо, а в качество активного вещества положительного электрода чаще всего используется кислород воздуха или чистый кислород.
Водородно-кислородный топливный элемент.
 На
рисунке: 1 и 2 - соответственно водородный
(-) и кислородный (+) электроды, 3 и 4 -
газовые камеры; 5 - терморегулятор; 6 -
циркуляционный контур для электролита;
7 - электролит.
На
рисунке: 1 и 2 - соответственно водородный
(-) и кислородный (+) электроды, 3 и 4 -
газовые камеры; 5 - терморегулятор; 6 -
циркуляционный контур для электролита;
7 - электролит.

9. Коррозия металлов и методы борьбы с ней
Износ металлических изделий под влиянием механического воздействия среды на поверхность - эрозия.
Коррозия - самопроизвольно протекающий процесс поверхностного окисления металла в результате его химического или электрохимического взаимодейсвия с агрессивной средой.
1) Классификация процессов коррозии
Коррозия подразделяется на химическую и электрохимическую.
Химическая коррозия протекает в средах, не проводящих ток.
Химическая коррозия подразделяется на газовую - разрушение металла в атмосфере сухого газа - окислителя и жидкостную - разрушение металла в жидкостях.
Электрохимическая коррозия подразделяется на гальванокоррозию (микро- и макро) и электрокоррозию. При протекании процесса гальванокоррозии разрушающийся металл является отрицательным электродом самопроизвольно возникающего коррозионного коротко-замкнутого гальванического элемента. Этот коррозионный элемент, работая, сам себя разрушает. Если электроды элемента неразличимы невооруженным глазом, например, име отся многочисленные мельчайшие вкрапления одного металла на поверхности другого металла, то это - микро-гальванокоррозия. Работа тысяч коррозионных микроэлементов дает в совокупности макроэффект разрушения поверхности металла.
Если же в условиях агрессивной среды контактируют два разнорорных металла, имеющих определенную (иногда весьма большую) массу и значительно различающихся по величинам электродных потенциалов, то в данном случае будет протекать процесс макро-гальванокоррозии.
При протекании процесса электрокоррозии разрушающийся металл является анодом самопроизвольно возникающей электролизной цепи, получающей питание от внешнего источника ЭДС за счет блуждающих токов токов утечки.
